
2.下列电离方程式正确的是
A.碳酸溶于水:H2CO3 = HCOO- + H+
B.硫酸氢钠溶于水:NaHSO4 = Na+ + H+ +SO42-
C.碳酸氢钾溶于水:KHCO3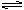 HCO3- + K
HCO3- + K
D.硫化氢溶于水:H2S 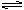 2H+ + S2-
2H+ + S2-
1.下列各组物质的分类组合中,按强电解质、弱电解质、非电解质的顺序排列正确的是
A.NaCl 、HF、 Cl2 B.NaHCO3 、CH3COOH 、CCl4
D.Ba(OH)2、 HCl 、Cu D. H2S 、AgCl、C2H5OH
15.(12分)已知25℃时几种物质的电离度(溶液浓度为0.1mol/L),如下表(已知H2SO4的第一步电离是完全的):
|
①H2SO4溶液中的HSO4- |
②NaHSO4溶液中的 |
③CH3COOH |
④HCl |
|
10% |
29% |
1.33% |
100% |
⑴25℃时, 0.1mol/l上述溶液中c(H+)由大到小的顺序是 。
⑵25℃时c(H+)值相同的上述几种溶液,其物质的量浓度由大到小的顺序是 .
⑶25℃时0.1mol/l H2SO4溶液中HSO4-的电离度小于0.1mol/ NaHSO4溶液中HSO4-的电离的原因 . .
B卷
14.(8分)根据酸碱质子理论,能给出质子的物质是酸,能接受质子的物质子是碱:酸 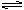 碱 + H+;右边的碱是左边酸的“共轭碱”,反之左边的酸是右边的碱的“共轭酸”。由下式
碱 + H+;右边的碱是左边酸的“共轭碱”,反之左边的酸是右边的碱的“共轭酸”。由下式
HAc 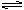 H + + Ac-
H + + Ac-
HCl = H+ + Cl-
NH4+ 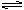 H+ + NH3
H+ + NH3
H2O 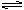 H+ + OH-
H+ + OH-
请推断并写出各酸的共轭碱的化学式为 。按碱性由强到弱的排列顺序为 。
13.(4分)试用简单的实验证明在醋酸溶液中存在着的电离平衡:CH3COOH 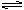 CH3COO-
+ H+,要求写出简单的现象及实验能够说明的问题:
CH3COO-
+ H+,要求写出简单的现象及实验能够说明的问题:
。
12.(10分)已知在次氯酸溶液中存在下列平衡:HClO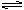 H+ + ClO-,△H>0,请用“向左”“向右”“不移动”“增大”“减小”“不变”填写下表
H+ + ClO-,△H>0,请用“向左”“向右”“不移动”“增大”“减小”“不变”填写下表
|
|
平衡移动方向 |
C(H+) |
n(H+) |
导电能力 |
|
加水稀释 |
|
|
|
|
|
升高温度 |
|
|
|
|
|
加氢氧化钠固体 |
|
|
|
|
|
加次氯酸钠固体 |
|
|
|
|
|
加金属镁 |
|
|
|
|
11.(16分)写出下列物质的电离方程式
①明矾
②氢氧化钡
③熔融态的氧化铝
④石炭酸
10.水的电离过程为H2O 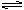 H++OH- ,在不同温度下其平衡常数为K(25℃)=1.0×l0-14,K(35℃)=2.1×l0-14。则下列叙述正确的是
H++OH- ,在不同温度下其平衡常数为K(25℃)=1.0×l0-14,K(35℃)=2.1×l0-14。则下列叙述正确的是
A.c(H+)随着温度的升高而降低 B.在35℃时,c(H+)>c(OH-)
C.水的电离度a(25℃)>a(35℃) D.水的电离是吸热的
9.c(OH-)相同的氢氧化钠溶液和氨水,分别用蒸馏水稀释至原体积的a倍b倍,若稀释后两溶液的c(OH-) 仍相同,则a和b的关系是
A.a>b B.a=b C.a<b D.不能确定
8.在相同温度时100mL0.1mol/L的醋酸溶液与10mL1mol/L的醋酸溶液相比较,下列数值前者大于后者的是
A.中和时所需NaOH的量 B.电离程度
C.H+的物质的量浓度 D.CH3COOH的物质的量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com