
9.(2009·衡水模拟)如图为对10 mL一定物质的量浓度的盐酸X用一定物质的量浓度的NaOH溶液Y滴定的图像,依据图像推出X和Y 的物质的量浓度是下表内各组中的 ( )
的物质的量浓度是下表内各组中的 ( )
|
|
A |
B |
C |
D |
|
X/(mol·L-1) |
0.12 |
0.04 |
0.03 |
0.09 |
|
Y/(mol·L-1) |
0.04 |
0.12 |
0.09 |
0.03 |
答案:D
8.(2009·安徽六校模拟)下列溶液中,说法正确的是 ( )
A.NaHCO3溶液中可以大量存在NO、Al3+、K+、S2-等离子
B.室温下0.1 mol/L的NaOH溶液与pH=1的某酸HA等体积 混合后,溶液中c(Na+)≥c(A-)
混合后,溶液中c(Na+)≥c(A-)
C.1 mol/L的醋酸溶液加水稀释时,溶液中所有离子浓度均减小
D.t℃时,水的离子积常数为KW,则[c(OH)-]2=KW的水溶液一定呈中性
解析:A项中HCO与Al3+因发生水解相互促进反应3HCO+Al3+===Al(OH)3↓+3CO2↑而不共存;B项中若酸HA为弱酸时,反应后剩余的HA因发生电离HAH++A-,使c(Na+)<c(A-),正确关系应为c(Na+)≤c(A-);1 mol/L的醋酸溶液加水稀释时,溶液中c(H+)将减小,而KW=c(H+)·c(OH-)不变,则c(OH-)增大,故A、B、C错误;D项因为KW=c(H+)·c(OH-),若[c(OH)-]2=KW,则c(H+)=c(OH-),故水溶液一定呈中性,正确。
答案:D
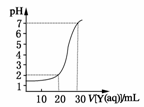
7.(2009·东城模拟)室温时,下列溶液混合后,pH大于7的是 ( )
A.0.1 mol/L的盐酸和pH=13的氢氧化钡溶液体积混合
B.0.1 mol/L的NaHCO3溶液和pH=1的盐酸等体积混合
C.pH=3的硫酸和pH=11的氨水等体积混合
D.pH=1的醋酸和0.1 mol/L的氢氧化钠溶液等体积混合
答案:C
6.用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考如图从下表中选出正确选项 ( )

|
|
锥形瓶 中溶液 |
滴定管 中溶液 |
选用 指示剂 |
选用 滴定管 |
|
A |
碱 |
酸 |
石蕊 |
乙 |
|
B |
酸 |
碱 |
酚酞 |
甲 |
|
C |
碱 |
酸 |
甲基橙 |
甲 |
|
D |
碱 |
酸 |
酚酞 |
乙 |
[答案] C
5.(2009·凤阳模拟)下列四种溶液:①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液。相同条件下,有关上述溶液的比较中,正确的是 ( )
A.由水电离的c(H+):①=②>③=④
B.将②、③两种溶液混合后,若pH=7,则消耗溶液的体积:②>③
C.等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大
D.向等体积的四种溶液中分别加入100 mL水后,溶液的pH:③>④>①>②
解析:加入酸、碱都会抑制水的电离。因CH3COOH、HCl中c(H+)与氨水、NaOH溶液中c(OH-)相同,对水电离的抑制程度相等,所以A错误。将②③混合若pH=7,则消耗溶液的体积②>③,B正确。等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量①最多,C不正确。向等体积的四种溶液中分别加入100 mL水后溶液pH大小关系应为③>④>②>①,D错误。
答案:B
4.(2008·全国卷Ⅱ)取浓度相同的NaOH和HCl溶液,以3∶2体积比相混合,所得溶液的pH等于12,则原溶液的浓度为 ( )
A.0.01 mol/L B.0.017 mol/L
C.0.05 mol/L D.0.50 mol/L
答案:C
3.下列叙述正确的是 ( )
A.无论是纯水,还是酸性、碱性或中性稀溶液,在常温下,其c(H+)·c(OH-)=1×10-14
B.c(H+)等于1×1 0-7mol·L-1的溶液一定是中性溶液
0-7mol·L-1的溶液一定是中性溶液
C.0.2 mol·L-1 CH3COOH溶液中的c(H+)是0.1 mol·L-1CH3COOH溶液中的c(H+)的2倍
D.任何浓度的溶液都可以用pH来表示其酸性的强弱
答案:A
2.水的电离过程为H2OH++OH-,在25℃时水的离子积为:KW=1.0×10-14,在35℃时水的离子积为:KW=2.1×10-14,则下列叙述正确的是 ( )
A.c(H+)随着温度的升 高而降低
高而降低
B.35℃时c(H+)<c(OH-)
C.35℃时的水比25℃时的水电离程度小
D.水的电离是个吸热过程
答案:D
1.(2008·北京高考)对H2O的电离平衡不产生影响的粒子是 ( )
A.H?····? B.26M3+
C.  D.
D.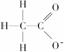
答案:C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com