
6.C 提示:可以用pD一样的定义来规定pOD=-lg(OD-);该温度下Kww=1.6×10-15,则pD+pOD=16-2lg4
5.C 强酸强碱溶液混合,若溶液呈碱性,由pH先换算出混合后溶液的c(OH-),代入公式计算:
c(OH-) = c(碱)V(碱) -c(酸)V(酸) /V(酸)+V(碱)
4.B 提示: 醋酸溶液中可电离出的n(H+)大,反应过程中醋酸溶液中c(H+)大,所以单位时间产生的氢气的体积大,相同时间内醋酸的平均速率大。
3.A
2.C提示: 已知室温时,纯水或稀酸稀碱溶液中Kww=c(H+)·c(OH-)=10-14 ;c(H+)w水=c(OH-)水=Kww/ c(H+)
1.B 提示:强酸溶液pH=a,c(H+)=10-a mol / L,强碱溶液pH=b,c(OH-)=10-(14-b) mol / L
10-a V(酸) = V(碱) 10-(14-b)
19.答:(1) 偏高 (2) 偏高 (3) 无影响(4) 偏高 .(5) 偏低 (6) 偏低
B卷
18.答: (1) 否;若a=3,b=6,溶液显酸性,与题意不符,故a≠3 (2) 否;若a=5,c(H+)a=10-5 mol·L-1,则b=10,c(OH-)b=10-4 mol·L-1,
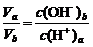 >1,不符合题意,故a≠5
>1,不符合题意,故a≠5
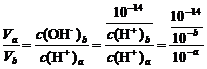 =10(a+b-14)<1
=10(a+b-14)<1
所以(a+b-14)<0,而a=0.5b,即3a<14,a< 。
。
又pH=b=2a>7,a>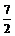 。所以,
。所以,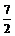 <a<
<a<
17.答:强酸的pH值与强碱的pH值之和等于15。(注:若答“强酸的c(H+)与强碱的c(OH-)之比为1∶10”,以及其它未用pH表达的,均为零分。)
提示:“两种溶液混合后呈中性”是解本题的主要线索。由于10体积强酸溶液与1体积强碱溶液混合后呈中性,可见强酸溶液的浓度小于强碱溶液的浓度,并且是10倍的关系,因此可判断出,两种溶液的pH与pOH的关系,可写出关系式:pHa-1=14-pHb,因此,pHa+pHb=15。
16.答.把一张pH试纸放在表面皿(或玻璃片)上,用蘸有待测溶液的玻璃棒点在试纸的中部,试纸变色后,与标准比色卡比较来确定溶液的pH。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com