
7.(10分)课题式课堂教学是研究性学习的一种方式,其基本教学模式为:
提出课题→确定研究方案→解决问题→总结和评价
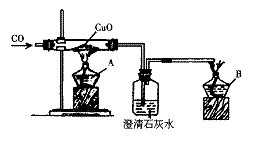
下面关于“一氧化碳的化学性质”的课题式课堂教学中解决问题阶段甲同学设计的证明CO具有还原性的实验装置。
(1)点燃酒精灯A、B的先后顺序为:先_______________后______________。
(2)硬质试管中发生的反应的化学方程式为_______________ _____。
(3)洗气瓶中的实验现象为_____________________________________。
(4)酒精灯B的作用为________________________________。
 (5)乙同学提出甲装置太复杂,可将酒精灯合二为一,去掉B,而将尾气导管出口旋转到A的火焰上即可。乙同学的设计是否合理?_________,简述理由(从A、B使用的一致性的角度考虑)_________________________。
(5)乙同学提出甲装置太复杂,可将酒精灯合二为一,去掉B,而将尾气导管出口旋转到A的火焰上即可。乙同学的设计是否合理?_________,简述理由(从A、B使用的一致性的角度考虑)_________________________。
(6)丙同学认为甲装置有待优化,如尾气可先储存在瓶内,然后再处理。右图是他设计的贮气瓶,尾气应从_________(选a、b填空)口通入。
(7)丁同学质疑:CO能否使澄清石灰水变浑浊?因此,其设计在CO通入CuO之前,应先通入澄清石灰水,以比较排除CO与澄清石灰水反应。试对此作出评价。你认为丁的设计是否必要___________________________,
理由是________________________________________________________。
 w.w.w.k.s.5.u.c.o.
w.w.w.k.s.5.u.c.o.
6.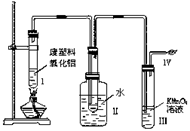 (7分)某研究性学习小组在研究塑料的降解时做了如下实验。装置如图:
(7分)某研究性学习小组在研究塑料的降解时做了如下实验。装置如图:
(1)写出你所知道的生成乙烯的化学方程式
。
(2)Ⅲ中的现象是 ,Ⅳ中的反应方程式是 。
据此现象提出你在治理白色污染方面的设想:
5.(8分)某校化学课外活动小组对实验室两瓶失去标签的白色固体Na2SO4和NH4Cl进行鉴别,经讨论可行的实验方案有多种,请你设计四种实验方案加以鉴别。简要写出操作过程、现象和结论。
|
方案 |
操作过程 |
现象和结论 |
|
① |
|
|
|
② |
|
|
|
③ |
|
|
|
④ |
|
|
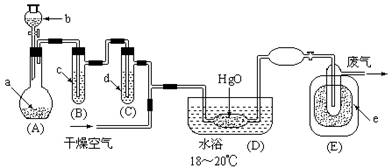
4.(12分)氧化二氯是黄棕色具有强烈刺激性的气体。它的熔点-116℃,沸点3.8℃.氧化二氯不稳定,接触一般有机物易爆炸;它易溶于水(1∶100)同时反应生成次氯酸溶液.制备出之后要冷却为固态才便于操作和贮存。制取少量氧化二氯,是用干燥的氧化汞与氯气反应(还生成HgO·HgCl2)。装置如图,铁架台和夹持仪器已略去。
 部分物质的有关物理数据如下:
部分物质的有关物理数据如下:
|
化学式 |
熔点(单位:℃) |
沸点(单位:℃) |
|
N2 |
-209.86 |
-195.8 |
|
O2 |
-218.4 |
-183 |
|
CO2 |
-57 |
/ |
|
NH3 |
-77.3 |
-33.35 |
|
Cl2 |
-101 |
-34.6 |
试回答: ①A中盛有深色固体试剂a是 ,分液漏斗中b试剂是 。
②B中盛有液体c是 ,C中的液体d是 。
③D中发生化学反应的化学方程式是 。
④E中的保温瓶中盛有致冷剂,它应是 (在干冰、冰水、液态空气、液氨中选择)。在E的内管得到的Cl2O中可能含有的主要杂质是 。
⑤装置A、B、C间的连接方式与D、E间的连接方式有明显的区别,这区别是 ,用这些不同的连接方式的主要理由是 。
3.(7分)用实验确定某酸HA是弱电解质。两同学的方案是:
甲:① 称取一定质量的HA配制0.lmol/L的溶液100mL;
② 用pH试纸测出该溶液的pH值,即可证明HA是弱电解质。
乙:① 用已知物质的量浓度的HA溶液、盐酸,分别配制pH=l的两种酸溶液各100mL;
② 分别取这两种溶液各10mL,加水稀释为100mL;
③ 各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH 1(选填>、<、=)
乙方案中,说明HA是弱电解质的现象是 (多选扣分)
(a)装HCl溶液的试管中放出H2的速率快;
(b)装HA溶液的试管中放出H2的速率快;
(c)两个试管中产生气体速率一样快。
(3)请你评价:乙方案中难以实现之处和不妥之处
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
实验完成后,老师评议说:按上述实验设计,即使G中反应完全、D中吸收完全,也不会得出正确的结果。经讨论,有同学提出在B与G之间加入一个装置。再次实验后,得到了较正确的结果。那么,原来实验所测得的铜的质量分数偏小的原因可能是 ,在B与G之间加入的装置可以是 ,其中盛放的药品是 。
2.(4分)某中学化学小组查阅资料发现金属氧化物A也能催化氯酸钾的分解,且A和二氧化锰的最佳催化温度均为500℃左右。于是对A和二氧化锰的催化性能进行了定量对照实验。实验时均以收满500mL氧气为准(其他可能影响实验的因素均已忽略)。
表一 用MnO2作催化剂
|
实验序号 |
KCIO3质量(g) |
MnO2质量(g) |
反应温度(℃) |
待测数据 |
|
1 |
8.00 |
2.00 |
500 |
|
|
2 |
8.00 |
2.00 |
500 |
|
表二 用A作催化剂
|
实验序号 |
KCIO3质量(g) |
MnO2质量(g) |
反应温度(℃) |
待测数据 |
|
1 |
8.00 |
2.00 |
500 |
|
|
2 |
8.00 |
2.00 |
500 |
|
请回答:上述实验中的待测数据应是 。
完成此研究后,他们准备发表一篇研究报告,请你替他们拟一报告的题目:
|
实验过程 |
实验现象 |
有关化学方程式 |
|
在C中加入样品标本W克,D中装入样品后并称量为m1克。连接好仪器后,检查气密性 |
|
|
|
打开A的活塞,慢慢滴加溶液 |
|
|
|
对G进行加热。当G中药品充分反应后。关闭A的活塞。停止加热 |
|
|
|
冷却后,称量D的质量为m2克。 |
|
|
仪器:天平、分液漏斗、锥形瓶、硬玻璃管、干燥管、酒精灯、洗气瓶等
药品:红褐色铜粉(含炭)样品、过氧化氢溶液、二氧化锰、碱石灰、浓硫酸等
31、(6分)三种气态链烃A、B、C的相对分子质量之比为4:7:11,现将它们按体积之比为11:7:4混合。在标准状况下取该混合气体4.928L充分燃烧,将生成的气体先通过浓硫酸,质量增加9.36g;再通过碱石灰,质量增加16.28g。试推测:
① 原混合烃中C、H元素的质量分别为多少?
②A、B、C的结构简式。

30、(10分)有机粘合剂是生产和生活中一类重要的材料。粘合过程一般是液态的小分子粘合剂经化学反应转化为大分子或高分子而固化。
(1)“502胶”是一种快干胶,其主要成分为α-氰基丙烯酸乙酯(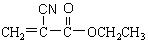 )。在空气中微量水催化下发生加聚反应,迅速固化而将物粘牢。请写出“502胶”发生粘合作用的化学方程式:
)。在空气中微量水催化下发生加聚反应,迅速固化而将物粘牢。请写出“502胶”发生粘合作用的化学方程式:
(2)厌氧胶(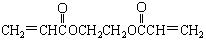 )也是一种粘合剂,在空气中稳定,但在隔绝空气(缺氧)时,分子中双键断开发生聚合而固化。工业上用丙烯酸和某种物质在一定条件下反应可制得这种粘合剂。这一制取过程的化学方程式为
)也是一种粘合剂,在空气中稳定,但在隔绝空气(缺氧)时,分子中双键断开发生聚合而固化。工业上用丙烯酸和某种物质在一定条件下反应可制得这种粘合剂。这一制取过程的化学方程式为
(3)白乳胶是常用的粘合剂,其主要成分为醋酸乙烯酯(CH3COOCH=CH2),它有多种同分异构体,如 。已知含有
。已知含有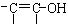 结构的物质不能稳定存在。请另外任写四种含-CH=CH-结构的链状同分异构体的结构简式:
结构的物质不能稳定存在。请另外任写四种含-CH=CH-结构的链状同分异构体的结构简式:
。
(4)已知醇醛反应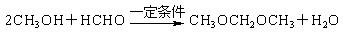 可以发生。聚乙烯醇
可以发生。聚乙烯醇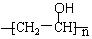 可用做普通胶水,它的羟基可全部与正丁醛缩合脱水,得到含六原子环的强力粘合剂聚乙烯缩丁醛。请写出制取聚乙烯缩丁醛的化学方程式:
可用做普通胶水,它的羟基可全部与正丁醛缩合脱水,得到含六原子环的强力粘合剂聚乙烯缩丁醛。请写出制取聚乙烯缩丁醛的化学方程式:
。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com