
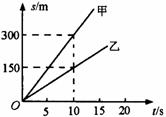
8.(选做)如图所示为在同一直线上运动的甲乙两物体的 图象,则甲物体速度
图象,则甲物体速度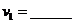 ,
,
乙物体运动速度 s时,甲乙两物体相距________m.
s时,甲乙两物体相距________m.
7.对于各种速率和速度,正确的说法是( )
A.平均速率就是平均速度 B.瞬时速率是即时速度大小
C.匀速直线运动中任意一段时间内的平均速度,都等于其任一时刻的即时速度
D.匀速直线运动中任意一段时间内的平均速度相等
6.某人沿直线做单方向运动,由A到B的速度为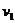 ,由B到C的速度为
,由B到C的速度为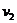 ,若
,若 ,则这全过程的平均速度是( )
,则这全过程的平均速度是( )
A. B.
B.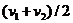
C. D.
D.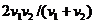
5.物体滑直线运动,下列说法中正确的是( )
A.物体某一秒内的平均速度是5m/s,则物体在这1s内的位移一定是5m
B.物体在第1s末的速度是5m/s,则物体在1s内的位移一定是5m
C.物体在10s内的平均速度是5m/s,则物体在其中1s内的位移一定是5m
D.物体通过某位移的平均速度是5m/s,则物体在通过这段位移一半时的速度一定是2.5m/s
4.下列说法中正确的是( )
A.在匀速直线运动中,v跟s成正比,跟t成反比
B.在匀速直线运动中,各段时间内的平均速度都相等
C.物体在1s内通过的位移与1s的比值叫做这1s的即时速度
D.在直线运动中,某段时间内的位移的大小不一定等于这段时间通过的路程
3.火车以76km/h的速度经过某一段路,子弹以600m/s的速度从枪口射出,则( )
A.76km/h是平均速度 B.76km/h是瞬时速度
C.600m/s是瞬时速度 D.600m/s是平均速度
2.关于平均速度的下列说法中,物理含义正确的是( )
A.汽车在出发后10s内的平均速度是5m/s
B.汽车在某段时间内的平均速度是5m/s,表示汽车在这段时间的每1s内的位移都是5m
C.汽车经过两路标之间的平均速度是5m/s
D.汽车在某段时间内的平均速度都等于它的初速度与末速度之和的一半
1.关于速度的说法正确的是( )
A.速度与位移成正比
B.平均速率等于平均速度的大小
C.匀速直线运动任何一段时间内的平均速度等于任一点的瞬时速度
D.瞬时速度就是运动物体在一段较短时间内的平均速度
8、白色世界
(1)基态:Pb(蓝白色)、Hg、铝粉、大多数块状金属、 PbSO4 、BaSO4 、AgCl 、BaCO3 、 Ba3(PO4)2 、BaSO3 、CaCO3 、 Fe (OH)2 (不稳定)、 Mg (OH)2 、 Al (OH)3 、 ZnS
(2)化学变化:
①H2在Cl2中燃烧呈现苍白色火焰,
②NH3遇 HCl 产生白烟,
③Mg 、 Al在氧气中燃烧发出耀眼的白光
④红磷在氯气中燃烧时产生白色烟雾,
⑤红磷在氧气中燃烧时产生白烟。
[例2]只用一种试剂即可区别NaBr、NaI、NaOH、Na2CO3、NaSCN、H2S、AgNO3、C6H5OH等八种无色溶液,这种试剂为( )
A.硫酸 B.氨水 C.FeCl3溶液 D.盐酸
[解析]FeCl3溶液与NaBr不反应,与NaI反应生成I2产生紫色沉淀,与NaOH生成Fe(OH)3 红褐色沉淀,与Na2CO3产生沉淀和气体,与NaSCN生成血红色溶液,与H2S产生淡黄S沉淀、与AgNO3产生白色沉淀,与C6H5OH显紫色。
答案 C
考点3特殊的除杂方法
特别提醒:在使用常规的方法无法进行除杂操作时,即根据物理方法或化学反应不能将杂质直接除去,可突破定势思维,“一反常规”,将被提纯的物质先转化为其他物质,然后再利用化学反应将其重新还原为被提纯物质,在此过程中杂质即被除去。
[例3] (09届盐城高三联考) 七水硫酸镁(MgSO4·7H2O)在印染、造纸和医药等工业上都有广泛的应用,利用化工厂生产硼砂的废渣-一硼镁泥可制取七水硫酸镁。硼镁泥的主要成分是MgCO3,还含有其他杂质(MgO、SiO2、Fe2O3、FeO、CaO、Al2O3、MnO等)。
表1 部分阳离子以氢氧化物形式完全沉淀时溶液的pH
|
沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Mn(OH)2 |
Mg(OH)2 |
|
pH值 |
5.2 |
3.2 |
9.7 |
10.4 |
11.2 |
表2 两种盐的溶解度(单位为g/100g水)
|
温度 / ℃ |
10 |
30 |
40 |
50 |
60 |
|
CaSO4 |
0.19 |
0.21 |
0.21 |
0.20 |
0.19 |
|
MgSO4·7H2O |
30.9 |
35.5 |
40.8 |
45.6 |
/ |
硼镁泥制取七水硫酸镁的工艺流程如下:

根据以上流程图并参考表格pH数据和溶解度数据,试回答下列问题:
(1)过滤I的滤液中加入硼镁泥,调节溶液的pH=5-6,再加入NaClO溶液加热煮沸,将溶液中的Mn2+氧化成MnO2,反应的离子反应方程式为 _______ 。加热煮沸的主要目的是_ _______ 。
(2)沉淀B中除MnO2、SiO2外还含有 _______ (填化学式)等物质。
(3)检验过滤Ⅱ后的滤液中是否含有Fe3+的实验方法是 _______ ;
(4)沉淀C的化学式是 _______ 。过滤II需趁热过滤的理由是 _______
[解析]向硼镁泥中加硫酸时MnO2、SiO2不溶解,PH=5-6时Fe(OH)3 、 Al(OH)3也会沉淀,加热煮沸的主要目的是促进Al3+、Fe3+水解及Mn2+氧化成MnO2 ,由于MgSO4的溶解度不大,温度低时结晶析出,所以过滤II需趁热过滤。
答案:(1)Mn2++ClO-+H2O=MnO2↓+2H++Cl-
促进Al3+、Fe3+水解及Mn2+氧化成MnO2 (2)Fe(OH)3 Al(OH)3
(3)取过滤II后的滤液1-2 ml于试管中,加入少量KSCN溶液,如果溶液不显红色,证明滤液中无Fe3+
(4)CaSO4·2H2O或CaSO4 以防MgSO4在温度低时结晶析出。
7、紫色世界
(1)基态:KMnO4 (H+)、紫色石蕊、碘单质呈紫黑色
(2)激发态:充氩气的灯光呈紫蓝色,钾元素的焰色呈紫色(透过蓝色钴玻璃观察)
(3)化学变化:
①I2 升华生紫烟,
②NH4I受热生紫烟,
③紫色石蕊在(5.0<pH<8.0)溶液中呈紫色,
④锌粉与碘的混合物中滴入水会生紫烟(反应放热使碘升华)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com