
1.0×10-a mol·L-1和是1.0×10-b mol·L-1,在此温度时,水的离子积为1.0×10-(b+a)
10.下列叙述正确的是
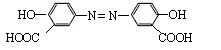
A.1 mol奥沙拉嗪 ( ) 与足量Na2CO3溶液反应能生成4 mol CO2
B.已知反应mX(g)+nY(g)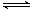 qZ(g)
,若平衡时X、Y的转化率相等,说明反应开始时X、Y的物质的量之比为1∶1
qZ(g)
,若平衡时X、Y的转化率相等,说明反应开始时X、Y的物质的量之比为1∶1
C.1 L 1 mol/L Na2CO3溶液中含有3×6.02×1023个离子
D.在一定温度下,相同pH的硫酸和硫酸铁溶液中水电离出来的c(H+)分别是
9.下列各组溶液中,只用括号内的试剂及物质间相互反应无法鉴别的一组是
A.Ba(OH)2、KSCN、NaCl、K2SO4(FeCl3溶液)
B.NaNO3、NaHCO3、Na2SO3、Na2SiO3(H2SO4溶液)
C.NaBr、HCl、KI、CaCl2(AgNO3溶液)
D.NH4Cl、Mg(NO3)2、CuSO4、AlCl3(KOH溶液)
8.下列是某同学对相应反应的离子方程式所作的评价,其中合理的是
|
编号 |
化学反应 |
离子方程式 |
评价 |
|
A |
碳酸钙与醋酸反应 |
CO32-+2CH3COOH = CO2↑+H2O+2CH3COO- |
错误,碳酸钙是弱电解质,不应写成离子形式 |
|
B |
甲醛和足量银氨溶液充分反应 |
 HCHO+2Ag(NH3)2+
+2OH- HCHO+2Ag(NH3)2+
+2OH-HCOO 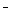 +NH +NH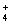 +2Ag↓+H2O +2Ag↓+H2O |
正确 |
|
C |
NaHSO3溶液的水解 |
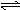 HSO3-+H2O
SO32-+H3O+ HSO3-+H2O
SO32-+H3O+ |
错误,水解方程式写成了电离方程式 |
|
D |
等物质的量的FeBr2和Cl2反应 |
2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
错误,Fe2+与Br-的物质的量之比与化学式不符 |
7.阿伏加德罗常数为NA,下列说法中不正确的是
A.足量Zn与一定量的浓硫酸反应,产生22.4 L(标况)气体时,转移的电子数一定为2NA
B.2 mol SO2和1 mol O2 混合在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数大于2 NA
C.71g氯气通入足量水中,反应中转移的电子总数为NA
D.6 g SiO2晶体中含有的硅氧键数为0.4NA
6.下列有关化学用语使用正确的是
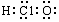 A.质量数为37的氯原子:
A.质量数为37的氯原子: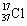 B.次氯酸分子的电子式:
B.次氯酸分子的电子式:
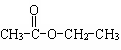
C.乙酸乙酯的结构式:
D.Al(OH)3的电离:H+ + AlO2- +
H2O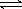 Al(OH)3
Al(OH)3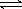 Al3+
+3OH-
Al3+
+3OH-
5.下述实验不能达到预期目的的是
|
|
实验内容 |
实验目的 |
|
A |
将AlCl3溶液蒸干灼烧 |
制备Al2O3 |
|
B |
向淀粉水解后的溶液中,依次加入NaOH溶液、新制Cu(OH)2,共热 |
探究水解产物的还原性 |
|
C |
向某溶液中加入稀硫酸,将产生的气体通入澄清石灰水 |
检验该溶液中是否含有CO32- |
|
D |
向H2O2溶液中滴加少量FeCl3溶液 |
探究催化剂对化学反应速率的影响 |
4.下列判断不正确的是
A.微粒半径:S2->K+>F B.沸点:HCl < HF
C.反应速率:Fe加入稀H2SO4中 < Fe加入稀H2SO4和含少量CuSO4的混合溶液中
D.给出质子的能力:CH3COOH>C2H5OH>H2O
3.已知某溶液中存在较多的SO42-、NO3-,则溶液中还可能大量存在的离子组是
A.Fe3+、AlO2-、Cl- B.Na+、NH4+、S2-
C.H+、Cl-、Fe2+ D.Mg2+、Ba2+、Br-
2.下列各组化学式表示分子的是
A.NaCl、H2O、CO2、H2S B.Ne、NH3、P2O5、H2SO4
C.Na2SO4、NH4NO3、PH3、H2S D.Si、S、SO2、CO
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com