
16.(6分)(1)钇(Y)是激光材料和超导材料中的重要元素。其钇矿石成分是Be2YxFeSi2O10。该矿石与过量烧碱共熔后,加水溶解,所得沉淀中有Y(OH)3和Fe2O3(反应时Fe由+2价变成+3价),则x等于 ,若改用氧化物的形式表示其组成,则化学式为 。
(2)把SO2通入Fe(NO3)3溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时若滴入BaCl2溶液,则会产生白色沉淀。在上述变化过程中
溶液由棕黄色变为浅绿色用离子方程式表示为 ,后又由浅绿色变为棕黄色的离子方程式为 。
17(8分)
某无色溶液X,由Na+、Ag+、Ba2+、Al3+、AlO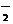 、MnO
、MnO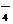 、CO
、CO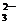 、SO
、SO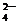 中的若干种离子组成,取溶液进行如下连续实验:
中的若干种离子组成,取溶液进行如下连续实验:
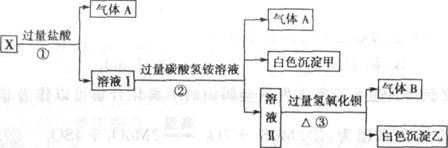
(1)白色沉淀甲是 _________。
(2)X溶液中一定存在的离子是_____________。
(3)可能存在的离子是:______ 证明其是否存在的方法是 。
(4)若将过量的气体A与适量的气体B通入水中,写出反应的离子方程式
15.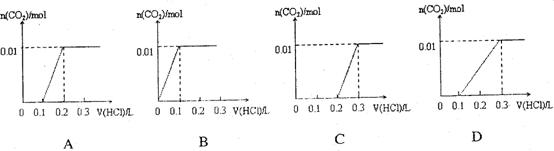 将2.24 L(标准状况下) CO2通入100 mL3 mol/L NaOH溶液后,向溶液中滴加1mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是
将2.24 L(标准状况下) CO2通入100 mL3 mol/L NaOH溶液后,向溶液中滴加1mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是
14.在KI和KIO3混合溶液中通入H2S发生反应后,生成碘、硫酸钾和水,在此反应中被氧化的碘元素与被还原的碘元素的物质的量之比为
A.5:1 B.1:1 C.1:3 D.1:5
13.将2 mol NaHCO3和一定量Na2O2固体混合,在加热条件下让其充分反应,150 ℃下所得气体仅含2种组分,反应后固体的物质的量n的取值范围是
A. 2≤n<3 B.2≤n<4 C.l≤n<3 D.n≥4
12.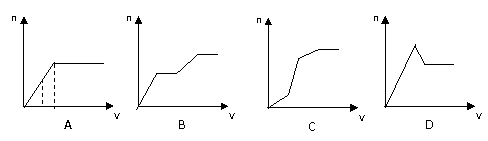 将Ba(OH)2溶液滴入混有盐酸的MgSO4溶液中,若混合液中n(HCl)=n(MgSO4)则下列图像表示合理的是(纵坐标表示沉淀的物质的量,横坐标表示氢氧化钡溶液的体积)
将Ba(OH)2溶液滴入混有盐酸的MgSO4溶液中,若混合液中n(HCl)=n(MgSO4)则下列图像表示合理的是(纵坐标表示沉淀的物质的量,横坐标表示氢氧化钡溶液的体积)
11.在由Fe、FeO和Fe2O3组成的混合物中加入100mL 2mol/L的盐酸,恰好使混合物完全溶解,并放出448mL气体(标准状况),此时溶液中无Fe3+。根据以上信息判断下列说法不正确的是
A. FeO的物质的量无法确定 B. Fe与Fe2O3的物质的量之比为定值C. Fe与Fe2O3的物质的量之差为定值 D.溶液中n(Fe2+)=0.1 mol
10.现有4摩尔铝和足量的盐酸和NaOH溶液,若将铝完全转化为氢氧化铝所需HCl和NaOH的物质的量之和最少为
A 4mol B 6mol C 8mol D 16mol
9.三氧化二铁、氧化亚铜和铜都是红色固体。某校一化学实验小组通过实验来探究某红色固体成分。若固体粉末能完全溶解于稀硫酸且无固体存在,滴加 KSCN 试剂时溶液不变红色
(查阅资料:Cu2O是一种碱性氧化物, Cu+在溶液中不能存在 2Cu+== Cu+ Cu2+)
A. 此固体一定无三氧化二铁 B. 此固体一定是三氧化二铁和铜
C. 此固体可能是三氧化二铁和氧化亚铜 D. 此固体可能是铜和氧化亚铜
8、从海水中提取镁,可按如下步骤进行:①把贝壳制成石灰乳; ②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物; ③将沉淀物与盐酸反应,结晶过滤、在HCl气体氛围中干燥产物; ④将得到的产物熔融电解得到镁。下列说法不正确的是 ( )
A.此法的优点之一是原料来源丰富
B.①②③步骤的目的是从海水中提取MgCl2
C.以上提取镁的过程中涉及化合、分解和复分解反应
D.上述过程中涉及到的分解反应都是氧化还原反应
7.为了提纯下列物质(括号内为杂质),所选用的除杂试剂与分离方法都正确的是( )。
|
选项 |
不纯物质 |
除杂试剂 |
分离方法 |
|
A |
溴乙烷(乙醇) |
水 |
分液 |
|
B |
溴苯(溴) |
NaOH溶液 |
过滤 |
|
C |
Cu(NO3)2溶液(AgNO3) |
铜粉 |
结晶 |
|
D |
K2SO4(K2CO3) |
盐酸 |
蒸发 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com