
10.一定温度下,可逆反应A2(g)+3B2(g) 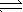 2AB3(g)达到平衡的标志是
2AB3(g)达到平衡的标志是
A.容器内每减少1mol A2,同时生成2mol AB3
B.容器内每减少1mol A2,同时生成3mol B2
C.容器内A2、B2、AB3的物质的量之比为1:3:2
D.容器内A2、B2、AB3的物质的量浓度之比为1:1:1
9.对于任何一个平衡体系,采用以下措施一定会使平衡移动的( )
A.加入一种反应物 B.升高温度
C.对平衡体系增加压强 D.使用催化剂
8.在铁制品上镀上一定厚度的锌层,以下电镀方案中正确的是( )
A.锌作阳极,铁制品作阴极,溶液中含Fe2+
B.锌作阴极,铁制品作阳极,溶液中含Zn2+
C.锌作阴极,铁制品作阳极,溶液中含Fe3+
D.锌作阳极,铁制品作阴极,溶液中含Zn2+
7、氢氧化钠标准溶液因保存不当,吸收了少量的二氧化碳,若有1%的NaOH转变为Na2CO3,以此NaOH溶液滴定未知浓度的盐酸,选用甲基橙作指示剂;盐酸浓度的测定结果会( )
A.偏低1% B.偏高1% C.无影响 D.偏高0.1%
6.1gH2燃烧生成液态水放出142.9KJ的热量,表示该反应的热化学方程式正确的是( )
A. 2H2(g)+O2(g)=2H2O(l) ; ΔH=-142.9kJ·mol-1
B. 2H2(g)+O2(g)=2H2O(l) ; ΔH=-571.6kJ·mol-1
C. 2H2+O2=2H2O ; ΔH=-571.6kJ·mol-1
D. H2(g)+1/2O2(g)=H2O(g) ; ΔH=--285.8kJ·mol-1
5.在25℃、101kPa下,1g乙醇完全燃烧生成CO2和液态水时放热29.72kJ,下列热化学方程式正确的是 ( )
A.CH3CH2OH(l)+3O2(g)=2CO2(g)+ 3H2O(l);△H=+1367kJ/mol
B.2CH3CH2OH(l)+6O2(g)=4CO2(g)+ 6H2O(l);△H=-2734kJ/mol
C.2CH3CH2OH(l)+6O2(g)=4CO2(g)+ 6H2O(l);△H=-1367kJ/mol
D.2CH3CH2OH(l)+6O2(g)=4CO2(g)+ 6H2O(l);△H=+2734kJ/mol
4.汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2 + Pb + 2H2SO4 = 2PbSO4
↓+ 2H2O,根据此反应判断下列叙述中正确的是 ( )
A.PbO2是电池的负极
B.负极的电极反应式为:Pb + SO42-– 2e – = PbSO4↓
C.PbO2得电子,被氧化 D.电池放电时,溶液酸性增强
3.用酸滴定碱时,滴定前读酸式滴定管读数时视线低于水平线,滴定结束时读数正确,这样会使测得的碱溶液的浓度 ( )
A.偏高 B.偏低 C.不受影响 D.不能确定
2.已知450℃时,反应H2(g)+I2(g) 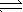 2HI(g)的K=50,由此推测在450℃时,反应
2HI(g)的K=50,由此推测在450℃时,反应
2HI(g) 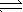 H2(g)+I2(g)的化学平衡常数为
H2(g)+I2(g)的化学平衡常数为
A.50 B.0.02 C.100 D.无法确定
1.一定条件下反应N2(g)+3H2(g) 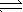 2NH3(g
)在10L的密闭容器中进行,测得2min内,
2NH3(g
)在10L的密闭容器中进行,测得2min内,
N2的物质的量由20mol减小到8mol,则2min内N2的反应速率为
A.1.2mol/(L·min) B.1mol/(L·min)
C.0.6mol/(L·min) D.0.4mol/(L·min)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com