
(三)为了使实验“定量化”、使结果更精确,可以对实验进行如下改进:
1.配制c(H+)相同的稀盐酸和稀硫酸:现有浓度为1mol·L-1的盐酸和密度为1.225g·cm-3、质量分数为20%的硫酸,若要准确量取该硫酸20.00mL,需要用⑤ (填仪器名称);将量取的硫酸配制成c(H+)=1mol·L-1的溶液,可得溶液的体积为⑥ 。
配制溶液时还需要用到的玻璃仪器有⑦ 、烧杯、胶头滴管和量筒等。
2.比较反应速率:反应时间可以用秒表测定。如果要对上述实验中的反应速率进行比较,可以通过测定哪些物理量来确定?要求回答一种即可。⑧ 。
21.(11分) 已知R表示烃基,R/表示烃基或氢原子,
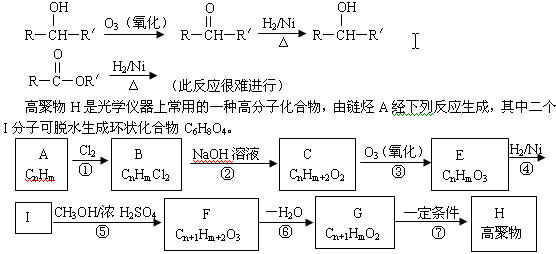
请回答下列问题:
(1)C6H8O4的结构简式是 。
(2)说明下列反应的类型:①是 反应;②是 反应;⑥是 反应。
(3)分别写出反应④、⑤和⑦的化学方程式(有机物用结构简式):
④ ;
⑤ ;
⑦ 。
(二)该同学取了两片等质量、外形和组成相同、表面经过砂纸充分打磨的铝片,分别放入到盛有同体积、c(H+)相同的稀硫酸和盐酸的试管(两试管的规格相同)中:
1.在盛有硫酸的试管中加入少量NaCl或KCl固体,观察反应速率是否变化;
2.在盛有盐酸的试管中加入少量Na2SO4或K2SO4固体,观察反应速率是否变化。
若观察到实验1中③ ,实验2中④ ,则说明原因Ⅲ是正确的。依次类推。该同学通过分析实验现象,得出了结论:Cl-对反应具有加速作用。
(一)该同学认为:由于预先控制了反应的其他条件,那么,两次实验时反应的速率不一样的原因,只有以下五种可能:
原因Ⅰ:Cl-对反应具有促进作用,而SO42-对反应没有影响;
原因Ⅱ:① ;
原因Ⅲ:Cl-对反应具有促进作用,而SO42-对反应具有阻碍作用;
原因Ⅳ:Cl-、SO42-均对反应具有促进作用,但Cl-影响更大;
原因Ⅴ:②
18. 有人认为CH2==CH2与Br2的加成反应,实质是Br2先断裂为Br+和Br-,然后Br+首先与CH2==CH2一端碳原子结合,第二步才是Br-与另一端碳原子结合。已知I2和I-无此类反应。如果让CH2==CH2与Br2在盛有NaCl 和NaI的水溶液中反应,则得到的有机物不可能是()
A.BrCH2CH2Br B. ClCH2CH2I C. BrCH2CH2I D. BrCH2CH2Cl
17.某烃有两种或两种以上的同分异构体,其同分异构体中的某一种的一氯代物只有一种,
则这种烃可能是( )
①分子中具有7个碳原子的芳香烃 ②分子中具有4个碳原子的烷烃 ③分子中具有12个氢原子的烷烃 ④分子中具有6个碳原子的烷烃 ⑤分子中具有8个碳原子的烷烃
A. ①②③ B. ③⑤ C. ③④⑤ D. ②③④⑤
16.下列各组物质中,不能按右图所示关系相互转化的是("→"表示一步完成)( )
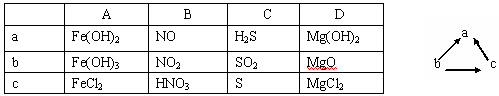
15、下列离子方程式中正确的是( )
A、铁跟稀硫酸反应:2Fe+6H+ = 2Fe3++3H2↑
B、碳酸氢钙溶液跟盐酸反应: Ca(HCO3)2+2H+ = Ca2++2H2O+2CO2↑
C、醋酸跟氢氧化钾溶液反应: CH3COOH+OH- = CH3COO-+H2O
D、碳酸镁跟稀硫酸反应: CO32-+2H+ = Mg2++H2O+CO2↑
14、 人造地球卫星用到的一种高能电池--银锌蓄电池,其电池的电极反应式为Zn + 2OH- - 2e- = ZnO + H2↑,Ag2O + H2O + 2e- = 2Ag+ 2OH-。据此判断氧化银是( )
A、负极,并被氧化 B、正极,并被还原
C、负极,并被还原 D、正极,并被氧化
13、在一定条件下,反应N2+3H2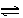 2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为 ( )
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为 ( )
A、V(H2)=0.03mol/(L·min) B、V(N2)=0.005mol/(L·min)
C、V(NH3)=0.17mol/(L·min) D、V(NH3)=0.02mol/(L·min)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com