
11.下列各表为元素周期表中的一部分,表中数字为原子序数,其中M的原子序数为37的
 是
是
10.短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是
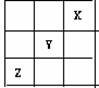
A.Z一定是活泼的金属元素 B.Y的最高价氧化物的水化物是一种强酸
C.1molX的单质跟足量水反应时,发生转移的电子为2mol
D.Y的氢化物稳定性大于Z的氢化物稳定性
9.运用元素周期律分析下面的推断,其中错误的是:①铍(Be)的氧化物的水化物可能具有两性,②铊(Tl)既能与盐酸作用产生氢气,又有跟NaOH溶液反应放出氢气,Tl(NO3)3溶液的酸性 很强,③砹(At)为有色固体,HAt不稳定,AgAt感光性很强,但不溶于水也不溶于稀酸,④锂(Li)在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱,⑤硫酸锶 (SrSO4)是难溶于水的白色固体,⑥硒化氢(H2Se)是无色,有毒,比H2S稳定的气体
A.①②③④ B.②④⑥ C.①③⑤ D.②④⑤
8.在IIA族中,Be是惟一可以生成含氧酸根(铍酸根离子:BeO)的元素,与铍的性质相似的短周期元素是 ( )
A.Na B.Mg C.Al D.Si
7.科学家预测原子序数为114的元素,具有相当稳定性的同位素,它的位置在第7周期IVA族,称为类铅。关于它的性质,预测错误的是
A.它的最外层电子数为4 B.它的金属性比铅强
C.它具有+2、+3、+4价 D.它的最高价氧化物的水化物是强酸
6.两种短周期元素X和Y,可以组成化合物XY3,当Y的原子序数为m时,X的原子序数为:① m-4 ②m+4 ③m+8 ④m-2 ⑤m+6
A.①②④⑤ B.①②③⑤ C.①②③④ D.①②③④⑤
5.元素周期表中前7周期的元素数如下:
|
周 期 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
元素数 |
2 |
8 |
8 |
18 |
18 |
32 |
32 |
请分析周期表与元素数的关系,然后预言第8周期最多可能含有的元素种数是
A.18 B.32 C.50 D.64
4.已知1-18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是
A. 质子数c>b B. 离子的还原性Y2->Z-
C. 氢化物的稳定性H2Y>HZ D. 原子半径X<W
3.下列叙述不正确的是
A.H2S、H2O、HF的稳定性依次增强 B.RbOH、KOH、Mg(OH)2的碱性依次减弱
C.Na+、Mg2+、Al3+的氧化性依次减弱 D.H4SiO4、H2CO3、H2SO4酸性依次增强
2.甲、乙是周期表中同一主族的两种元素,若甲的原子序数为x,则乙的原子序数不可能是
A.x+2 B.x+4 C.x+8 D.x+18
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com