
10、下列关于实验现象的描述不正确的是
A、把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B、用锌片做阳极,铁片做做阴极,电解氯化锌溶液,铁片表面出现一层锌
C、把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D、把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
9、实验室用铅蓄电池作电源电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应: 负极 Pb+SO42-=PbSO4+2e- 正极 PbO2+4H++ SO42-+2e-=PbSO4+2H2O
今若制得Cl2l0.050摩,这时电池内消耗的H2 SO4的物质的量至少是
A、0.025摩 B、0.050摩 C、0.10摩 D、0.20摩
8.铅蓄电池的两极分别为Pb、PbO2,电解质溶液为H2SO4,工作时的反应为Pb+PbO2+2H2SO4===2PbSO4+2H2O,下列结论正确的是
A.Pb为正极被氧化 B.溶液的pH不断减小
C.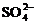 只向PbO2处移动 D.电解质溶液pH不断增大
只向PbO2处移动 D.电解质溶液pH不断增大
7.燃料电池是一种新型电池,它主要是利用燃料在燃烧过程中把化学能直接转化为
电能.氢氧燃料电池的基本反应是:
X极: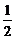 O2(g)+H2O(l)+2e-=2OH- Y极:H2(g)+2OH-=2H2O(l)+2e-
O2(g)+H2O(l)+2e-=2OH- Y极:H2(g)+2OH-=2H2O(l)+2e-
下列判断正确的是
A.X是正极 B.Y是正极 C.Y极发生还原反应 D.Y极发生氧化反应
6.把a、b、c、d四块金属浸泡在稀硫酸中,用导线两两相连可以组成各种原电池.若a、b相连时,a为负极;c、d相连时,c为负极;a、c相连时, c为正极;b、d相连时,b为正极.则这四种金属的活动性顺序由大到小为
A.a>b>c>d B.a>c>d>b C.c>a>b>d D.b>d>c>a
5.如图所示的装置能够组成原电池且产生电流的是
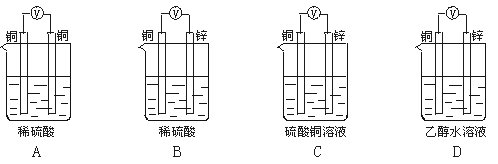
4.已知空气-锌电池的电极反应为:
锌片:Zn+2OH--2e-=ZnO+H2O;碳棒: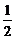 O2+H2O+2e-=2OH-
O2+H2O+2e-=2OH-
据此判断,锌片是
A.正极,并被还原 B.正极,并被氧化C.负极,并被还原 D.负极,并被氧化
3.实验室欲制氢气,所用稀盐酸和稀硫酸的浓度相同,反应速率最快的是
A.纯锌与稀硫酸反应 B.纯锌和浓硫酸反应
C.纯锌与稀盐酸反应 D.粗锌(含铅、铜杂质)与稀硫酸反应
2.银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为:
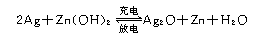
此电池放电时,负极上发生反应的物质是
A.Ag B.Zn(OH)2 C.Ag2O D.Zn
1.有a、b、c、d四种金属,将a与b用导线连结起来浸入电解质溶液中,b不易腐蚀.将a、d分别投入等浓度的盐酸中,d比a反应剧烈.将Cu浸入b的盐溶液里,无明显变化.如果把Cu浸入c的盐溶液里,有c的单质析出.据此判断它们的活动性由强到弱的顺序是
A.d、c、a、b B.d、a、b、c C.d、b、a、c D.b、a、d、c
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com