
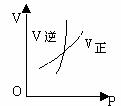
16. 在下列两图中,V表示反应速率,C%表示某反应物在平衡体系中的体积分数,P表示压强,t表示反应时间,图(I)为温度一定时,压强与反应速率的关系曲线;图(Ⅱ)为压强一定时,在不同时间的C%与温度的关系曲线。在下列反应中,同时符合以上两个图象的是20. A
A.4NH3(气)+5O2(气) 4NO(气)+6H2O(气)△H =-808.7kJ·mol-1
4NO(气)+6H2O(气)△H =-808.7kJ·mol-1
B.N2O3(气)  NO2(气)+NO(气) △H =+ 41.8kJ·mol-1
NO2(气)+NO(气) △H =+ 41.8kJ·mol-1
C.3NO2(气)+H2O(液)  2HNO3(液)+NO(气)△H =-261.3kJ·mol-1
2HNO3(液)+NO(气)△H =-261.3kJ·mol-1
D.CO2(气)+C(固) 2CO(气) △H = +171.4kJ ·mol-1
2CO(气) △H = +171.4kJ ·mol-1

|
|
15.化学反应可视为旧键断裂和新键形成的过程。共价键的键能是两种原子间形成1 mol共价键(或其逆过程)时释放(或吸收)的能量。已知H-H键的键能为436 kJ/mol,Cl-Cl键的键能为243 kJ/mol,H-Cl键的键能为431 kJ/mol,则H2(g)+Cl2(g)=2HCl(g)的反应热(ΔH)等于
A. -183 kJ·mol-1 B. +183 kJ·mol-1 C. -862 kJ·mol-1 D. +862 kJ·mol-1
14.强酸与强碱的稀溶液发生中和反应的反应热为:
H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ·mol-1。
分别向1L0.5mol/L的NaOH溶液中加入:①稀醋酸、②浓H2SO4、③稀硝酸,恰好完全反应时的反应热分别为△H1、△H2、△H3,它们的关系正确的是
A.△H1>△H2>△H3 B.△H2<△H3<△H1
C.△H1=△H2=△H3 D.△H1>△H3>△H2
13、2003年10月15日,我国成功地发射了第一个载人航天飞船--“神舟”五号,从此向全世界宣告我国进入航天大国和航天强国。此次发射用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成氮气和水蒸气。已知:N2 (g) + 2O2 (g) = 2NO2 (g); △H =+ 67.7 kJ · mol-1,N2H4 (g) + O2 (g) = N2 (g) + 2H2O (g);△H = -534 kJ · mol-1。下列关于肼和二氧化氮反应的热化学方程式中,正确的是
A. 2N2H4 (g) + 2NO2 (g) = 3N2 (g) + 4H2O (l);△H = -1135.7 kJ · mol-1
B. 2N2H4 (g) + 2NO2 (g) = 3N2 (g) + 4H2O (l);△H = +1135.7 kJ · mol-1
C. N2H4 (g) + NO2 (g) = 3/2N2 (g) + 2H2O (l);△H = -1135.7 kJ · mol-1
D. 2N2H4 (g) + 2NO2 (g) = 3N2 (g) + 4H2O (g);△H = -1135.7kJ · mol-1
12. 某工业生产中发生反应:2A(g)+B(g) 2M(g),△H<0。下列有关该工业生产的说法正确的是
某工业生产中发生反应:2A(g)+B(g) 2M(g),△H<0。下列有关该工业生产的说法正确的是
A.工业上在合成M时,一定采用高压条件,因为高压有利于M的生成
B.物质B价廉易得,因此工业上一般采用加入过量的B,以提高A的转化率
C.工业上一般采用较高温度合成M,因温度越高,反应物的转化率越高
D.工业生产中常采用催化剂,因为使用催化剂可提高M的日产量
11. 根据下列热化学方程式分析,C(S)的燃烧热△H等于
C(S) + H2O(l) === CO(g) + H2(g); △H1 ==175.3KJ·mol-1
2CO(g) + O2(g) == 2CO2(g); △H2 ==-566.0 KJ·mol-1
2H2(g) + O2(g) == 2H2O(l); △H3 ==-571.6 KJ·mol-1
A. △H1 + △H2 -△H3 B.2△H1 + △H2 + △H3
C. △H1 + △H2/2 + △H3 D. △H1 + △H2/2 + △H3/2
9.已知①2C(s)+ O2(g)=2CO(g);△H=-221.0KJ·mol-1 ② 2H2(g) +O 2 (g) = 2H2O(g);△H=-483.6KJ·mol-1,则制备半水煤气的反应C(s)+H2O(g)= CO(g)+ H2(g); △H为
A.+262.6KJ·mol-1 B.-131.3KJ·mol-1
C.-352.3KJ·mol-1 D.+131.3KJ·mol-1
10 已知氟化氢气体中有平衡关系:
2H3F3
 3H2F2 ;△H1= a KJ·mol-1 ; H2F2
3H2F2 ;△H1= a KJ·mol-1 ; H2F2
 2HF ;△H2= b KJ·mol-1
2HF ;△H2= b KJ·mol-1
已知a、b均大于0;则可推测反应:H3F3  3HF的△H3为
3HF的△H3为
A.(a + b) KJ·mol-1 B.(a - b)KJ·mol-1
C.(a + 3b)KJ·mol-1 D.(0.5a + 1.5b)KJ·mol-1
8.已知葡萄糖的燃烧热是2840kJ· mol-1,当它氧化生成1g水时放出的热量是
A.26.0kJ B.51.9kJ C.155.8kJ D.467.3kJ
7.已知
(l)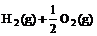 =H2O(g) △H1=a kJ·
=H2O(g) △H1=a kJ·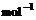
(2)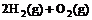 =2H2O(g) △H2=b kJ·
=2H2O(g) △H2=b kJ·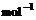
(3)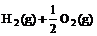 =H2O(l) △H3=c
kJ·
=H2O(l) △H3=c
kJ·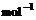
(4) =2H2O(l) △H4=d kJ·
=2H2O(l) △H4=d kJ·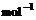
下列关系式中正确的是
A. a<c <0 B.b>d>0 C.2a=b<0 D.2c=d>0
6.已知:CH4(g)+2O2(g)=2H2O(l)+CO2(g);△H= -890.3kJ·mol-1
2H2O(l)=2H2(g)+O2(g); △H= +517.6kJ·mol-1
1g氢气和1g甲烷分别燃烧后,放出的热量之比约是
A.1:3.4 B.1:1.7 C.2.3:1 D.4.6:1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com