
19.可逆反应:A2(?)
+ B2(?) 2AB(?);ΔH=-QkJ/mol,当温度和压强改变时n(AB)的变化如下图,下列叙述正确的是 ( )
2AB(?);ΔH=-QkJ/mol,当温度和压强改变时n(AB)的变化如下图,下列叙述正确的是 ( )
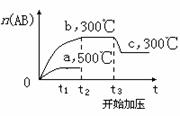
A.A2、B2及AB均为气体,Q>0
B.AB为气体,A2、B2至少有一种为非气体,Q>0
C.AB为气体,A2、B2有一种为非气体,Q<0
D.AB为固体,A2、B2有一种为非气体,Q>0
18.(2005黄冈检测)在一恒定的容器中充人2molA和lmolB发生反应:2A(g)+B(g)  xC(g)达到平衡 后,C的体积分数为α%;若维持容器的容积和温度不变,按起始物质的量A为0.6mol, B为0.3mol,C为1.4mol充入容器中,达到平衡后,C的体积分数仍为α%,则z的值为 ( )
xC(g)达到平衡 后,C的体积分数为α%;若维持容器的容积和温度不变,按起始物质的量A为0.6mol, B为0.3mol,C为1.4mol充入容器中,达到平衡后,C的体积分数仍为α%,则z的值为 ( )
A.只能为2 B.只能为3 C.可能为2,也可能为3 D.无法确定
17. (05年北京西城模拟)一定温度下,向容积恒定的密闭容器中投入2molA和1molB,发生如下可逆反应:2A(g)+B(g)  C(g)+D(s)。达到平衡时,测得压强为原压强的
C(g)+D(s)。达到平衡时,测得压强为原压强的 。则A的转化率为( )
。则A的转化率为( )
A.25% B.40% C.50% D.75%
16.(05年南通调研)已知甲为恒温恒压容器,乙为恒温恒容容器。两容器中均充入2mol SO2、1mol O2,初始时两容器的温度体积相同。一段时间后反应达到平衡,为使两容器中的SO2在平衡混合物的物质的量分数相同,下列措施中可行的是 ( )
A.向甲容器中充入一定量的氦气 B.向乙容器中充入一定量的SO3气体
C.升高乙容器的温度 D.增大甲容器的压强
15.(05年天津河西模拟)在一定温度下发生反应: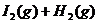

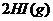 ;
; 并达平衡。HI的体积分数
并达平衡。HI的体积分数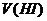 随时间变化如图曲线(II)所示。若改变反应条件,在甲条件下
随时间变化如图曲线(II)所示。若改变反应条件,在甲条件下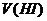 的变化如曲线(I)所示。在乙条件下
的变化如曲线(I)所示。在乙条件下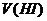 的变化如曲线(III)所示。则甲条件、乙条件分别是
的变化如曲线(III)所示。则甲条件、乙条件分别是

① 恒容条件下,升高温度 ② 恒容条件下,降低温度③ 恒温条件下,缩小反应容器体积④ 恒温条件下,扩大反应容器体积⑤ 恒温恒容条件下,加入适当的催化剂( )
A. ①⑤,③ B. ②⑤,④ C. ③⑤,② D. ③⑤,④
14.(05年南通调研)一定温度下,将2mol A、2mol B、2mol C的气体混合物充入一体积不变密闭容器中,充分反应后恢复到起始温度,测得容器内的压强比起始时增大了20%,则容器中可能发生的反应是 ( )
A.2A+B 2C B.A+B
2C B.A+B 2C C.2A+B
2C C.2A+B C D.A+B
C D.A+B 3C
3C
13. (05年广州三测)在容积一定的密闭容器中,反应2A  B(g) + C(g) 达到平衡后,升高温度容器内气体的密度增大,则下列叙述正确的是
( )
B(g) + C(g) 达到平衡后,升高温度容器内气体的密度增大,则下列叙述正确的是
( )
A. 正反应是吸热反应,且A不是气态 B. 正反应是放热反应,且A气态
C. 其他条件不变,加入少量C,该平衡向逆反应方向移动
D.改变压强对该平衡的移动无影响
12.对于mA(气)+nB(气)  pC(气)+qD(气)的平衡体系,当L高温度时体系的平均
pC(气)+qD(气)的平衡体系,当L高温度时体系的平均
分子量从16.5变成16.9,则下列说法正确的是 ( )
A.m+n>p+q,正反应是放热反应。 B.m+n<p+q,逆反应是放热反应。
C.m+n>p+q,正反应是吸热反应。 D.m+n<p+q,逆反应是吸热反应。
11.对于任何一个平衡体系,采用以下措施,一定会平衡移动的是 ( )
A.加入一种反应物 B.升高温度 C.对平衡体系增加压强 D.使用催化剂
10.在密闭容器中发生反应2SO2+O2  2SO2(气),起始时SO2和O2分别为20mol和10mol,
2SO2(气),起始时SO2和O2分别为20mol和10mol,
达到平衡时,SO2的转化率为80%,若从SO3开始进行反应,在相同的条件下,欲使平衡时各成分的体积分数与前者相同,则起始时SO3的物质的量及SO3的转化率分别为( )
A.10mol和10% B.20mol和20% C.20mol和40% D.30mol和80%
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com