
2. 充电电池
(1)铅蓄电池: 铅蓄电池充电和放电的总化学方程式

放电时电极反应:
负极:Pb + SO42--2e-=PbSO4
正极:___________________________;
(2)氢氧燃料电池:它是一种高效、不污染环境的发电装置。它的电极材料一般为活性电极,具有很强的催化活性,如铂电极,活性炭电极等。
总反应:2H2 + O2=2H2O
电极反应为(电解质溶液为KOH溶液)
负极:________________;
正极:________________;
疑难点拨
1、干电池(锌锰电池)
负极:________________;
正极(石墨):2NH4+ +2e-====2NH3+H2O
H2+2MnO2====Mn2O3+H2O 4NH3+Zn2+==== [Zn(NH3)4]2+
总反应式:________________;
(1)不纯的金属(或合金)在电解质溶液中的腐蚀,关键形成了____,加速了金属腐蚀。
(2) 金属腐蚀的防护: ①改变金属内部组成结构,可以增强金属耐腐蚀的能力。如:不锈钢。②在金属表面覆盖一层保护层,以断绝金属与外界物质接触,达到耐腐蚀的效果。(油脂、油漆、搪瓷、塑料、电镀金属、氧化成致密的氧化膜)。③ 电化学保护法:牺牲活泼金属保护法,外加电流保护法。
根据电池反应设计原电池:(三部分+导线)
(1)负极为___的金属(即化合价__的物质);
(2)正极为_______的金属或___;
(3) 电解质溶液含有________离子(即化合价____的物质)。
2、金属活泼性的判断:
(1)金属活动性顺序表;(2)原电池的负极(电子流出的电极,质量减少的电极)的金属更活泼 ; (3)原电池的正极(电子流入的电极,质量不变或增加的电极,冒气泡的电极)为较不活泼金属
3 原电池的电极反应:
(1) 负极反应:X-ne=Xn- (2) 正极反应:溶液中的阳离子得电子的还原反应
1、原电池:(1)概念:________________。 (2)工作原理:
负极:__电子(化合价___),发生__反应
正极:__电子(化合价__),发生__反应
(3) 原电池的构成条件 :关键是能自发进行的氧化还原反应能形成原电池,a. 有______________作电极; b. 电极均插入____________;c. 两电极______________形成闭合回路。(4)原电池正、负极的判断:负极:_______的电极(较___的金属),金属化合价__;正极:电子__的电极(较___的金属、石墨等):元素化合价__ 。
20.“汽车尾气污染”已备受世人关注。汽车内燃机中,汽油气化后与空气按一定比例混合进入气缸,引擎用电火花点燃。燃烧使汽缸内温度迅速升高,气体体积急剧膨胀,产生压力推动活塞。燃烧时产生污染大气的有害气体通过尾气排出。为简化讨论,以辛烷(C8C18)
代表汽油的成分,并设空气中O2占1/5体积。请回答下列问题:
(1)设辛烷气与空气的体积比(相同条件下)为α。要使辛烷完全燃烧,α的最大值为(用小数表示,设此最大值为α′)_________。
(2)若辛烷气与空气的体积比大于α′,则尾气所含污染大气的有害气体中,相对含量会增多的是(写化学式)_________,产生这种气体的反应方程式是_____________________。
(3)若辛烷气与空气的体积比小于α′,则尾气所含污染大气的有害气体中,相对含量会增多的是(写化学式)_________,产生这种气体的反应方程式是_________。
19.下图是实验室干馏煤的装置图,根据图回答下列问题。
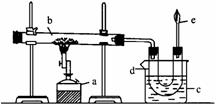
(1)指出图中各仪器的名称:a_________;b_________;c_________;d_________。
(2)装置c的作用是______________________。d中的液体有_________和_________,其中的无机物里溶有_________,可用_________检验出来;有机物可以通过_______________的方法使其中的重要成分分离出来。在170-230℃时可得到_________,加热到230℃以上可以得到_________。
(3)e处点燃的气体是_________,火焰的颜色是_________色。
18.将下图所列仪器组装为一套实验室蒸馏石油的装置,并进行蒸馏,得到汽油和煤油。

(1)图中A、B、C三种仪器的名称是_________。
(2)将以上仪器按(一)→(六)顺序,用字母a,b,c,…表示连接顺序:
e接( );( )接( );( )接( );( )接( );( )接( )
(3)A仪器中c口用于_________,d口用于_________。
(4)蒸馏时,温度计水银球应在_________位置。
(5)在B中注入原油后,加几片碎瓷片的目的是_______________________。
(6)给B加热,收集到沸点为60-150℃间的馏分是_________,收集到150-300℃间的
馏分是_________。
17.对工业“三废”的处理如果不当,则会严重的污染周围环境。工业“三废”指的是 、 和 。化学在工业“三废”治理方面发挥了重要的作用,若对工业“三废”的处理得当,可起到 和 的双重作用,如用石灰乳处理氯碱工业中的废气,则既可以减少 (填气体的化学式)气体对环境的污染,又可以得到漂白粉(有效成分是 )。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com