
13.有A、B和C三种主族元素,若A元素阴离子与B、C元素的阳离子具有相同的电子层结构,且B的阳离子半径大于C的阳离子半径,则这三种元素的原子序数大小次序是
A.B<C<A B.A<B<C
C.C<B<A D.B>C>A
12.超重元素的假说预言自然界中可存在原子序数为114号的稳定同位素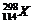 ,试根据原子结构理论和元素周期律预测正确的是
,试根据原子结构理论和元素周期律预测正确的是
A.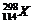 位于第七周期,第ⅣA族 B.X是非金属元素
位于第七周期,第ⅣA族 B.X是非金属元素
C.XO2是酸性氧化物 D.X元素的化合价有+2和+4
11.具有下列电子排布式的原子中,半径最大的是
A.ls22s22p63s23p1 B.1s22s22p3
C.1s22s2sp2 D.1s22s22p63s23p4
10.一个电子排布为1s22s22p63s23p1的元素最可能的价态是
A.+1 B.+2 C.+3 D.-1
9.下列对价电子构型为2s22p5的元素描述正确的是
A.原子半径最小 B.原子序数为7
C.第一电离能最大 D.电负性最大
8.下列各项叙述中,正确的是
A.电子层序数越大,s原子轨道的形状相同、半径越大
B.在同一电子层上运动的电子,其自旋方向肯定不同
C.镁原子由1s22s22p63s2→ls22s22p63p2时,原子吸收能量,由基态转化成激发态
D.原子最外层电子排布是5s1的元素,其氢氧化物不能使氢氧化铝溶解
7.对Na、Mg、Al的有关性质的叙述正确的是
A.碱性:NaOH<Mg(OH)2<Al(OH)3 B.第一电离能:Na<Mg<Al
C.电负性:Na>Mg>Al D.还原性:Na>Mg>Al
6.元素电负性随原子序数的递增而增强的是
A.Na > K > Rb B.N > P > As
C.O > S > Cl D.Si > P > Cl
5.X、Y为两种元素的原子,X的阴离子与Y的阳离子具有相同的电子层结构,由此可知
A.X的原子半径大于Y的原子半径
B.X的电负性大于Y的电负性
C.X的氧化性大于Y的氧化性
D.X的第一电离能小于Y的第一电离能
4.根据对角线规则,下列物质的性质具有相似性的是
A.硼和硅 B.铝和铁 C.铍和铝 D.铜和金
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com