
2.下列给变量赋值的语句正确的是( ▲ )
A.5=a B.a+2=a C.a=b=4 D.a=2*a
1.下列函数求值算法中需要条件语句的函数为( ▲ )
A. 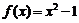 B.
B.
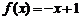
C.  D.
D.
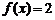
15.⑴ m(Cu)=64 g ⑵c(H2SO4)=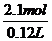 =17.5 mol/L
=17.5 mol/L
14. (1)C Na2SO3 是可溶性固体,不能用具“随开随用”功能的装置 Na2SO3 已部分变质 、硫酸溶液太稀
(2)FeS + H2SO4 = FeSO4 + H2S↑
(3)溶液红色褪去 溶液紫色褪去 有水生成试管壁变模糊,有淡黄色固体生成
(4)吸收尾气(H2S或SO2),避免污染空气
13、H2+S=H2S 、 H2SO3 + 2H2S=3S + 3H2O 、 C+2H2SO4(浓)=CO2 ↑+2SO2 ↑+2H2O
①H2SO3 +2OH- = SO32- + 2H2O ②大于 、 Na2SO3溶液中SO32-发生水解使溶液显碱性 、 ③增大 、升高温度促进Na2SO3溶液的水解
14.某课外学习小组的同学设计了如图的装置,以验证SO2的氧化性、还原性和漂白性。回答以下问题:
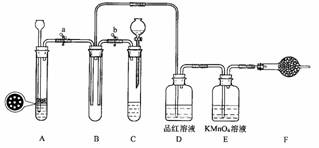
(1)用Na2SO3固体和硫酸溶液制取SO2气体,应选用__________(选“A”或“C”)做气体发生装置,不选用另一装置的理由是 。
小组同学发现产生气体的速率缓慢,可能的原因是 。
(2)课外学习小组的同学用FeS固体和稀硫酸制取H2S气体,
反应的方程式为 ____ 。
(3)SO2气体通过D装置时现象是 ,通过E装置时现象是 ;
SO2与H2S在B装置中反应,现象是_______________________________。
(4)F中盛有碱石灰,其作用是_____________________________________________。
★15.向铜片中加入某浓度的硫酸120 mL,在加热条件下反应,待铜片全部溶解后,将其溶液稀释到500 mL,再加入足量锌粉,使之充分反应收集到标准状况下氢气2.24 L,过滤残留固体,干燥后称量,质量减轻了7.5 g。
(1)求溶解的铜的质量。
(2)求原硫酸的物质的量浓度。
感悟高考:1、B、2、CD
例1:BD 例2:D 例3:C 例4:C
课时作业:
1-12:D、C、A、D、AC、D、 AB、B、D、AC、D、CD
13.下图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件
已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化
合物D是重要的工业原料。

(1)写出A在加热条件下与H2反应的化学方程式
_________________________________________________________________
(2)写出E与A的氢化物反应生成A的化学方程式_______________________
(3)写出一个由D生成B的化学方程式_______________________________;
(4)将5mL0.10mol·L-1的E溶液与10mL0.10 mol·L-1的NaOH溶液混合。
①写出反应的离子方程式________________________________________;
②反应后溶液的pH ______7(填“大于”、“小于”或“等于”),理由是________;
③加热反应后的溶液,其pH________(填“增大”、“不变”或“减小”),理由是_________________ _______________。
12.在200mL0.2mol/LNaOH溶液中,通入一定量三氧化硫气体,在一定条件下蒸发所得溶液,析出的固体物质只有5g,该固体物质的成分可能是
A、Na2SO4 B、NaHSO4 C、NaOH和Na2SO4·10H2O D、NaHSO4和Na2SO4·10H2O
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
|
|
|
|
|
|
|
|
|
|
|
|
|
11.某冶炼厂利用炼铜产生的SO2生产硫酸,变废为宝,化害为利。其原理是
A.利用了SO2的水溶性,将SO2直接通入水中
B.利用了SO2的氧化性,将SO2直接通入水中
C.利用了SO2的氧化性,使其与O2反应而转化为SO3,再与水反应
D.利用了SO2的还原性,使其与O2反应而转化为SO3,再与水反应
10.下列气体溶解于水,没有发生氧化还原反应的是
A.SO2溶解于水 B.NO2溶解于水 C.CO2溶解于水 D.Cl2溶解于水
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com