
14.B化学反应可视为旧键断裂和新键形成的过程。化学
键的键能是形成(或拆开)1mol化学键时释放(或吸收)
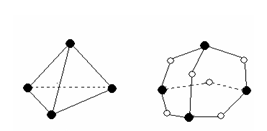
出的能量。已知白磷和P4O6的分子结构如图所示,现提供
以下化学键的键能(kJ·mol-1):P-P:198 P-O:360
O=O:498则反应P4(白磷)+3O2= P4O6
的反应热H为 ( )
A.-1638 kJ·mol-1 B.+1638 kJ·mol-1
C.-126 kJ·mol-1 D.+126 kJ·mol-1
13.B已知
(1) H2(g)+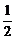 O2(g)=H2O(g) ; DH1=akJ·mol-1
O2(g)=H2O(g) ; DH1=akJ·mol-1
(2) 2H2(g)+O2(g)=2H2O(g) ; DH2=b kJ·mol-1
(3) H2(g)+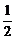 O2(g)=H2O(l) ; DH3=c kJ·mol-1
O2(g)=H2O(l) ; DH3=c kJ·mol-1
(4) 2H2(g)+O2(g)=2H2O(l) ; DH4=d kJ·mol-1
下列关系式中正确的是 ( )
A. a<c<0 B. b>d>0 C. 2a=b<0 D. 2c=d>0
12.B强酸和强碱在稀溶液中的中和热可表示为:
H+(aq)+OH-(aq)=H2O(l); △H= -57.3k kJ·mol-1,又知在溶液中反应有: CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l); △H=-Q1kJ·mol-1, H2SO4(浓)+NaOH(aq)=Na2SO4(aq)+H2O(l) ; △H= -Q2 kJ·mol-1
HNO3(aq)+KOH(aq) KNO3(aq)+H2O(l) ; △H= -Q3 kJ·mol-1,则Q1、Q2、Q3的关系正确的是
( )
KNO3(aq)+H2O(l) ; △H= -Q3 kJ·mol-1,则Q1、Q2、Q3的关系正确的是
( )
A. Q1 = Q2 = Q3 B.Q2 > Q1 > Q3 C. Q2 > Q3 > Q1 D. Q2 = Q3 > Q1
11.B已知胆矾溶于水时溶液温度降低,室温下将1mol无水硫酸铜制成溶液时放出热量为Q1kJ,又知胆矾分解的热化学方程式为CuSO4•5H2O(s) CuSO4(s)+5H2O(l);△H=+Q2 kJ·mol-1则Q1、Q2的关系为
( )
CuSO4(s)+5H2O(l);△H=+Q2 kJ·mol-1则Q1、Q2的关系为
( )
A.Q1<Q2 B.Q1>Q2 C.Q1=Q2 D.无法确定
10. A天然气和液化石油气(主要成分为C3~C5的烷烃)燃烧的化学方程式分别为:
|
|

 CH4+ 2O2 CO2+
2H2O,C3H8+
5O2 CO2+4H2O
现有一套以天然气为燃料的灶具,今改用液化石油气,应采取的正确措施是 ( )
A.增大空气进入量或减小石油气进入量
B.增大空气进入量或增大石油气进入量
C.减小空气进入量或减小石油气进入量
D.减小空气进入量或增大石油气进入量
CH4+ 2O2 CO2+
2H2O,C3H8+
5O2 CO2+4H2O
现有一套以天然气为燃料的灶具,今改用液化石油气,应采取的正确措施是 ( )
A.增大空气进入量或减小石油气进入量
B.增大空气进入量或增大石油气进入量
C.减小空气进入量或减小石油气进入量
D.减小空气进入量或增大石油气进入量
9.A已知25℃、101kPa下,石墨、金刚石燃烧的热化学方程式分别为: C(石墨) + O2(g)=CO2(g);△H=-393.51kJ ·mol-1 C(金刚石) + O2(g)= CO2(g);△H=-395.41kJ ·mol-1 据此判断,下列说法中正确的是 ( ) A.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低 B.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的高 C.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的低 D.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的高
8.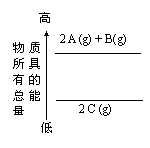 A分析右面的能量变化示意图,下列热化学方程式正确的是
( )
A分析右面的能量变化示意图,下列热化学方程式正确的是
( )
A.2A(g)+ B(g)=2C(g);△H=a(a>0)
B.2A(g)+ B(g)=2C(g);△H=a(a<0)
C.2A + B=2 C;△H=a(a<0)
D.2C=2A +B;△H=a(a>0)
7.A已知充分燃烧a g乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是 ( )
A. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l); ΔH=-2b kJ·mol-1
B. C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l); ΔH=2b kJ·mol-1
C. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l); ΔH=-4b kJ·mol-1
D. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l); ΔH=b kJ·mol-1
6.A在同温同压下,下列各组热化学方程式中,△H2>△H 1的是 ( )
A.2H2(g)+O2(g)=2H2O(g), △H 1;2H2(g)+O2(g)=2H2O(l), △H2
B.S(g)+O2(g)=SO2(g), △H 1;S(s)+O2(g)=SO2(g), △H2
C.C(s)+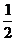 O2(g)=CO(g), △H 1;C(s)+O2(g)=CO2(g), △H2
O2(g)=CO(g), △H 1;C(s)+O2(g)=CO2(g), △H2
D.H2(g)+Cl2(g)=2HCl(g), △H 1;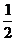 H2(g)+
H2(g)+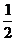 Cl2(g)=HCl(g),△H2
Cl2(g)=HCl(g),△H2
5.A在一定条件下,CO和CH4燃烧的热化学方程式分别为:
2CO(g)+O2(g)=2CO2(g), △H= -566kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l), △H= -890kJ·mol-1由1 mol CO和3 mol CH4组成的混和气在上述条件下完全燃烧时,释放的热量为 ( )
A.2912 kJ B.2953 kJ C.3236 kJ D.3867 kJ
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com