
5.汽车以20m/s的速度做匀速直线运动,刹车后的加速度为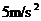 ,那么开始刹车后2s与开始刹车后6s汽车通过的位移之比为( )
,那么开始刹车后2s与开始刹车后6s汽车通过的位移之比为( )
A.1:1 B.3:1
C.3:4 D.4:3
4.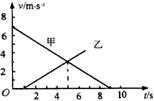 如图所示,是甲、乙两物体的
如图所示,是甲、乙两物体的 图象,由图可知:
图象,由图可知:
A.甲做匀加速运动,乙做匀速运动
B.甲、乙两物体相向运动
C.乙比甲迟1s出发
D.5s末两物体相遇
3.汽车甲沿平直公路以速度v做匀速直线运动,当它路过共处的同时,该处有一辆汽车乙开始做初速为零的匀加速运动去追赶甲车.根据上述已知条件( )
A.可求出乙车追上甲车时乙车的速度
B.可求出乙车追上甲车时乙车所走的路程
C.可求出乙车从开始起动到追上甲车所用的时间
D.不能求出上述三者中的任何一个
2.物体从静止开始做匀加速直线运动,第3s内通过的位移是3m,则( )
A.前3s的位移是6m
B.3s末的速度是3.6m/s
C.3s内平均速度是2m/s
D.第3s内平均速度是3m/s
1.某质点由A经B到C做匀加速直线运动,前2s和后2s位移分别为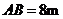 和
和 .该质点的加速度及经B点的瞬时速度分别是( )
.该质点的加速度及经B点的瞬时速度分别是( )
A. 、5m/s B.
、5m/s B.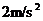 、5m/s
、5m/s
C. 、10m/s D.
、10m/s D.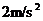 、10m/s
、10m/s
20. (2009
(2009 ·北师附中模拟)丁达尔效应是区分胶体与溶液的一种最常用的方法。
·北师附中模拟)丁达尔效应是区分胶体与溶液的一种最常用的方法。
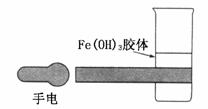
(1)如图是在实验室中进行氢氧化铁胶体丁达尔效应实验的示意图,该图中有一处明显错误是________,原因是_______________________
(试从分散系的分类进行讨论说明)。
(2)欲在树林中观察到丁达尔效应,你认为一天中最有可能观察到该现象的时间是_______,理由是_____________。
(3)去树林观察丁达尔效应有诸多不便,聪明的你想出了许多在家里看到丁达尔效应的方法,其中最简单、
最环保的方法是:_______________________________________________________。
解析:(1)进入烧杯前,光穿过的空气是溶液,不是胶体,不会产生丁达尔效应,所以该图中的明显错误是空气中也出现了光柱。
(2)清晨,水蒸气被太阳加热,形成水雾,可能构成1 nm-100 nm的分散质,阳光透过树叶间隙形成光束,穿过这些水雾会产生丁达尔效应,所以一天中最有可能观察到该现象的时间是清晨。
(3)打开暖瓶(加热水)让水汽升腾起来,用一束光照射即可。
答案:(1)空气中也出现了光柱 进入烧杯前,光穿过的空气是溶液,不是胶体,不会产生丁达尔效应
(2)清晨 水蒸气被太阳加热,形成水雾,可能构成1 nm-100 nm的分散质,阳光透过树叶间隙形成光束,穿过这些水雾会产生丁达尔效应
(3)打开暖瓶(加热水)让水汽升腾起来,用一束光照射即可
19.无机化合物可根据其组成和性质进行分类,
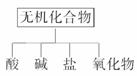
(1)上图所示的物质分类方法名称是___________。
(2)以Na、K、H、O、C、S、N中任两种或三种元素组 成合适的物质,分别填在下表②③⑥的后面。
成合适的物质,分别填在下表②③⑥的后面。
|
物质 类别 |
酸 |
碱 |
盐 |
氧化物 |
|
化学 式 |
①HCl ②____ |
③___ ④Ba(OH)2 |
⑤Na2CO3 ⑥____ |
⑦C O2 O2⑧Na2O2 |
(3)写出⑦转化为⑤的化学方程式_______________________________________。
(4)呼吸面具中用⑧作为O2来源的反应原理为: ______________________________
________________________________________________________________________。
(5)实验室制备⑦常用________和________反应,检验该气体的方法是___________。
答案:(1)树状分类法
(2)②H2SO4(或HNO3)
③NaOH(或KOH)
⑥Na2SO4(或K2CO3或Na2SO3或NaNO3等)
(3)2NaOH+CO2(少量)===Na2CO3+H2O
(4)2Na2O2+2CO2===2Na2CO3+O2,
2Na2O2+2H2O===4NaOH+O2
(5)盐酸 碳酸钙 将气体通入澄清石灰水中,若变浑浊,即可说明是CO2
18.(2009·厦门模拟)“探险队员”--盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或者是水溶液),盐酸必须避开它们,否则就无法通过。

(1)请你帮助它走出迷宫(请用图中物质前的序号连接起来表示所走的路线)。________________________________________________________________________。
(2)在能“吃掉”盐酸的化学反应中,属于酸和碱中和反应的有________个,属于氧化还原反应的有________个,其中能“吃掉”盐酸的盐是________,写出该反应的离子方程式________________________________________________________________________
________________________________________________________________________。
(3)在不能与盐酸反应的物质中,属于电解质的是________(填写物质序号),属于非电解质的是________。
(4)如果将盐酸换成氯气,它能沿着盐酸走出的路线“走出”这个迷宫吗?为什么?
________________________________________________________________________。
解析:(1)图中物质③、⑥、⑩、⑦、⑪、⑫均不与盐酸反应,沿该路线可走出迷宫。
(2)盐酸与NaOH、Ca(OH)2的反应属于酸和碱中和反应,与Zn的反应属于氧化还原反应,能“吃掉”盐酸的盐是Na2CO3,该反应的离子方程式为CO+2H+===CO2↑+H2O。
(3)在不能与盐酸反应的物质中,属于电解质的是H2SO4、NaCl,属于非电解质的是CO2、SO2。
(4)如果将盐酸换成氯气, 它沿着盐酸走出的路线不能“走出”这个迷宫,因为氯气或氯水有强氧化性,遇到二氧化硫、铜时都会发生氧化还原反应从而被“吃掉”。
答案:(1)③⑥⑩⑦⑪⑫
(2)2 1 Na2CO3 CO+2H+===CO2↑+H2O
(3)⑥⑪ ③⑩
(4)不能,因为氯气或氯水有强氧化性,遇到二氧化硫、铜时都会发生氧化还原反应从而被“吃掉”
17.(2009·广州河田中学高三月考)A、B、C三只 烧杯中,依次分别盛有NaOH溶液、KSCN溶液、煮沸的蒸馏水,各滴入FeCl3溶液,试根据实验现象分别回答以下问题:
烧杯中,依次分别盛有NaOH溶液、KSCN溶液、煮沸的蒸馏水,各滴入FeCl3溶液,试根据实验现象分别回答以下问题:
(1)分别写出三只烧杯中形成分散系的名称:A________,B________,C________。
(2)写出A中形成分散系的离子方程式___________________________________。
(3)写出C中形成分散系的化学方程式__________________________________。
解析:FeCl3溶液滴入NaOH溶液中,发生反应:Fe3++3OH-===Fe(OH)3↓,形成悬浊液;FeCl3溶液滴入KSCN中,发生络合反应,生成血红色溶液;FeCl3溶液滴入煮沸的蒸馏水中,发生反应:FeCl3+3H2O(沸水)Fe(OH)3(胶体)+3HCl。
答案:(1)悬浊液 溶液 胶体
(2)Fe3++3OH-===Fe(OH)3↓
(3)FeCl3+3H2O(沸水)Fe(OH)3(胶体)+3HCl
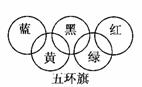
16.(思维拓展题)假定奥运五环旗中的每一环表示一种物质,相连环物质间一定条件下能发生常见反应,不相连环物质间不能发生反应。且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组是 ( )
|
选项 |
蓝 |
黑 |
红 |
黄 |
绿 |
|
A |
SiO2 |
CuSO4 溶液 |
O2 |
NaOH溶液 |
Ag |
|
B |
O2 |
稀H2SO4 |
CO2 |
Fe |
NaOH溶液 |
|
C |
O2 |
稀H2SO4 |
Al(OH)3 |
NH3 |
NaOH溶液 |
|
D |
Mg |
CO2 |
KOH溶液 |
Al |
Fe2O3 |
答案:B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com