
2.事物的现象与本质的区别在于( )
A.现象是事物的表面特征和外部联系,本质是事物相对稳定的内部联系
B.现象是个别的、多变的,本质是永恒不变的 C.现象是主观的,本质是客观的
D.事物的现象是本质的表现
1.感性认识与理性认识的区别在于( )
A.感性认识依赖于实践,理性认识不依赖于实践
B.感性认识是对事物现象的认识,理性认识是对事物本质和规律的认识
C.感性认识是人脑对客观事物的歪曲反映,理性认识是人脑对客观事物的如实反映
D.感性认识对实践没有指导作用,理性认识对实践有指导作用
24.(12分)有机物A的结构简式为:
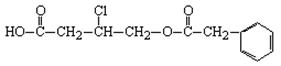
(1)A的分子式为____________________。
(2)A在NaOH水溶液中加热,经酸化得到有机物B和D,D是芳香族化合物。当有1 molA发生反应时,最多消耗_________molNaOH。
(3)B在一定条件下发生酯化反应可生成某五元环酯,该五元环酯的结构简式为___________________________________________________________________。
(4)写出苯环上只有一个取代基且属于酯类的D的所有同分异构体的结构简式 。
(5)D的某同系物在氧气中充分燃烧生成二氧化碳和水,其中n(CO2)∶n(H2O)=3∶2,该同系物的分子式为_______________________。
23.(12分)燃料电池具有广阔的发展前途,科学家近年研制出一种微型的燃料电池,采用甲醇取代氢气做燃料可以简化电池设计,该电池有望取代传统电池。某学生在实验室利用碱性甲醇燃料电池电解Na2SO4溶液。

请根据图示回答下列问题:
(1)图中a电极是 (填“正极”、“负极”、“阴极”或“阳极”)。该电极上发生的电极反应式为 。
(2)碱性条件下,通入甲醇的一极发生的电极反应式为 。
(3)当消耗3.36 L 氧气时(已折合为标准状况),理论上电解Na2SO4溶液生成气体的总物质的量是 mol,电解后溶液的PH____________(填增大、减小或不变)。
(4)25℃、101kPa时,燃烧16g甲醇生成CO2和H2O(l),放出的热量为363.26 kJ,写出甲醇燃烧的热化学方程式: 。
22、 (每空2分,共12分)有X、Y、Z三种单质和甲、乙、丙三种常见的化合物,它们有如下图及叙述所示的关系:
(每空2分,共12分)有X、Y、Z三种单质和甲、乙、丙三种常见的化合物,它们有如下图及叙述所示的关系:
(1)X、Y、Z都是短周期元素的单质,X元素原子的最外层电子数是其次外层电子数的2倍;Y元素有两种常见单质,二者质量相等时其物质的量之比为3 :2;Z元素原子的次外层电子数是其最外层电子数的4倍。则:
①写出化合物甲的电子式___________________;
②写出Z与甲反应的化学方程式_______________________________________________;
(2).X、Y、Z都是非金属单质,X是原子晶体,Y、Z都是分子晶体,X、Y都能与强碱溶液反应;乙的水溶液是工业三酸之一,也是实验室常用试剂。则:
①写出X与NaOH溶液反应的离子方程式________________________________________;
②在①所得溶液中加入乙的溶液,观察到的现象___________________________________
___________________________________ ;
(3).X、Z是常见金属,Z与甲的反应只有在高温下才能进行,甲是一种具有磁性的化合物,乙在工业上常用于制取Z单质。则:
①写出乙与NaOH溶液反应的化学方程式______________________ ;
②将等物质的量的X和Z分别与足量的稀硫酸反应,当两种金属完全溶解后,得到气体的质量之比是____________________________。
21.(12分)工业上用铝土矿(主要成分为Al2O3、Fe2O3、SiO2)提取氧化铝做冶炼铝的原料,提取的操作过程如下:

(1)第一步在铝土矿中加入盐酸后的实验基本操作是 ,若在固体B中加入氢氧化钠溶液 (填”会”或”不会”)发生反应,若会,则写出反应的离子方程式
(2)验证滤液A中是否含Fe3+,可取少量滤液A并加入 (填试剂名称),现象是 。
(3)写出碳酸氢钠的一种用途 。
20.已知NH3难溶于CCl4,如下图所示,下列装置中,不宜用于氨气吸收的是( )

第Ⅱ卷(非选择题 共48分)
19.将 0.2mol MnO2和50mL 12mol/L 盐酸混合后缓缓加热,反应完全后留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀的物质的量为(不考虑盐酸的挥发)( )
A、0.3mol B、小于0.3mol C、大于0.3mol,小于0.6mol D、以上都不正确
18.在允许加热的条件下,只用一种试剂就可以鉴别氯化钠、氯化镁、硫酸铵、硫酸铝和硫酸铁溶液,这种试剂是 ( )
A、AgNO3 B、BaCl2 C、NaOH D、NH3·H2O
17.某有机小分子化合物含有C、H、O、N四种元素,该有机物可能是( )
A、脂肪 B、蛋白质 C、葡萄糖 D、氨基酸
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com