
29.根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
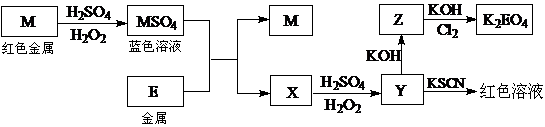
(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式: 。
(2)某同学取Y的溶液,酸化后加入KI、淀粉溶液,变为蓝色。写出与上述变化过程相关的离子方程式: 。
(3)写出Cl2将Z氧化为K2EO4的化学方程式: 。
28.已知: ① X是由短周期元素组成的气体单质,Y是含X元素的一种常用消毒剂。
② A、B、C、D、E、F都是化学中常见化合物,常温下C是气体,D是液体。
③ 自然界中存在较多的E矿石,工业上可用这种矿石为原料制取F,同时有温室气体C生成。
④ 存在如下转化关系:
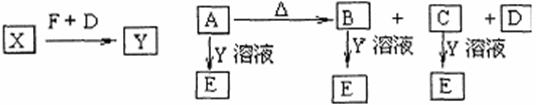
试回答:(1)写出C的电子式____ ____。
(2)写出C跟Y溶液反应的离子方程式__ ____。
(3)写出X转化为Y的化学方程式_______ __ _____。
27.在说明催化剂对反应速率的影响时,采用了双氧水( H2O2 )和MnO2 的反应,据此回答下列各小题。
(1)完成该反应的化学方程式: ,
(2)此反应能否用于实验室制O2 ?答: (回答“能”或“不能”),
(3)完成下列反应的化学方程式:MnO2作催化剂(上述除外): ,
MnO2作氧化剂(写出二个方程式,其中一个为置换反应): 、 。
(4)如下三个反应,其中E为黑色氧化物,B、C为气体单质:
2KClO3 + 2E = 2A + B↑+ C↑ 2A = D + E + C↑ D + B = 2KCl + E + C↑
则总的反应的化学方程式是: ,
26.硅单质及其化合物应用范围很广。请回答下列问题:
(1)制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:
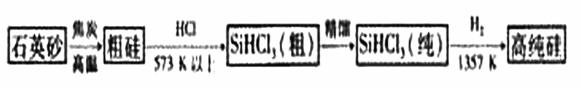
① 写出由纯SiHCl3制备高纯硅的化学反应方程式 。
② 整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式 ;H2还原SiHCl3过程中若混有02,可能引起的后果是爆炸。
(2)硅酸钠水溶液俗称水玻璃。取少量硅酸钠溶液于试管中,逐滴加入饱和氯化铵溶液,振荡。写出实验现象并用化学方程式给予解释 ;
再取少量硅酸钠溶液于试管中,暴露于空气中会出现沉淀,发生反应的化学方程式是:
;静置后又取上层的澄清溶液于另一个试管中,加入稀盐酸,出现沉淀和气体,发生反应的化学方程式是: 、 。
25.下图所示为减压过滤装置,回答有关问题。
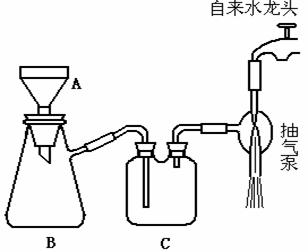
(1)写出图中A、B二种仪器的名称,A ;B 。
(2)该装置图有几处错误,请指出错误并加以改正(最少二处)
① ;② ;
24.某烃类化合物A的质谱图表明其相对分子质量为84,
红外光谱表明分子中含有碳碳双键,
核磁共振谱表明分子内所有氢原子都处于相同的化学环境,
由此推测
(1)A的结构简式为 ;
(2)A中的碳原子是否都处于同一平面? (填“是”或者“不是”)。
23.某有机样品3.1 g完全燃烧,燃烧后的混合物通入过量的澄清石灰水,石灰水共增重7.1 g,经过滤得到10 g沉淀。该有机样品可能是
A.乙二醇 B.乙醇 C.乙醛 D.甲醇和丙二醇的混合物
22.下列由事实得出的结论错误的是
A.维勒用无机物合成了尿素,突破了无机物与有机物的界限
B.门捷列夫在前人工作的基础上发现了元素周期律,表明科学研究既要继承又要创新
C.C60 是英国和美国化学家共同发现的,体现了国际科技合作的重要性
D.科恩和波普尔因理论化学方面的贡献获诺贝尔化学奖,意味着化学已成为以理论研究为主的学科
21.下列叙述合理的是
A.金属材料都是导体,非金属材料都是绝缘体
B.棉、麻、丝、毛及合成纤维完全燃烧都只生成 CO2 和H2O
C.水电站把机械能转化成电能,而核电站把化学能转化成电能
D.我国规定自 2008年 6 月 1 日起,商家不得无偿提供塑料袋,目的是减少“白色污染”
20.高温下,某反应达平衡,平衡常数K= , 恒容时,温度升高,H2 浓度减小。下列说法正确的是
A.该反应的焓变为正值
B.恒温恒容下,增大压强, H2 浓度一定减小
C.升高温度,逆反应速率减小
D.该反应的化学方程式为 CO
+ H2O CO2 + H2
CO2 + H2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com