
5. 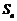 是数列
是数列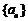 的前
的前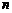 项和,则“数列
项和,则“数列 为等差数列”是“数列
为等差数列”是“数列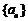 为常数列”的(B)
为常数列”的(B)
A.充分不必要条件 B.必要不充分条件
C.充分必要条件 D.既不充分也不必要条件 

解析:数列 为等差数列,当
为等差数列,当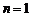 时,
时,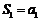 ,当
,当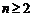 时,
时,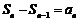 为常数,则数列
为常数,则数列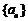 不一定为常数列,例如1,2,2,2,…;反过来,数列
不一定为常数列,例如1,2,2,2,…;反过来,数列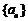 为常数列,由于
为常数列,由于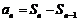 为常数,则数列
为常数,则数列 为等差数列;所以数列
为等差数列;所以数列 为等差数列是数列
为等差数列是数列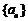 为常数列的必要不充分条件,故选B
为常数列的必要不充分条件,故选B
4. 已知函数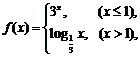 则
则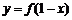 的大致图象是(C)
的大致图象是(C)
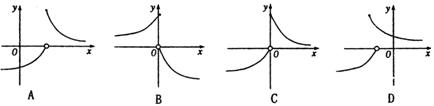
解析:画出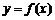 的图象,再作其关于
的图象,再作其关于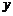 轴对称的图象,得到
轴对称的图象,得到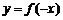 的图象,再将所得图象向右移动1个单位,得到
的图象,再将所得图象向右移动1个单位,得到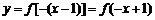 的图象,故选C
的图象,故选C
3. 等比数列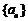 的各项为正,公比
的各项为正,公比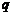 满足
满足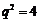 ,则
,则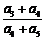 的值为(D)
的值为(D)
A.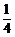 B.2 C.
B.2 C. D.
D.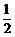
解析:因为此等比数列的各项为正,∴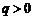 ,又
,又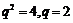 .
.
故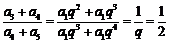 ,故选D.
,故选D.
2. 关于x的不等式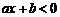 的解集为
的解集为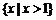 ,则关于x的不等式
,则关于x的不等式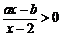 的解集为(C)
的解集为(C)
A.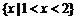 B.
B.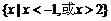
C.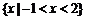 D.
D.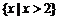
解析:由题意知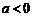 ,
,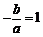 ,代入
,代入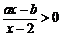 得
得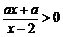 ,即
,即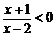 ,
,
∴解集为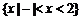
1. 设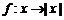 是集合A到集合B的映射,且集合B中的每一个元素都有原象,若
是集合A到集合B的映射,且集合B中的每一个元素都有原象,若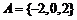 ,则
,则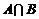 等于(C)
等于(C)
A.{0} B.{2} C.{0,2} D.{-2,0}
解析:B={0,2},∴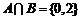
11.(9分) 有机物参加的反应往往比较复杂,常有副反应发生;如下图中乙烯跟溴水反应既可生成A.同时又可生成B和C2H5Br。
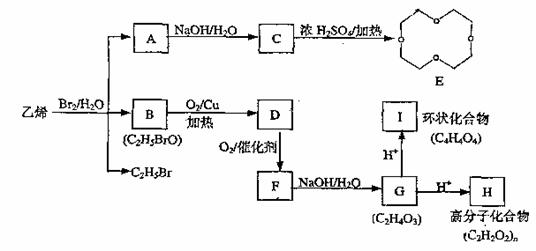
回答下列问题:
(1)环氧乙烷(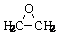 )的结构可简写为
)的结构可简写为 则E的分子式是 。
则E的分子式是 。
(2)A的结构简式是 ;B的结构简式是 。
(3)G→I的反应类型是____________。
(4)写出G转化为H的化学方程式:
(5)化合物A-I中,易发生加成反应的物质是 (填字母)。
11(9分)
(1)、C8H16O4 (1分)(2)BrCH2-CH2Br(1分) ;HO-CH2-CH2-Br (1分)
(3)酯化反应(2分)
(4)、nHOOC-CH2OH→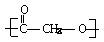 + nH2O (2分)
+ nH2O (2分)
(5)、D(2分)

10.(12分)(l)在整套装置末端接一带弯玻璃导管的乳胶管,并将玻璃导管末端放在盛有水的水槽中;用酒精灯在气体发生装置下面微热(打开弹簧夹),玻璃导管末端有气泡产生;停止加热后,玻璃导管内上升一段水柱,则不漏气( 2 分)。(其它合理答案酌情给分)
(2)浓硫酸( 1 分),吸收产生的氮气中的水,获得干燥的氮气( 1 分)。
(3)为了排尽整套装置中的空气( 2 分)。
 (4)经计算反应后的气体中碳、氧原子的物质的量之比为 2
: 3 ,介于 1 / 2 和 1 之间。( 2 分)(其它合理答案酌情给分); 1 : 1 ( 2 分)。
(4)经计算反应后的气体中碳、氧原子的物质的量之比为 2
: 3 ,介于 1 / 2 和 1 之间。( 2 分)(其它合理答案酌情给分); 1 : 1 ( 2 分)。
(5)在尾气出口处加一点燃的酒精灯或增加一尾气处理装置( 2 分)
10.(12分)某研究性学习小组对过量炭粉与氧化铁反应中气体产物的成分进行了研究。
 [提出假设]该反应中的气体产物可能是CO或者是CO2和CO的混合物。
[提出假设]该反应中的气体产物可能是CO或者是CO2和CO的混合物。
 [查阅资料]氮气不与碳、氧化铁发生反应。实验室可以用氯化铵饱和溶液和亚硝酸钠 ( NaNO2)饱和溶液混合加热反应制得氮气。
[查阅资料]氮气不与碳、氧化铁发生反应。实验室可以用氯化铵饱和溶液和亚硝酸钠 ( NaNO2)饱和溶液混合加热反应制得氮气。
 [设计方案 ] 如图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比。
[设计方案 ] 如图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比。
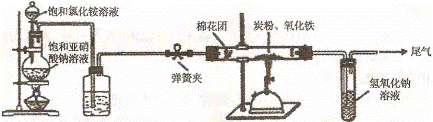
 试回答下列问题:
试回答下列问题:
 (l)按上图连接装置,如何检查该装置的气密性
(l)按上图连接装置,如何检查该装置的气密性
 (2)广口瓶内盛放的试剂为
,其作用为
(2)广口瓶内盛放的试剂为
,其作用为
 (3)实验开始时,应先打开弹簧夹,一段时间后关闭;再点燃酒精喷灯,理由是
(3)实验开始时,应先打开弹簧夹,一段时间后关闭;再点燃酒精喷灯,理由是

 (4)称取3.20g氧化铁、2.00g炭粉混合均匀,放入质量为48.48g的硬质玻璃管中;待反应结束,再通一段时间的氮气。冷却至室温,称得硬质玻璃管和固体总质量为52.24g。经进一步测定得知参加反应的氧元素质量为0.96g 。从而确认该反应的气体产物是C02和CO 的混合物,理由是
。根据数据处理结果判断,反应产生的气体中n(C02):n(CO)=
。
(4)称取3.20g氧化铁、2.00g炭粉混合均匀,放入质量为48.48g的硬质玻璃管中;待反应结束,再通一段时间的氮气。冷却至室温,称得硬质玻璃管和固体总质量为52.24g。经进一步测定得知参加反应的氧元素质量为0.96g 。从而确认该反应的气体产物是C02和CO 的混合物,理由是
。根据数据处理结果判断,反应产生的气体中n(C02):n(CO)=
。
 (5)有同学根据实验得出的结论,认为应对实验装置进一步完善,你认为应作如何改进?
(5)有同学根据实验得出的结论,认为应对实验装置进一步完善,你认为应作如何改进?

9.本题共14分,每空2分
(1)2NaCl+2H2O
 2NaOH+H2↑+Cl2↑(2分) (2)较低温度(2分)
2NaOH+H2↑+Cl2↑(2分) (2)较低温度(2分)
(3)2Fe3++3ClO-+10OH-=2FeO-4+3Cl-+5H2O(2分) (4)AC(2分)
(5)K2FeO4具有强氧化性(2分); 氢氧化铁胶体(2分) (6)KNO3、KCl(2分)
9.(14分)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝、沉淀、灭菌、消毒、脱色、除臭等特点于一体的新型多功能绿色环保水处理剂。其生产工艺如下:

根据上述工艺流程,请回答下列问题:
(1)工业所用Cl2主要来自氯碱工业,氯碱工业产生Cl2的化学方程式为
。
(2)已知Cl2与KOH溶液反应,在较低温度下主要生成KClO,在较高温度下主要生成KClO3,该生产工艺应在 (填“较低温度”或“较高温度”)下进行。
(3)该生产工艺中生成K2FeO4的离子方程式为 。
(4)在“反应液Ⅰ”中加KOH固体的目的是 。
A.与“反应液Ⅰ”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为KClO
(5)K2FeO4具有灭菌、消毒作用的主要原因是 。其灭菌、消毒后的产物具有很好的絮凝作用,根据你所学的知识推测,起絮凝作用的物质是 。
(6)从“反应液Ⅱ”中分离出K2FeO4后,会得到两种重要的化工产品,它们是
(写化学式)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com