
17.纯碱中常含有少量的NaCl等杂质,下图仪器装置可用来测定纯碱中Na2CO3的质量分数。
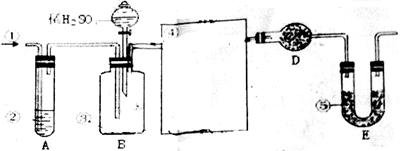
图中:①空气 ②某溶液 ③纯碱 ④某溶液 ⑤碱石灰 (注:碱石灰既能吸收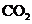 ,又能吸
,又能吸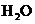 。
。
其实验步骤是:a.按上图所示,组装好实验仪器,并检查其气密性。b.准确称量盛有碱石灰的干燥管D的质量(设为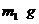 )。 c.准确称量一定量的纯碱(设为
)。 c.准确称量一定量的纯碱(设为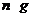 ),并将其放入广口瓶内。d.从分液漏斗中缓慢滴入一定量的稀硫酸,并从“1”处缓慢鼓入空气,直到B容器中不再产生气体为止。e.准确称量干燥管D的总质量(设为
),并将其放入广口瓶内。d.从分液漏斗中缓慢滴入一定量的稀硫酸,并从“1”处缓慢鼓入空气,直到B容器中不再产生气体为止。e.准确称量干燥管D的总质量(设为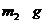 )。
)。
根据上述实验回答下列问题:
(1)该实验进行到操作d时,要缓缓鼓入空气,其作用是________________________。装置A中盛装的液体“2”应选用_____________,装置A的作用是_____________________,如果撤去装置A,直接向B中缓缓鼓入空气,则会导致实验测定结果(填“偏大”“偏小”或“不变”)__________________。
(2)在空气白格内画出装置C及试剂④是_____________;装置C的作用是_____________;如果撤去装置C,则会导致测定结果_______________(填“偏大”“偏小”或“不变”)
(3)根据此实验,计算纯碱中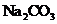 的质量分数的数学式为_________________(4分)(用
的质量分数的数学式为_________________(4分)(用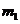 、
、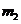 、
、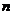 表示)
表示)
(4)装置E的作用是___________________________。
16. 电瓶车所用电池一般为铅蓄电池,这是一种典型的可
电瓶车所用电池一般为铅蓄电池,这是一种典型的可
充电电池,电池总反应式为:
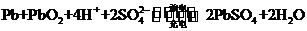 ,
,
则下列说法正确的是
A、放电时:电子流动方向由A到B
B、放电时:正极反应是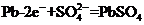
C、充电时:铅蓄电池的负极应与充电器电源的正极
相连
D、充电时,阳极反应是
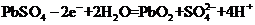
第II卷 非选择题(52分)
15. 取500mL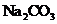 溶液与300mL、1mol/L盐酸反应,在不断搅拌下将碳酸钠同业逐滴滴入盐酸中与将盐酸逐滴滴入碳酸钠溶液中,所产生气体的物质的量之比为3:2。则碳酸钠溶液的物质的量浓度为
溶液与300mL、1mol/L盐酸反应,在不断搅拌下将碳酸钠同业逐滴滴入盐酸中与将盐酸逐滴滴入碳酸钠溶液中,所产生气体的物质的量之比为3:2。则碳酸钠溶液的物质的量浓度为
A、0.2mol/L B、0.3 mol/L C、0.4 mol/L D、0.5 mol/L
14. 下列有关热化学方程式的叙述正确的是
A、已知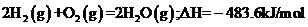 ,则氢气的燃烧热为241.8kJ
,则氢气的燃烧热为241.8kJ
B、已知C石墨,s)=C(金刚石,s);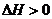 ,则金刚石比石墨稳定
,则金刚石比石墨稳定
C、含20.0g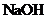 的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式:
的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式:
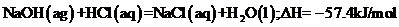
D、已知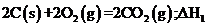
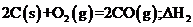 ,则
,则
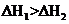
13. 将一定量的有机物充分燃烧后的产物先通入浓硫酸,浓硫酸增重5.4g,然后通入足量澄清石灰水中,完全吸收后,经过滤得到20g沉淀,该有机物可能是
A、乙烯 B、乙醇
C、甲酸甲酯 D、乙酸
12.下列各组离子一定能大量共存的是
A、在含大量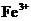 的溶液中:
的溶液中: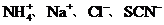
B、在强碱溶液中: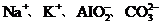
C、在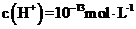 的溶液中
的溶液中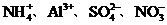
D、在pH=1的溶液中: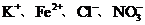
11. 将一定量的钠、铝合金置于水中,合金全部溶解,得到20mL、pH=14的溶液,然后用1mol/L的盐酸滴定至沉淀量最大时,消耗盐酸40mL。原合金中钠的质量为
A、0.92g B、0.69g C、0.46g D、0.23g
10. 甲、乙两个电解池均为Pt为电极,且互相串联。甲池盛有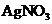 溶液,乙池中盛有一定量的某盐溶液。通电一段时间后,测得甲池电极质量增加2.16g乙池电极上析出0.64g金属,则乙池中的溶质可能是
溶液,乙池中盛有一定量的某盐溶液。通电一段时间后,测得甲池电极质量增加2.16g乙池电极上析出0.64g金属,则乙池中的溶质可能是
A、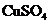 B、
B、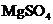 C、
C、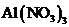 D、
D、
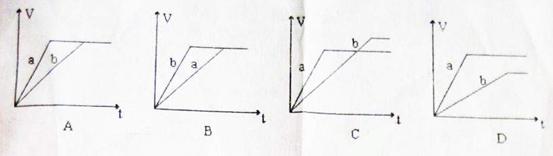
9. 将等质量的两份锌粉a、b,分别加入过量的稀硫酸,同时向a中加少许胆矾晶体,下列各图表示产生氢气的体积V(升)与时间t(分)的关系,其中正确的是
8. A、B两元素均是短周期元素,以下判断中错误的是
A、若A、B同主族,且能形成离子化合物,则该化合物一定能与水反应
B、若A、B同主族。且能形成原子晶体,则其熔点一定大于硅晶体
C、若A、B同周期,且质子数A>B,则Am+的离子半径一定大于Bn+
D、若A在第三周期,且Am+与Bn-具有相同的核外电子排布,则B在第二周期
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com