
3.铁、铝常温下遇浓硝酸,由于浓硝酸具有 ,所以在金属的表面形成一层 ,阻止反应继续进行,这个过程叫 。所以可用铁、铝容器装运浓硝酸(或浓硫酸)。
2.金属活动顺序表中,较不活泼的金属(如铜、银等)都能和硝酸反应,一般浓硝酸被还原为 , 稀硝酸被还原为 ,金属则变为相应的 。这类反应中硝酸只有一部分体现 被还原,另一部分体现 生成硝酸盐。
Ag+2HNO3(浓) 3Ag+4HNO3(稀)
3Ag+4HNO3(稀)
1.金属与硝酸反应,不论金属活泼与否,也不论硝酸的浓度大小,一般 氢气放出。这是因为: 。
3.氨气的实验室制法
(1)原理:固态铵盐与碱加热反应:
(2)发生装置:固+固+加热型,与制备 气体相似;
(3)收集: 。
(4)干燥:在干燥管中盛放 作干燥剂。不能用浓硫酸、P2O5、无水氯化钙作干燥剂,因CaCl2吸收氨气生成CaCl2·8NH3。
(5)验满:a.用湿润的红色石蕊试纸放在瓶口,若变蓝,则满;b.蘸有浓盐酸的玻璃棒接近瓶口,若产生白烟,则满。
[特别提醒]:①制氨气所用铵盐不能用硝铵、碳铵。因加热过程中NH4NO3可能发生爆炸性的分解反应,发生危险;而碳铵受热极易分解产生CO2,使生成的NH3中混有较多的CO2杂质。②消石灰不能用NaOH、KOH代替,原因是:a、NaOH、KOH具有吸湿性、易结块,不利于产生NH3;b、在高温下能腐蚀大试管。③因氨气比空气轻,易与空气发生对流,所以收集时,导气管应插入收集气体的试管底部附近,管口塞一团干燥的棉花团,来防止NH3与空气对流,确保收集到纯净的氨气。④制备NH3也可以通过加热浓氨水的方法,利用NH3·H2O NH3↑+H2O原理制备。也可以利用往浓氨水中加入烧碱制备,原理:烧碱溶于水为放热反应,促进NH3·H2O的分解,增大c(OH-)使上述可逆反应向左移动,而产生NH3。 NH3↑+H2O原理制备。也可以利用往浓氨水中加入烧碱制备,原理:烧碱溶于水为放热反应,促进NH3·H2O的分解,增大c(OH-)使上述可逆反应向左移动,而产生NH3。 |
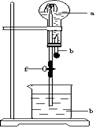 [例2]都能用右图所示装置进行喷泉实验的一组气体是(注:烧杯内为NaOH溶液)
( )
[例2]都能用右图所示装置进行喷泉实验的一组气体是(注:烧杯内为NaOH溶液)
( )
A.HCl和CO2 B.NH3和CH4
C.SO2和CO D.NO2和NO
[解析]在上述气体中,CH4、NO、CO不溶于NaOH溶液,也不与NaOH溶液反应,所以不能做喷泉实验,而HCl、SO2、CO2不仅可溶于NaOH溶液而且还可与NaOH溶液反应,所以能形成喷泉。
[答案]A
[规律总结]喷泉实验成功的关键:①烧瓶、预先吸水的滴管及直玻璃管都要干燥;②气体要充满圆底烧瓶;瓶塞要严密,不漏气,止水夹要夹紧。
注意:满足下列条件时,均能形成美丽的喷泉:①液体为水时,NH3、HBr、HCl、HI、SO2等易溶于水的气体或是NO2、NO2+O2、NO+O2、NO2+NO+O2等易与水反应的气体。
②液体是NaOH、KOH等强碱性溶液时,CO2、SO2、NO2、H2S等酸性气体。
③液体是盐酸或硫酸时,NH3等碱性气体。
考点3 硝酸的强氧化性
硝酸不论浓稀都具有强氧化性,主要有以下几个方面体现:
2.氨的化学性质;
(1)与水反应,溶液呈碱性:NH3+H2O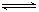 NH3·H2O
NH3·H2O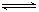 NH4++OH-
NH4++OH-
氨水中所含有微粒: ,氨水中溶质通常看作为NH3,而不是NH3·H2O。
(2)与酸反应
NH3+HNO3 NH4NO3 HCl+NH3
NH4NO3 HCl+NH3 NH4Cl H2SO4+2NH3
NH4Cl H2SO4+2NH3 (NH4)2SO4
氨气与氯化氢相遇便产生 ,可用于NH3与HCl的相互检验。
(NH4)2SO4
氨气与氯化氢相遇便产生 ,可用于NH3与HCl的相互检验。
(3)还原性
NH3分子中氮元素呈-3价,具有还原性,能在一定条件下与O2、Cl2、CuO等反应,被它们氧化:2NH3+3Cl2 2NH3+3CuO
2NH3+3CuO
1.氨的物理性质
氨气为 色、有 气味的气体,比空气轻,易液化, 溶于水,氨水的密度小于水的密度,氨水的浓度 ,密度 。
3.NO、NO2的制法
(1)NO的实验室制法
①原理:
②装置:铁架台、铁夹、铁圈、烧瓶、分液漏斗、胶塞、导管、酒精灯等
③收集:
④检验:无色气体和空气接触立即变红棕色
(2)NO2的实验室制法
①原理:
②装置:锥形瓶(或烧瓶)、分液漏斗、带导管胶塞
③收集:
[特别提醒]:通常“纯净”的NO2或N2O4并不纯,因为在常温、常压下能发生2NO2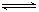 N2O4反应。由于此可逆反应的发生,通常实验测得NO2的相对分子质量大于它的实际值,或在相同条件下,比相同物质的量的气体体积要小。此外涉及NO2气体的颜色深浅、压强、密度等要考虑此反应。因而可逆反应2NO2 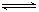 N2O4在解化学题中有很重要的应用。 N2O4在解化学题中有很重要的应用。 |
[例1] 最新研究表明:NO吸收治疗法可快速改善SARS重症患者的缺氧状况,缓解病情。病毒学研究同时证实,NO对SARS病毒有直接抑制作用。下列关于NO的叙述正确的是 ( )
A.NO是一种红棕色的气体 B.常温常压下,NO不能与空气中氧气直接化合
C.含等质量的氧元素的NO和CO的物质的量相等
D.NO易溶于水,不能用排水法收集
[解析]NO是一种无色难溶于水的气体,可以用排水法收集。常温常压下,NO容易与氧气直接化合生成NO2。
[答案]C
考点2 氨的性质
2.NO、NO2都是大气污染物,空气中NO、NO2主要来自石油产品和煤燃烧、汽车尾气以及制硝酸工厂的废气。其中空气中的NO2是造成 的主要因素。
1.氮元素有+1、+2、+3、+4、+5等五种正价态,五种正价对应六种氧化物:N2O、NO、N2O3、NO2、N2O4、N2O5。其中N2O3和N2O5分别是HNO2和HNO3的酸酐。NO是一种 色还原性较强的气体,易被O2氧化生成 ,NO2是一种 色的易溶于水且与水反应的气体,氧化性强,能氧化SO2,能使湿润的KI-淀粉试纸变 。
4.检验步骤
①在待测溶液中加入 ,排除 等离子的干扰。注意一般不用稀HNO3,因为稀HNO3能将 氧化成 而被漏检。
②在排除干扰后的溶液中加入 ,产生的白色沉淀一定是BaSO4,则此溶液中一定含有SO42-。
|
[特别提醒]:检验SO42-的关键是既要注意试剂的选择,又要注意操作顺序的优化,方能排除干扰离子的误导,要全面考虑,综合分析,正确推导。 |
[例4]对某酸性溶液(可能含有Br-、SO42-、H2SO3、NH4+)分别进行如下实验:
①加热时放出的气体可以使品红溶液褪色 ②加碱调至碱性后,加热时放出的气体可以使湿润的红色石蕊试纸变蓝 ③加入氯水时,溶液略显黄色,再加入BaCl2溶液时,产生的白色沉淀不溶于稀硝酸。对于下列物质不能确认其在溶液中是否存在的是 ( )
A.Br- B.SO42- C.H2SO3 D.NH4+
[解析]①加热时放出的气体可以使品红褪色,则溶液中一定含有H2SO3,因H2SO3不稳定,分解产生的SO2可使品红褪色。②加碱后加热,产生使润湿的红色石蕊试纸变蓝的气体,即有NH3产生,说明溶液中一定含有NH4+。③加氯水时溶液显黄色,说明原溶液中含有Br-。再加BaCl2有白色不溶于HNO3的沉淀生成,说明此时溶液中含SO42-,但可能是原溶液含有的,也可能是氯水氧化H2SO3产生的,故不能确定的为SO42-。
[答案]B
[误区警示]SO42-检验的误区:
①只加可溶性钡盐,不酸化。误将CO32-、PO43-、SO32-、Ag+等干扰离子判成SO42-,此时上述离子同样会产生BaCO3、Ba3(PO4)2、BaSO3、AgCl的白色沉淀。
②误将Ag+、Pb2+判成SO42-。如向待测液中滴加BaCl2溶液,再加盐酸有白色沉淀便断定含SO42-。其错误是未注意溶液中不含SO42-而含Ag+或Pb2+也会有同样现象。
因为Ag++Cl- AgCl↓(白色)
Pb2++2Cl-
AgCl↓(白色)
Pb2++2Cl- PbCl2↓(白色)
PbCl2↓(白色)
③误将SO32-判成SO42-。如向待测液中滴加用盐酸酸化的Ba(NO3)2溶液生成白色沉淀,便误以为有SO42-。该错误是未注意NO3-具有强氧化性,在酸性环境中发生反应:Ba2++
SO32- BaSO3↓(白色),3BaSO3+2H++2NO3-
BaSO3↓(白色),3BaSO3+2H++2NO3- 3BaSO4↓(白色)+2NO↑+H2O
3BaSO4↓(白色)+2NO↑+H2O
再如向待测液中滴加用硝酸酸化的BaCl2溶液产生白色沉淀便错误认定一定含SO42-,也同样是落入干扰离子转化为SO42-从而生成BaSO4的陷阱中。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com