
1、乙酸的组成与结构
乙酸的分子式:C2H4O2; 结构简式:CH3COOH;官能团是-COOH(羧基)。从结构上看,乙酸是羧基和甲基相联接而成的。由于乙酸分子中羧基和羟基的相互影响,使羟基上的氢更活泼,在水溶液中能部分电离出氢离子,乙酸是一种典型的有机弱酸;羟基的存在也使羧基的加成反应相当困难,很难与氢气等发生加成反应。
3、乙醇的主要用途
乙醇有相当广泛的用途,是一种重要的有机原料,可用它制取乙酸、乙醚等。乙醇还可用作燃料它还是一种有机溶剂,用于溶解树脂、制造染料。在医疗上常用75%(体积分数)的酒精作消毒剂。
3、乙醇的化学性质
(1)乙醇与金属钠反应的化学方程式:2CH3CH2OH+2Na→2CH3CH2ONa +H2↑,此反应属于 ,该反应比钠与水反应要缓和得多,说明乙醇羟基上的氢原子活泼性 水分子中的氢原子,乙醇比水 电离,乙醇是非电解质。
(2)氧化反应
①乙醇燃烧的化学方程式:CH3CH2OH+3O2  2CO2+3H2O,乙醇燃烧时放出大量的热,常被用作酒精灯和内燃机的 。
2CO2+3H2O,乙醇燃烧时放出大量的热,常被用作酒精灯和内燃机的 。
特别提醒:燃烧消耗氧气的量与乙烯相同,燃烧生成二氧化碳和水的量与乙烷相同。
②乙醇的的化学方程式: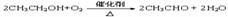 ,如果将光亮的铜丝放在酒精灯火焰上灼烧,然后再趁热插入乙醇中,将发现铜丝先由 色变为
色,插入乙醇中后,又变为 色,可闻到
。
,如果将光亮的铜丝放在酒精灯火焰上灼烧,然后再趁热插入乙醇中,将发现铜丝先由 色变为
色,插入乙醇中后,又变为 色,可闻到
。
③乙醇能被酸性高锰酸钾溶液或酸性(或酸性重铬酸钾)氧化生成乙酸,使溶液 。
(3)乙醇生成乙烯的化学方程式: ,醇发生消去反应时,是羟基与相连接碳原子相邻的碳原子上氢原子一起结合成水脱去,如果羟基相连接碳原子相邻的碳原子上无氢原子,则不能发生消去反应。
,醇发生消去反应时,是羟基与相连接碳原子相邻的碳原子上氢原子一起结合成水脱去,如果羟基相连接碳原子相邻的碳原子上无氢原子,则不能发生消去反应。
2、乙醇的物理性质
乙醇是无色透明而有特殊香味的液体,密度比水小,沸点为78.5 ℃,易挥发,能和水以以任意比混溶,乙醇本身是良好的 ,能溶解多种有机物和无机物。
特别提醒:乙醇由于和水互溶,不能萃取溴水和碘水。
1、乙醇的组成与结构
乙醇的分子式:C2H6O;结构式: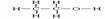 ;结构简式:CH3CH2OH或C2H5OH。官能团是 。
;结构简式:CH3CH2OH或C2H5OH。官能团是 。
4.用途:苯是一种很重要的有机化工原料,它广泛用来生产合成纤维、合成橡胶、塑料、农药、染料、香料等,苯也常用作有机溶剂。
3.化学性质:
⑴氧化反应
①可燃性
化学方程式: ;现象:在空气中燃烧,发出明亮的光,产生大量的黑烟。
②苯 使高锰酸钾(KMnO4)褪色。
⑵取代反应
①卤代反应
苯与液溴在铁的催化作用下发生反应的化学方程式:
②硝化反应
苯与硝酸发生取代反应的化学方程式:
⑶加成反应
苯与氢气发生加成反应的化学方程式:
2.物理性质:
苯在通常情况下,是无色、带有特殊芳香气味的 体,有毒, 于水,与有机溶剂互溶,熔、沸点比较 。苯是常用的有机溶剂。
1.苯的结构
(1)苯的发现:苯是1825年由英国科学家法拉第首先发现的。
(2)苯的分子式 ,结构式 ,结构简式 或 ,分子中所有的原子都在 上,苯分子中6个碳碳化学键 ,苯分子中不含有简单的 ,不是 结构,是一种 的独特的键。
4.化学性质:
⑴氧化反应
①与酸性高锰酸钾反应(特征反应)
现象: 。结论:乙烯的C=C易被强氧化剂如KMnO4氧化而断裂,产物可能是CO2, 利用此性质可以用来鉴别甲烷和乙烯。
②可燃性:
化学方程式: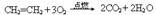 ;现象:
。
;现象:
。
⑵加成反应:
乙烯与溴的四氯化碳溶液或溴水反应的化学方程式:CH2=CH2+Br2→ (1,2-二溴乙烷)
①现象: 。结论:利用此性质可以用来鉴别甲烷和乙烯。
②加成反应:有机物分子中双键(或三键)两端的碳原子与其他原子或原子团直接结合生成新的化合物的反应叫做加成反应。乙烯还能与Cl2、H2、HX、H2O加成。
乙烯与氢气反应的化学方程式: ,乙烯与氯化氢反应的化学方程式: ,乙烯与水反应的化学方程式:
⑶加聚反应
乙烯加成得到聚乙烯的化学方程式:
①加聚反应:相对分子质量小的化合物分子互相结合成相对分子质量很大的高分子化合物的反应叫聚合反应。在聚合反应中,由不饱和(即含碳碳双键或三键)的相对分子质量小的化合物分子通过加成聚合的形式结合成相对分子质量很大的高分子化合物的反应。
②高分子化合物: ,简称高分子或高聚物。聚乙烯,塑料,分子量达几万到几十万,性质坚韧,化学性质稳定,难降解。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com