
2.磷元素单质及化合物性质记忆不清,解有关习题时容易出错。
1.对氮族元素原子结构特点理解不清,对同主族元素性质相似性、递变性理解不到位,不能灵活运用同主族元素性质相似性、递变性规律解题。
10.2.1克Cu与100mL的1.0mol/L稀硝酸完全反应。计算生成NO多少升(标准状况)。反应消耗硝酸的物质的量是多少?(写出计算过程)
(此题考查过量计算的计算技能)
第26课时 氮族元素 氮和磷(B卷)
易错现象
8. NO分子因污染空气而臭名昭著。近年来,发现少量的NO在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,而成为当前生命科学的研究热点,NO亦被称为“明星分子”。请回答下列问题。
(1)NO对环境的危害在于 (填以下项目的编号)
A.破坏臭氧层 B.高温下能使一些金属被氧化
C.造成酸雨 D.与人体血红蛋白结合
(2)在含Cu+ 离子的酶活化中心中,亚硝酸根离子
(NO2-)可转化为NO,写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式: 。
(3)在常温下,把NO气体压缩到100个大气压,在一个体积固定的容器里加热到50℃,发现气体的压力迅速下降,压力降至略小于原压力2/3就不再改变,已知其中一种产物为N2O,写出上述变化的化学方程式: 。
(4)解释变化(3)中为什么最后的气体总压力小于原压力的2/3 。
(此题属于信息题,一般认为NO是有害气体,此题告诉人们它对人也有有用的一面。考查根据客观事实写方程式的能力。)
9(96年上海高考题).实验室常用饱和NaNO2和NH4Cl溶液反应制取纯净的氮气。反应式为:
NaNO2 + NH4Cl == NaCl + N2↑+2H2O↑+ Q实验如下图
试回答:
(1) 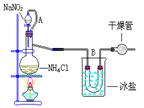 装置中A部分的分液漏
装置中A部分的分液漏
斗与蒸馏烧瓶之间连接的导
管所起的
作用是( )。
a. 防止NaNO2饱和溶液蒸
发
b.保证实验装置不漏气
c.NaNO2饱和溶液容易滴下
(2) B部分的作用是( )
a. 冷凝 b. 冷却氮气 c. 缓冲氮气流
(3) 加热前必须进行一个操作步聚是: _ ;加热片刻后,即应移去酒精灯以防反应物冲出,其原因是: _ 。
(4)收集N2前必须进行的步聚是: ;收集N2最适宜的方法是( )。
a. 用排气法收集在集气瓶中
b. 用排水法收集在集气瓶中
c.直接收集在球胆或塑料袋中
7.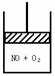 右图为装有活塞的密闭容器,内盛22.4ml的一氧化氮,若通入11.2L氧气(气体体积均在标准状况下测定)保持温度和压强不变
,则容器内的密度
右图为装有活塞的密闭容器,内盛22.4ml的一氧化氮,若通入11.2L氧气(气体体积均在标准状况下测定)保持温度和压强不变
,则容器内的密度
A. 等于1.369克/升
B.等于2.054克/升
C.在1.369克/升和2.054克/升之间
D 大于2.054克/升
(此题考查密度的计算技能及极值法的应用。)
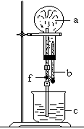
6.在下图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是 ( )
 (此题考查NH3、NO2、CO2等形成喷泉的实验,要求掌握喷泉实验形成的原理,从物理有关知识理解。)
(此题考查NH3、NO2、CO2等形成喷泉的实验,要求掌握喷泉实验形成的原理,从物理有关知识理解。)
5.在NO2与水的反应中,水 [ ]
A.是还原剂 B.是氧化剂
C.既是氧化剂又是还原剂
D.既不是氧化剂又不是还原剂
 (此题考查NO2与水的反应,该反应中NO2一部分做氧化剂,一部分做还原剂,属于歧化反应。)
(此题考查NO2与水的反应,该反应中NO2一部分做氧化剂,一部分做还原剂,属于歧化反应。)
4.常温下,在密闭容器中将物质的量相同的下列各组气体混合,完全反应后容器中压强没有发生变化的是
A、H2S和SO2 B、NO和O2
C、HI和Cl2 D、H2S和Cl2
(此题是元素化合物知识的综合题,考查硫、氮、氯等性质,阿伏加得罗定律推论的运用)
3.某金属的硝酸盐加热分解生成的NO2和O2的物质的量之比8:1。在加热过程中,该金属元素的化合价
A、降低 B、升高
C、不变 D、无法确定
(此题看似超纲,需要硝酸盐的分解知识,但实际是考查运用氧化还原反应知识解决问题的能力,氧化还原反应中化合价生降总数必相等。)
2、工业废气中氮氧化物是主要的大气污染源之一。
已知2NO2+2NaOH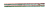 NaNO3+NaNO2+H2O,NO2+NO+2NaOH
NaNO3+NaNO2+H2O,NO2+NO+2NaOH 2NaNO2+H2O。现有a mol NO2和b mol NO的混合气,若用足量的NaOH溶液将其完全吸收,则混合气中两种气体的物质的量必须满足的关系是
2NaNO2+H2O。现有a mol NO2和b mol NO的混合气,若用足量的NaOH溶液将其完全吸收,则混合气中两种气体的物质的量必须满足的关系是
A、a=b/3 B、2a=b
C、a≥b D、a<b
(此题是信息题,考查接受信息的能力,解决问题的能力)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com