
2H2Θ®gΘ© + O2 = 2H2OΘ®gΘ© ΓςH= ®D 483.6kJ/mol
CΘ®sΘ© + O2 = CO2 ΓςH= ®D 393.5kJ/mol
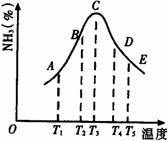 Θ®1Θ©AΘ§BΘ§CΘ§DΘ§EΈεΒψ÷–Θ§…–Έ¥¥οΒΫΜ·―ßΤΫΚβΉ¥Χ§
Θ®1Θ©AΘ§BΘ§CΘ§DΘ§EΈεΒψ÷–Θ§…–Έ¥¥οΒΫΜ·―ßΤΫΚβΉ¥Χ§
ΒΡΒψ «_______ΓΘ
Θ®2Θ©¥ΥΩ…ΡφΖ¥”ΠΒΡ’ΐΖ¥”Π «______Ζ¥”ΠΓΘΘ®Ζ≈»»ΓΔΈϋ»»Θ©
Θ®3Θ©ACΕΈΒΡ«ζœΏ «‘ωΚ· ΐΘ§CEΕΈ«ζœΏ «ΦθΚ· ΐΘ§ ‘¥”
Ζ¥”ΠΥΌ¬ ΚΆΤΫΚβΫ«Ε»ΥΒΟςάμ”…ΓΘ________________
____________________
IIΘ°Θ®1Θ© ΙCl2ΚΆH2OΘ®gΘ©Ά®ΙΐΉΤ»»ΒΡΧΩ≤ψΘ§…ζ≥…HClΚΆCO2 «Ζ≈»»Ζ¥”ΠΘ§Β±Ζ¥”Π÷–ΉΣ“Τ1molΒγΉ” ± ΆΖ≈145kJΒΡ»»ΝΩΘ§–¥≥ω’βΗω»»Μ·―ßΖΫ≥Χ ΫΘΚ ΓΘ
Θ®2Θ©“―÷ΣN2 Θ®gΘ©+ O2 Θ®gΘ© ΘΫ2NO Θ®gΘ© ΓςH= + 180kJ/mol Θ§Τδ÷–NΓ‘NΦϋΒΡΦϋΡήΈΣ946kJ/molΓΔ―θΖ÷Ή”÷–―θ―θΦϋΒΡΦϋΡήΈΣ498kJ/mol Θ§‘ρ“Μ―θΜ·ΒΣΖ÷Ή”÷–ΒΣ―θΦϋΒΡΦϋΡή_____kJ/molΓΘ
Θ®3Θ©“―÷Σœ¬Ν–»»Μ·―ßΖΫ≥Χ ΫΘΚ
29Θ°Θ®10Ζ÷Θ©Δώ.‘Ύ»ίΜΐ≤ΜΆ§ΒΡΟή±’»ίΤςΡΎΘ§Ζ÷±π≥δ»κΆ§ΝΩΒΡN2ΚΆH2Θ§‘Ύ≤ΜΆ§Έ¬Ε»œ¬Θ§»ΈΤδΖΔ…ζΖ¥”ΠN2+3H2 2NH3Θ§≤ΔΖ÷±π‘ΎtΟκ ±≤βΕ®Τδ÷–NH3ΒΡΧεΜΐΖ÷ ΐΘ§ΜφΆΦ»γœ¬ΘΚ
2NH3Θ§≤ΔΖ÷±π‘ΎtΟκ ±≤βΕ®Τδ÷–NH3ΒΡΧεΜΐΖ÷ ΐΘ§ΜφΆΦ»γœ¬ΘΚ
28Θ°Θ®16Ζ÷Θ©Χζ «»’≥Θ…ζΜν÷–Ήν≥ΘΦϊΒΡΫπ τΘ§Ρ≥ΑύΆ§―ß‘Ύ―ßœΑΧζΒΡ÷Σ Ε ±Θ§”–œ¬Ν–Έ ΧβΘΚ
Έ Χβ1ΘΚΧζΈΣΚΈ≥ΤΈΣΚΎ…ΪΫπ τΘΩ
Έ Χβ2ΘΚCuO‘ΎΗΏΈ¬œ¬Ω…Ζ÷ΫβΈΣCu2OΚΆO2Θ§Fe2O3‘ΎΗΏΈ¬œ¬Ω…Ζ÷ΫβΈΣFeOΚΆO2¬πΘΩ
Θ®1Θ©Ε‘”ΎΈ Χβ1Θ§Ά§―ßΟ«…œΆχ≤ι―ΑΘ§”–ΝΫ÷÷Ϋβ ΆΘΚ
AΓΔ“ρΈΣ‘ΎΧζ±μΟφ…œ”–ΚΎ…ΪΒΡΧζΒΡ―θΜ·ΈοΘ§Υυ“‘Ϋ–ΚΎ…ΪΫπ τΓΘ
BΓΔ“ρΈΣΧζΒΡΖέΡ©ΈΣΚΎ…ΪΘ§ΧζΒΡ―θΜ·Έο“≤ΨυΈΣΚΎ…ΪΘ§Υυ“‘Ϋ–ΚΎ…ΪΫπ τΓΘ
ΔΌΡψ»œΈΣ’ΐ»ΖΒΡΥΒΖ® « ΓΘ
ΔΎ»τ”–“ΜΚΎ…ΪΖέΡ©Θ§Ρψ»γΚΈΦχ±π «ΧζΖέΘ§ΜΙ «Fe3O4ΖέΡ©ΓΘ
Δέ»τ”–“ΜΚΎ…ΪΖέΡ©Θ§ΈΣΧζΚΆΥΡ―θΜ·»ΐΧζΒΡΜλΚœΈοΘ§Ρψ»γΚΈ÷ΛΟςΤδ÷–”–Fe3O4Θ®÷Μ“Σ«σΦρ ω Β―ιΖΫΖ®Θ©ΓΘ
Θ®2Θ©Ε‘”ΎΈ Χβ2Θ§Ά§―ßΟ«ΉΦ±Η Β―ιΧΫΨΩΘ§ΥϊΟ«…ηœκΝΥΝΫ÷÷ΖΫΖ®ΘΚ
AΘΚΫΪ»ΐ―θΜ·ΕΰΧζΗΏΈ¬ΉΤ…’Θ§Ω¥ΉΤ…’«ΑΚσ―’…Ϊ «Ζώ±δΜ·ΓΘ
BΘΚΫΪ»ΐ―θΜ·ΕΰΧζΗΏΈ¬ΉΤ…’Θ§Ω¥ΉΤ…’«ΑΚσ÷ ΝΩ «Ζώ±δΜ·ΓΘ
ΔΌ Β―ι÷–”ΠΫΪFe2O3Ζ≈‘Ύ Θ®Χν“«ΤςΟϊ≥ΤΘ©÷–ΉΤ…’ΓΘ
ΔΎΖΫΖ®A÷–Θ§»γΙϊΗΏΈ¬ΉΤ…’Κσ―’…Ϊ”… ±δΈΣ Θ§ΥΒΟςFe2O3»Ζ ΒΖΔ…ζΝΥ±δΜ·ΓΘΡήΥΒΟς…ζ≥…ΒΡ“ΜΕ®ΈΣFeO¬πΘΩ Θ§άμ”… « ΓΘ
ΔέΖΫΖ®B÷–Θ§»γΙϊΖΔ…ζΝΥ‘ΛΤΎΒΡΖ¥”ΠΘ§ΙΧΧεΗΏΈ¬ΉΤ…’«ΑΚσ÷ ΝΩ±»”ΠΈΣ Θ§ΒΪ «Θ§ Β―ιΫαΙϊΙΧΧεΉΤ…’«ΑΚσ÷ ΝΩ±»ΈΣ30 ΘΚ29Θ§‘ρΗΏΈ¬ΉΤ…’Κσ…ζ≥…Έο « ΓΘ
Δή±»ΫœΝΫ÷÷ΖΫΖ®Θ§Ρψ»œΈΣΫœΚΟΒΡΖΫΖ® « ΓΘ
|