
(四)重要含氯化合物的转化关系
1、主要化合价:
2、转化关系:
[教学反思]
(三)、氯气的制取、用途:
(1)实验室制取Cl2的反应原理: (离子方程式)
(2)足量MnO2和含4mol HCl的浓盐酸加热制得Cl2物质的量为 ;
(3)若实验室没有浓盐酸,可用什么代替?
(4)完成以下生成Cl2的反应:
KMnO4+HCl(浓)-- KClO3+HCl(浓) --
K2Cr2O7+HCl(浓)-- PbO2+HCl(浓)--
Ca(ClO)2+HCl(浓)-- NaCl+H2O--
思考与交流:有人提出以下方法均能用于检验氯气是否集满:①观察法(黄绿色)②湿淀粉--KI试纸(或品红试纸)③湿石蕊试纸 ④浓NH3水,试评价是否可行?
(5)氯气的工业制法:
 (6)用途:
(6)用途:
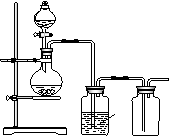
例4:可用如图装置制取(必要时可加热)、
净化、收集的气体是
(A)铜和稀硝酸制一氧化氮 (B)氯化钠与浓硫酸制氯化氢
(C)锌和稀硫酸制氢气 (D)硫化亚铁与稀硫酸制硫化氢
(二)、氯气的分子结构和化学性质
1、 结构
2、 化学性质:
(1)跟金属反应(与变价金属反应,均使金属达到高价态):
(2)跟非金属反应(跟H2、P等反应):
(3)与水反应:
①新制的氯水与久置的氯水成分有何不同?
②新制的氯水的性质有哪些?
思考与交流:将新制的氯水滴入含酚酞的NaOH溶液中,当滴到一定量时红色突然褪去。试回答下列问题:(1)实验室怎样保存氯水?
(2)酚酞褪色的原因可能有两种:①是氯水与NaOH发生反应,且氯气溶于水显酸性,使溶液碱性降低;②是Cl2与水反应产生的HClO将酚酞漂白。怎样用一个简单实验证明上述原因究竟哪一个合理?
(3)氯水中存在哪些平衡体系?HClO有哪些性质?
(4)跟碱反应:
Cl2+2NaOH=
2Cl2+2Ca(OH)2=
工业上用氯气和石灰乳制得漂白粉。漂白粉的有效成分是 漂白粉的漂白原理是: .
例2:氯气通入石灰乳得漂白粉,其主要成分是Ca(OH)2·3CaCl(ClO)·nH2O,现有一种漂白粉的“有效氯”(HCl和漂白粉作用生成Cl2的质量和漂白粉质量之比)为35%,若该漂白粉的组成和上述化学式相符,则式中n的值应是
A.6.5 B.8 C.8.5 D.10
(5)与具有还原性的化合物:FeCl2、H2S、SO2、Na2SO3等反应:
反应方程式:
(6)与某些有机物(如烃反应):
思考与交流:常见的漂白剂有哪些?
例3:氯气是一种重要的工业原料。工业上利用反应3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气。下列说法错误的是
(A)若管道漏气遇氨就会产生白烟 (B)该反应利用了Cl2的强氧化性
(C)该反应属于复分解反应 (D)生成1 mol N2有6 mol电子转移
(一)、氯气的物理性质
通常情况下,氯气是 色、有 气味、比空气 的有毒气体,易液化,能溶于水。
例1:氯气是有毒的,曾被法西斯制成毒气弹用于侵略战争。当这种毒气弹顺风爆炸时,通常可用的防御方法是 ( )
A.人、畜应躲到低洼的地方 B.人、畜应至较高的地方去
C.人、畜应多喝豆浆和牛奶 D.可用肥皂水浸湿软布蒙面
2、(09年山东理综)下列关于氯的说法正确的是
A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂
B.若35
17Cl、37 17若Cl为不同的核素,有不同的化学性质
C.实验室制备Cl2,可用排饱和食盐水集气法收集
D.1.12LCl2含有1.7NA个质子(NA 表示阿伏伽德罗常数)
感悟高考:
1、(07年山东)氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是
A.在通入少量氯气,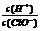 减小
减小
B.通入少量SO2,溶液的漂白性增强
C.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-)
D.加入少量水,水的电离平衡向正反应方向移动
3、了解实验室制取氯气的装置及操作。
2、了解常见非金属氯及其化合物的主要性质和重要应用。
1、了解非金属原子核外电子排布的周期性与元素性质递变关系,掌握典型非金属氯元素在元素周期表中的位置及性质的关系;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com