
24.(4分)氢能源是21世纪极具开发前景的新能源之一,它既是绿色能源,又可循环使用。请在下图的两个空框中填上循环过程中反应物和生成物的分子式,以完成理想的氢能源循环体系图(循环中接受太阳能的物质在自然界中广泛存在)。从能量转换的角度看,过程II主要是_______能转化为________能。

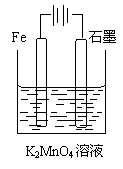
23.(6分)工业上采用以铁、石墨为电极,电解K2MnO4溶液制取KMnO4,装置如图所示
(1)Fe作_______极,其附近溶液的pH________(填“变大”“变小”或“不变”)。
(2)石墨电极上的反应式为________________________________。
(3)总方程式为__________________________________________。
22. (2分)已知:2H2(g) + O2(g)
== 2H2O(g);△H= –483.6 kJ·
(2分)已知:2H2(g) + O2(g)
== 2H2O(g);△H= –483.6 kJ· , H2(g) + 1/2O2(g) == H2O(l)的△H=–285.8 kJ·
, H2(g) + 1/2O2(g) == H2O(l)的△H=–285.8 kJ· ,由此可知,在等温下蒸发45g液态水需吸收________KJ的热量
,由此可知,在等温下蒸发45g液态水需吸收________KJ的热量
21.(4分)由氢气和氧气反应生成1mol水蒸气放热241.8KJ,写出该反应的热化学方程式_______________________.
若1g水蒸气转化成液态水时放热2.444KJ,则反应H2(g) + 1/2O2(g) == H2O(l)的△H=______________
kJ· 。
。
20.在500mL1mol·L-1的CuSO4溶液中,阳极为100gCu片,阴极为100gZn片,通电一段时间后,立即取出电极,测得锌片质量增加到106.4g,此时剩余溶液中CuSO4的物质的量浓度为( )
A.0.25 mol·L-1 B.0.8 mol·L-1 C.1.0 mol·L-1 D.1.2 mol·L-1
第II卷(共50分)
19.CuI是一种白色不溶于水的固体,以石墨(阴)和铜(阳)为电极组成电解槽,以含酚酞和淀粉的KI水溶液为电解液进行电解。电解开始不久,阴极区溶液显红色,而阳极区仍为无色。过了相当长的时间后,阳极区才呈蓝色,则电解开始时的电极反应为( )
A. 阳极反应:Cu – 2e– == Cu2+
阴极反应:Cu2+ +2e– == Cu
B. 阳极反应:2Cu – 2e–+ 2I–== 2CuI
阴极反应:2H+ +2e– == H2↑
C. 阳极反应: 2I–– 2e– == I2
阴极反应:2H+ +2e– == H2↑
D. 阳极反应:Cu – 2e– == Cu2+
阴极反应:2H+ +2e– == H2↑
18.氢-镍电池是近年来开发出来的可充电电池,它可以取代会产生镉污染的镍镉电池,
|
|
 Ni(OH)2。根据此反应判断,下列叙述中正确的是( )
Ni(OH)2。根据此反应判断,下列叙述中正确的是( )
A. 电池放电时,镍元素被氧化
B. 电池充电时,氢元素被还原
C. 电池放电时,电池负极周围溶液的pH不断减小
D. 电池充电时,H2在阴极生成
17.有X、Y、Z、M四种金属,已知:X可以从Y 的盐溶液中置换出Y;X和Z作原电池电极时,Z为正极;Y和Z的离子共存于电解液中,Y离子先放电;M的离子的氧化性强于Y的离子,则这四种金属的活动性由强到弱的顺序是( )
A.X 〉Y〉Z〉M B. X 〉Z〉M〉Y
C. M 〉Z〉X〉Y D. X 〉Z〉Y〉M
16.下列关于实验现象的描述不正确的是( )
A. 把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B. 用锌片做阳极,铁片作阴极,电解氯化锌溶液,铁片表面出现一层锌
C. 把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D. 把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
15.下列说法中正确的是( )
A. 原电池的正极和电解池的阳极都是发生氧化反应
B. 用铂做电极电解NaOH溶液时,溶质的质量不变,但浓度却随着电解的进行而增大
C. 电解食盐水时,由于OH-离子向阳极移动,所以加酚酞时阳极附近可变红色
D. 电解食盐水时,阴极区溶液里OH-离子的浓度相对增大,使酚酞试液变红
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com