
2. 溶液的酸碱性
溶液的酸碱性
溶液的酸碱性 常温(25℃)
中性溶液:C(H+) C(OH-) C(H+) 1×10- 7mol/L
酸性溶液:C(H+) C(OH-) C(H+) 1×10-7mol/L
碱性溶液:C(H+) C(OH-) C(H+) 1×10- 7mol/L
1.影响水的电离平衡的因素
(1)温度:温度升高,水的电离度 ,水的电离平衡向 方向移动,C(H+)和C(OH-) ,KW 。
(2)溶液的酸、碱度:改变溶液的酸、碱度均可使水的电离平衡发生移动。
讨论:改变下列条件水的电离平衡是否移动?向哪个方向移动?水的离子积常数是否改变?是增大还是减小?
①升高温度 ②加入NaCl ③加入NaOH ④加入HCl
练习:①在0.01mol/LHCl溶液中, C(OH-)= , C(H+)= ,
由水电离出的H+浓度= ,由水电离出的OH-浓度= 。,
②在0.01mol/LNaOH溶液中,C(OH-)= ,C(H+)= ,
由水电离出的H+浓度= ,由水电离出的OH-浓度= 。
 ③在0.01mol/LNaCl溶液中,
C(OH-)=
,C(H+)=
,
③在0.01mol/LNaCl溶液中,
C(OH-)=
,C(H+)=
,
由水电离出的H+浓度= ,由水电离出的OH-浓度= 。
小结:(1)升高温度,促进水的电离KW增大
(2)酸、碱抑制水的电离
2.水的离子积
水的离子积:KW= 。
注:(1)一定温度时,KW是个常数,KW只与 有关, 越高KW越 。
25℃时,KW= ,100℃时,KW=10-12。
(2)KW不仅适用于纯水,也适用于酸、碱、盐的稀溶液。 任何水溶液中,由水所电离而生成的C(H+) C(OH-)。
[思考]水是不是电解质?它能电离吗?写出水的电离方程式.
1.水的电离:水是 电解质,发生 电离,电离过程
水的电离平衡常数的表达式为
思考:实验测得,在室温下1L H2O(即 mol)中只有1×10-7 mol H2O电离,则室温下C(H+)和C(OH-)分别为多少? 纯水中水的电离度α(H2O)= 。
12. 如图,已知Rt△ABC中,∠B=90°,tanC=0.5,AB=1,在△ABC内有一系列正方形,求所有这些正方形面积之和.0.8
如图,已知Rt△ABC中,∠B=90°,tanC=0.5,AB=1,在△ABC内有一系列正方形,求所有这些正方形面积之和.0.8
11.已知数列{an}中,an= Sn为其前n项的和,求
Sn为其前n项的和,求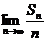 的值.1
的值.1
10.一个热气球在第一分钟时间里上升了25米高度,在以后的每一分钟里,它上升的高度都是它在前一分钟里上升高度的80%,这个热气球最多能上升 米.
9.已知 则m=
n=
.
则m=
n=
.
8.用数学归纳法证明n∈N*时,34n+2+52n+1被14整除的过程中,当n=k+1时,对34(k+1)+2+52(k+1)+1可变形为 .
7.已知一个数列的通项公式为f(n),n∈N*,若7f(n)=f(n-1)(n≥2)且f(1)=3,则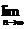 [f(1)+f(2)+…+f(n)]等于( )
[f(1)+f(2)+…+f(n)]等于( )
A. B.
B. C. -7
D. -
C. -7
D. -
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com