
3.热化学方程式书写正误判断方法是:
(1)检查是否标明聚集状态;
(2)检查ΔH的 是否与吸热、放热一致;
(3)检查ΔH的数值是否与反应物或生成物的 相对应(成比例)。
本考点考查较多的是热化学方程式的书写与正误判断,以及由热化学方程式判断物质的稳定性或比较反应热的大小。
[例2] 已知在25℃,101kPa下,1g辛烷C8H8燃烧生成二氧化碳和液态水时放出48.40kJ热量.表示上述反应的热化学方程式正确的是( )
A. ;△H=-48.40kJ/mol
;△H=-48.40kJ/mol
B.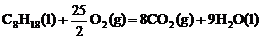 ;△H=-5518kJ/mol
;△H=-5518kJ/mol
C.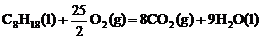 ;△H=+5518kJ/mol
;△H=+5518kJ/mol
D.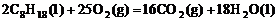 ;△H=+11036kJ/mol
;△H=+11036kJ/mol
[解析] 1 molC8H18 燃烧放出热量48.40kJ/g×114g=5518kJ。2molC8H18放热为11036mol,但是一定要注意符号是“+”还是“-”.
[答案]B
[规律总结]:放热为“+”吸热为“-”,但是焓变△H表达是“+”表示吸热,“-”表示放热.
考点3使用化石燃料的利弊及新能源的开发
(1)重要的化石燃料: 。
(2)煤作燃料的利弊问题。
(3)燃料充分燃烧的条件:①要有足够的 。②跟空气有足够大的 。
(4)新能源的开发:①调整和优化能源结构,降低 在能源结构中的比率。
②最有希望的新能源是核能、太阳能、燃料电池、风能和氢能、潮汐能、地热能等。这些新能源的特点是资源丰富,且有些可以再生,为再生性能源,对环境没有污染或污染少。
[例3] (2007年高考理综上海卷)氢能是一种既高效又干净的新能源,发展前景良好,用氢作能源的燃料电池汽车倍受青睐。我国拥有完全自主知识产权的氢燃料电池轿车“超越三号”,已达到世界先进水平,并加快向产业化的目标迈进。氢能具有的优点包括( )
①原料来源广 ②易燃烧、热值高 ③储存方便 ④制备工艺廉价易行
A.①② B.①③ C.③④ D.②④
[解析]水是广泛的氢来源,但是氢气储存不方便,制备时候要消耗大量能源
[答案] :A
[规律总结]水是多的,但是用水得到氢气的制备工艺并不是廉价易行。能源问题是高考考查的一个热点,开发利用新能源、清洁能源是绝大多数同学都熟知的内容,进一步考查这方面的知识是高考的一个明显趋势
考点4盖斯定律及其应用
2.书写热化学方程式的注意事项:
(1)需注明反应的 ;因反应的温度和压强不同时,其△H不同。
(2)要注明反应物和生成物 。
(3)热化学方程式各物质前的化学计量数不表示分子个数,它可以是整数也可以是分数。对于相同物质的反应,当化学计量数不同时,其△H也不同。
1.定义:表示 的化学方程式,叫做热化学方程式。
5.某化学课外兴趣小组在做铜与浓硝酸、稀硝酸反应实验时发现:“相同质量的铜分别与等体积且足量的浓硝酸、稀硝酸充分反应后,前者溶液颜色是绿色的,后者溶液的颜色是蓝色的。”
(1)一种观点认为:这可能是Cu2+浓度差异的结果,你同意这种看法吗?__________(填“同意”或“不同意”),原因是____________________________________________。
(2)另一种观点认为:溶液呈绿色是铜与浓硝酸反应时产生的NO2溶于过量浓硝酸显黄色,加上和蓝色的硝酸铜溶液混在一起,使溶液呈绿色。为了验证推断是否正确,甲、乙、丙三位同学分别设计了三种方案进行验证:
①甲同学方案:将盛绿色溶液的试管加热,看是否有红棕色气体产生。
你认为甲同学的方案是否妥当?为什么?________________________________________
②乙同学方案:用双氧水和二氧化锰制得氧气,并把氧气通入绿色溶液中,观察其溶液是否变蓝色。请用方程式表示其中的反应原理_______________________________________________
③丙同学方案:在通风橱内,将一根下端弯成螺旋状且可抽动的铜丝插在盛有足量浓硝酸的试管甲中,立即可观察到试管中充满红棕色的NO2气体。将气体经导管通入到倾斜的另一支盛有淡蓝色Cu(NO3)2试管乙中,随着实验进行,试管乙中的溶液蓝色加深,很快又变成绿色,继续通入NO2,绿色保持不变,向上抽起铜丝,使反应停止。写出铜与浓硝酸反应的离子方程式:________________________________________________________________________。
④从环保的角度看,你认为三个方案中最好的是哪一个?__________。其原因是__________
答案:(1)不同意 铜片质量相同,溶液体积相同,生成的铜离子浓度相同
(2)①不妥当,硝酸是过量的,加热过程中因为硝酸的分解也会产生二氧化氮,应当通过观察其溶液是否变蓝色来加以验证②4NO2+2H2O+O2===4HNO3
③Cu+4H++2NO===Cu2++2NO2↑+2H2O ④乙 乙方案中没有有毒气体产生
4. 铜及其化合物一般都具有特征的颜色,例如Cu、Cu2O呈红色,CuO呈黑色,CuSO4·5H2O呈蓝色等。研究性学习小组甲为检测实验室的Cu2O试样中是否含有Cu进行了认真的探究。
Ⅰ.查阅资料:①Cu2O属于碱性氧化物; ②在空气中灼烧Cu2O生成CuO;③Cu2O在酸性条件下能发生自身氧化还原反应(Cu2O+2H+=Cu+Cu2++H2O)。
Ⅱ.设计实验方案:
方案1:取该红色试样溶于足量的稀硝酸中,观察溶液颜色变化
方案2:取该红色试样溶于足量的稀硫酸中,观察是否有残渣
方案3:称得干燥坩埚的质量为a g ,取红色试样置于坩埚中称得总质量为b g,在空气中充分灼烧至完全变黑,并在干燥器中冷却,再称量。如此反复多次直到质量不变,称得最后质量为c g。分析数据,作出合理判断。
(1)请你评价方案1和方案2。如果你认为该方案合理,请简述其工作原理;如果你认为该方案不合理,请简述原因。
(2)方案3中,如果a、b、c的关系符合c= 可确认红色粉末是Cu2O
Ⅲ.研究性学习小组乙,设计了新的探究方案,装置如图所示。

(3)简述新探究方案中,气体发生装置的气密性如何检验(操作、现象、结论):
(4)你认为依据新方案测定上述红色试样成分必须获得下列哪些物理量:(选填序号)
①通入氢气体积;②反应前,红色试样+硬质试管的总质量;③完全反应后红色固体+硬质试管的总质量;④实验前,干燥管(含药品)的质量;⑤硬质试管质量;⑥锌粒质量;⑦稀硫酸中含溶质的量;⑧实验后,干燥管(含药品)的质量
(5)有人提出,在氢气发生器与硬质试管之间应加一个干燥装置,你认为 (选填“需要”或“不需要”),简述理由
答案(1)方案Ⅰ不合理,铜和氧化亚铜都能和硝酸生成Cu2+;方案Ⅱ不合理,Cu+在酸性条件下能发生自身氧化还原反应,也生成了铜单质。(2)c= (10b-a)(3)关闭活塞,从长颈漏斗向试管中注入一定量的水,使漏斗内液面高于试管内液面,静置后若漏斗内液面不下降,则装置的气密性良好;液面下降,则装置漏气
(4)②③⑤(5)需要 反应后,应让铜粉在氢气流中冷却,如没有干燥管,铜粉将吸湿。
3.某化学小组利用实验室提供的下列试剂:铁粉、0.1mol·L-1FeCl3溶液、0.1mol·L-1FeCl2溶液、KSCN溶液、新制氯水,探究Fe2+ 、Fe3+ 的氧化性、还原性,并对实验结果加于应用。
(1)根据氧化还原的有关原理,兴趣小组对Fe2+、Fe3+ 的还原性、氧化性提出了如下2种假设:假设一:Fe2+ 既有还原性又有氧化性; 假设二:Fe3+ 具有氧化性;
(2)设计实验方案,进行实验并描述实验现象,完成下列表格。
|
探究内容 |
实验方案 |
实验现象 |
|
探究Fe2+具有还原性 |
取少量0.1mol·L-1FeCl2溶液,加入足量新制氯水后,再往溶液中加入少量KSCN溶液 |
|
|
探究Fe3+具有氧化性 |
|
|
(3)该兴趣小组为说明“Fe2+具有氧化性”,提出了一个反应事实:FeCl2 + Zn = ZnCl2 + Fe
该反应的离子方程式为:
(4)根据Fe3+的性质,该小组用FeCl3溶液腐蚀铜箔制造印刷线路板,离子方程式是: ___
|
探究内容 |
实验方案 |
实验现象 |
|
探究Fe2+具有还原性 |
取少量0.1mol·L-1FeCl2溶液,加入足量新制氯水后,再往溶液中加入少量KSCN溶液 |
加入氯水后,溶液由浅绿色变黄色,再加入少量KSCN溶液后溶液变红色 |
|
探究Fe3+具有氧化性 |
取少量0.1mol·L-1FeCl3溶液,加入足量铁粉后,再往溶液中加入少量KSCN溶液 |
加入铁粉后,溶液由黄色变浅绿色,加入KSCN溶液后,溶液不显红 |
答案(2)
(3)Fe2++Zn =Zn2+ + Fe (4)2Fe3+ + Cu=2Fe2++ Cu2+
1. 某固体混合物可能含Al、(NH4)2SO4、MgCl2、A1Cl3、FeCl3中的一种或几种,现对该混合物作如下实验,所得现象和有关数据如图(气体体积已换算成标况下的体积):
某固体混合物可能含Al、(NH4)2SO4、MgCl2、A1Cl3、FeCl3中的一种或几种,现对该混合物作如下实验,所得现象和有关数据如图(气体体积已换算成标况下的体积):
请回答:
(1)混合物中是否存在FeCl2 (填“是”或“否”); ,
(2)混合物中是否存在(NH4)2SO4 (填“是”或“否”),你的判断依据是_______。
(3)写出反应⑤的离子反应方程式; 。
(4)请根据图中数据分析,原固体混合物中一定含有的物质为 (写化学式),不写计算过程。
(5)把AlCl3溶液加热浓缩蒸干,不能得到较纯的A1Cl3晶体,请你设计一个可行的简易实验从溶液中得到较纯的AlCl3结晶: 。
答案:(1)否 (2)是 气体通过浓硫酸减少4.48L (3)A1(OH)3++3H+=A13++3H2O
(4)一定含有A1、(NH4)2SO4和MgCl2三种物质
(5)往氯化铝溶液中加入一定量的浓盐酸后,再加热浓缩析出晶体。
 2.氯化铜晶体中常含FeC12杂质,为制得纯净氯化铜晶体(CuC12·2H2O),首先将其溶于稀盐酸中,然后按下面所示操作步骤进行提纯。
2.氯化铜晶体中常含FeC12杂质,为制得纯净氯化铜晶体(CuC12·2H2O),首先将其溶于稀盐酸中,然后按下面所示操作步骤进行提纯。
已知:
|
|
氢氧化物开始沉淀时的pH |
氯氧化物沉淀完全时的pH |
|
Fe3+ |
1.9 |
3.2 |
|
Cu2+ |
4.7 |
6.7 |
(1)下列物质中,最适合作为氧化剂X的是 (填序号)
A.H2O2 B.KMnO4 C.NaC1O D.浓硫酸
写出加入X后发生反应离子的方程式 。
(2)加入的物质Y可以是 ,目的是
(3)某同学利用反应Cu+2H+ Cu2++H2↑
设计实验来制取氯化铜溶液。该同学设计
的装置应该为 。(填“原电
池”或“电解池”)。请在右侧方框中画出
该同学设计的装置图,并指明电极材料和
电解质溶液。
(4)从CuC12稀溶液中得到CuC12·2H2O晶体,在蒸发结晶的过程中,为了防止Cu2+的水解,应采取的措施是 。
 答案:(1)A 2Fe2++H2O2+2H+
2Fe3++2H2O
答案:(1)A 2Fe2++H2O2+2H+
2Fe3++2H2O
(2)CuO或Cu(OH)2或CuCO3(2分);调节溶液的pH,只生成Fe(OH)3沉淀(2分);

(3)电解 (4)加入适量稀盐酸
2、注意事项:用稀硫酸作催化剂,而酯化反应则是用浓硫酸作催化剂和吸水剂。
在验证水解产物葡萄糖时,须用碱液中和,再进行银镜反应或与新制Cu(OH)2悬浊液的反应。
实验探究题精选:
1、实验步骤:在一支洁净的试管中加入蔗糖溶液,并加入几滴稀硫酸,将试管放在水浴中加热几分钟,然后用稀的NaOH溶液使其呈弱碱性。
2、注意事项:(1)Cu(OH)2必须是新制的(2)要加热至沸腾(3)实验必须在碱性条件下(NaOH要过量)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com