
2、线上只标出转移电子的总数。
巩固性练习、用双线桥法和单线桥法表示下列氧化还原反应的电子转移。
MnO2+4HCl(浓)==MnCl2+C12↑+2H2O
2NaBr+Cl2===2NaCl+Br2
1、箭号由还原剂中失电子的元素指向氧化剂中得电子的元素;
2、线上标出得失电子的情况及价的升降、被氧化或被还原等内容。

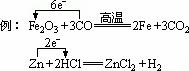
氧化剂为Fe2O3,还原剂为CO,氧化产物为CO2,还原产物为Fe。
●单线桥法
●双线桥法
1、双箭号从反应物指向生成物,箭号起止所指的均为同一种元素。

 联系:
联系:
氧化剂(具有氧化性)→所含元素化合价降低→得电子→被还原剂还原→发生还原反应→得还原产物。
还原剂(具有还原性)→所含元素化合价升高→失电子→被氧化剂氧化→发生氧化反应→得氧化产物。

巩固性练习:铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾.更强,本身在反应中被还原为Fe3+
化学反应方程式为:2Fe(NO3)3+16NaOH+3C12=2Na2FeO4+6NaNO3+8NaCl+6H2O
反应中的氧化剂是 还原剂是 ;反应中 元素被氧化,转移电子总数是
(二) 、从电子转移的角度认识氧化还原反应
|
反应 |
化合价升降 |
电子转移 |
氧化还原情况 |
|
2Na+Cl2==2NaCl |
钠元素 氯元素 |
钠 氯 |
Na发生 反应,被 Cl2发生 反应,被 |
|
H2+Cl2==2HCl |
氢元素 氯元素 |
氢 氯 |
H2发生 反应,被 Cl2发生 反应,被 |
小结:1、从反应前后电子转移的角度看,氧化还原反应是有 的反应;(氧化还原反应的本质)
2、氧化反应是物质 (填“得到”或“失去”)电子的反应;还原反应是物质 (填“得到”或“失去”)电子的反应。
3、氧化还原反应的本质是
4、在氧化还原反应中,失去电子的物质是 ,得到电子的物质是 。
氧化剂: 电子;化合价 ;发生 反应(具有 性);
还原剂: 电子;化合价 ;发生 反应(具有 性)。
5、氧化反应与还原反应同时发生,既对立又统一,在反应中化合价上升和下降总数相等,得到电子和失去电子总数相等。
6、氧化还原反应与四种基本类型反应的关系为:
置换反应全部属于氧化还原反应,复分解反应全部属于非氧化还原反应,
有单质参加的化合反应和有单质生成的分解反应全部属于氧化还原反应。
(一)、从元素化合价升降的角度认识氧化还原反应
|
反应 |
是否氧化 还原反应 |
“得”还是 “失”氧 |
化合价升降 |
氧化还原情况 |
|
C+2CuO==2Cu+CO2 |
|
C 氧, CuO 氧 |
碳元素 铜元素 |
C发生 反应,被 CuO发生 反应,被 |
|
C+H2O==H2+CO |
|
C 氧, H2O 氧 |
碳元素 氢元素 |
C发生 反应,被 H2O发生 反应,被 |
小结:①从反应前后元素化合价是否升降看,氧化还原反应是有 的反应(氧化还原反应的特征);②氧化反应是物质所含元素化合价 (填“升高”或“降低”)的反应;还原反应是物质所含元素化合价 (填“升高”或“降低”)的反应。
20.(本小题满分14分)
设 是定义在
是定义在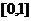 上的函数,若存在
上的函数,若存在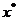
 ,使得
,使得 在
在 上单调递增,在
上单调递增,在 上单调递减,则称
上单调递减,则称 为
为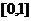 上的单峰函数,
上的单峰函数,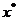 为峰点,包含峰点的区间为含峰区间. 对任意的
为峰点,包含峰点的区间为含峰区间. 对任意的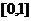 上的单峰函数
上的单峰函数 ,下面研究缩短其含峰区间长度的方法.
,下面研究缩短其含峰区间长度的方法.
(1)证明:对任意的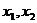
 ,
,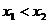 ,若
,若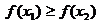 ,则
,则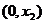 为含峰区间;若
为含峰区间;若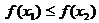 ,则
,则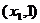 为含峰区间;
为含峰区间;


(2)对给定的 ,证明:存在
,证明:存在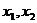
 ,满足
,满足 ,使得由(1)所确定的含峰区间的长度不大于
,使得由(1)所确定的含峰区间的长度不大于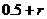 ;
;
19.(本小题满分14分)
各项均为正数的数列{an}的前n项和Sn,函数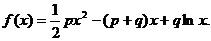
(其中p、q均为常数,且p>q>0),当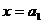 时,函数f(x)取得极小值,点
时,函数f(x)取得极小值,点 均在函数
均在函数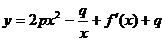 的图象上,(其中f′(x)是函数f(x)的导函数)
的图象上,(其中f′(x)是函数f(x)的导函数)
(1)求a1的值;
(2)求数列 的通项公式;
的通项公式;


(3)记 的前n项和Tn.
的前n项和Tn.
18.(本小题满分14分)
 已知点C为圆
已知点C为圆 的圆心,点A(1,0),P是圆上的动点,点Q在圆的半径CP上,且
的圆心,点A(1,0),P是圆上的动点,点Q在圆的半径CP上,且
(Ⅰ)当点P在圆上运动时,求点Q的轨迹方程;
(Ⅱ)若直线 与(Ⅰ)中所求点Q
与(Ⅰ)中所求点Q
的轨迹交于不同两点F,H,O是坐标原点,
且 ,求△FOH的面积.
,求△FOH的面积.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com