
2.每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦擦干净后,再选涂其他答案标号。答在试卷上的答案无效。
选择题(本大题共22小题,每小题2分,共44分。在每小题给出的
四个选项中,只有一项是符合题目要求的)
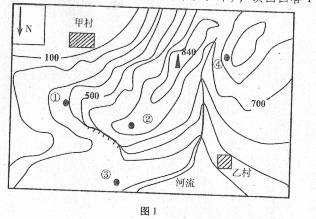
图1为北半球某地等高线示意图(单位:米),读图回答1~4题。
30.(14分)
I.(9分)
某研究小组成员在讨论鉴别浓硫酸和稀硫酸的方案时,设计了如下方案:
|
|
操作 |
结论 |
|
甲 |
火柴梗 |
变黑者为浓硫酸 |
|
乙 |
加入金属铝片 |
产生刺激性气味者为浓硫酸 |
|
丙 |
分别加入到盛水的试管中 |
放热者为浓硫酸 |
|
丁 |
用玻璃棒蘸浓氨水靠近盛酸的瓶口 |
冒白烟者为浓硫酸 |
|
戊 |
加到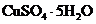 晶体中 晶体中 |
变白者为浓硫酸 |
请回答下列问题:
(1)其中可行的是 。
(2)其中一个稍作改进就能成为可行的是 ,改进方法是
。
(3)完全错误的是 ,因为 。
II.(5分)
另一研究小组成员从化学手册上查知硫酸铜在500℃以上按下式分解:
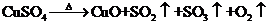 ,便决定设计一个验证性实验探究测定反应产生的
,便决定设计一个验证性实验探究测定反应产生的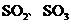 。和O2的物质的量,并经计算确定该条件下CuSO4分解反应方程式中各物质的化学计量数。实验可能用到的仪器如图8所示:(假定每步吸收都是完全的)
。和O2的物质的量,并经计算确定该条件下CuSO4分解反应方程式中各物质的化学计量数。实验可能用到的仪器如图8所示:(假定每步吸收都是完全的)
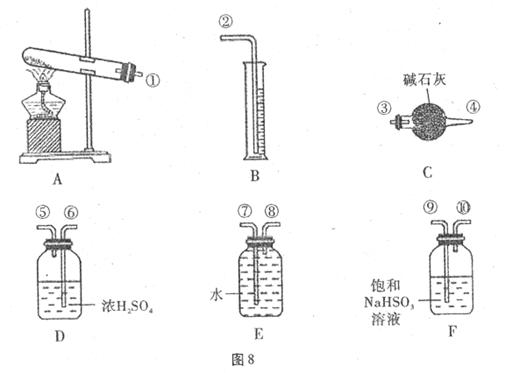
实验测得数据及有关结果如下:
①准确称取12.0g无水CuSO4;
②干燥管总质量在实验结束时增加了m g;
③测出量筒中水的体积后,折算成标准状况下气体的体积为560mL;
④实验结束时,装置F中的溶液变为NaHSO4溶液(不含其他溶质)。
试回答下列问题:
(1)按装置从左到右的方向,各仪器接口连接顺序为 (每种装置只使用一次)。
(2)通过计算m= g,推断出该条件下反应的化学方程式:
。


29.(10分)
图7中,A、C是工业上用途很广的两种重要的酸和碱,B为日常生活中常见的金属,H、G是正四面体结构的非极性分子,H是一种重要的气体能源,J是一种耐高温材料,K是由常见元素组成的化合物(图中部分反应物或生成物没有列出)。请按要求回答:
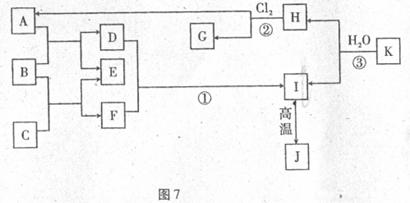
(1)写出B的名称 ,G的化学式 ,K的化学式 。
(2)反应①的离子方程式为 。
(3)写出B和C反应的离子方程式 。
28.(6分)
臭氧与氧气的关系为 ,O3有非常强的氧化性,将少量臭氧通入KI溶液中,发现有以下现象:溶液颜色变成黄色,并测得溶液的pH大于7,同时有一种无色无味的气体放出,该气体能使带火星的木条复燃。写出上述反应的化学方程式 ,
1mol O3发生反应时,转移的电子为 mol。
27.(10分)
A、B、C是短周期主族元素,且原子序数依次增大,A元素的原子最外层电子数是次外层电子数的3倍,B和C的原子序数之和是A的原子序数的3倍,B和C形成的离子具有相同的电子层结构。试回答下列问题:
(1)C离子的结构示意图是 ;由A和B形成的含有非极性键的离子化合物的电子式是 :
(2)B离子半径 (填“<”或“>”)C离子半径,B和C元素最高价氧化物的水化物之间反应的离子方程式为 ;
(3)化合物X由元素A、B、C组成,写出X的溶液与过量盐酸反应的离子方程式:
。
26.(10分)
含六个碳原子的烷烃A只可能有三种一氯取代产物B、C和D。B和D分别与强碱的醇溶液共热,都只能得到有机化合物E。C在强碱的醇溶液中不能反应。以上反应及B的进一步反应如图6所示。
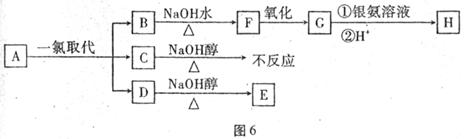
请回答下列问题:
(1)C的结构简式是 。
(2)B转变为F的反应属于 反应(填反应类型名称,后同),D转变为E的反应属于 反应。
(3)①写出F转化为G的化学方程式 ;
②G转化为H的化学方程式为 。
25.将某种由FeS和FeS2组成的混合物在空气中充分燃烧,得到标准状况下15.68L SO2气体;将燃烧后的固体粉碎后溶于足量的盐酸中过滤并向滤液中加入足量NaOH溶液,再将沉淀滤出灼烧至恒量,得到三氧化二铁40g,则该混合物中 和
和 的物质的量之比为
的物质的量之比为
A.2:3 B.3:2 C.2:l D.1:l
第Ⅱ卷(非选择题,共5小题,共50分)
本卷用黑色碳素笔将答案答在答题卡上,答在试题卷上的答案无效。
24.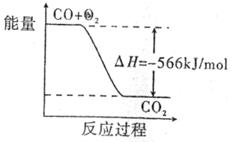 已知:
已知: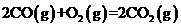
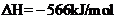
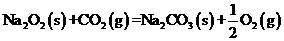
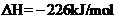 根据以上热化学方程式判
根据以上热化学方程式判
断,下列说法正确的是
A.CO的燃烧热为283kJ
B.图5可表示由CO生成CO2的反应过程和能
量关系
C.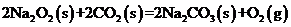
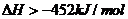
D.CO(g)与Na2O2(s)反应放出509kJ热量时,电子转移数为6.02×1023
23.下列实验设计和结论相符的是
A.将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中
B.某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性
C.某无色溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有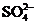
D.在含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热,除去过量的Cl2,即可得到较纯净的FeCl3溶液
22.W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7:17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是
A.金属性:Y>Z B.氢化物的沸点:X>W
C.离子的还原性:X>W D.原子及离子半径:Z>Y>X
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com