
2.勒沙特列原理
如果改变平衡的一个条件(如浓度、温度、压强等),平衡就会向 的方向移动。
[例2] (08天津卷)对平衡CO2(g) CO2(aq);△H= -19.75kJ/mol,为增大二氧化碳气体在水中的溶解度,应采用的方法是( )
CO2(aq);△H= -19.75kJ/mol,为增大二氧化碳气体在水中的溶解度,应采用的方法是( )
A.升温增压 B.降温减压 C.升温减压 D.降温增压
[解析] 增大二氧化碳气体在水中的溶解度,即使平衡向正向移动,而正向为一气体体积减少同时放热,因此可以降低温度,同时还可增大压强。
[答案]D。
特别提醒:改变固体或纯液体的量.化学平衡不移动;恒温、恒容时,通入稀有气体,化学平衡不移动;恒温、恒压时,通入稀有气体,化学平衡向着气体分子数增大的方向移动;加入一种反应物后另一种反应物的转化率会增大,其本身的转化率反而减小;对于等体积反应,改变体系压强对化学平衡无影响。
考点3化学平衡图象
解平衡图象要注意识图方法,总的来说有以下几点:
一看面(即横坐标和纵坐标);
二看线(即看线的走向、变化的趋势);
三看点(看线是否通过原点,两条线的交点及线的拐点)(重点理解);
四看辅(要不要作辅助线,如等温线、等压线);
五看数 (定量图像中有关数值的多少大小)。
[例3](08全国Ⅰ卷)已知:4NH3(g)+5O2(g)=4NO(g)+6H2(g). △H=-1025kJ/mol该反应是一个可逆反应。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是( )
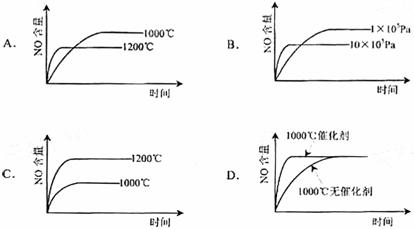
[解析]根据“先拐先平数值大”的原则,选项A、B正确;根据升高温度,平衡向吸热反应方向移动(即逆反应方向移动),可确定A、B正确;根据使用催化剂只能改变化学反应速率,缩短达到平衡的时间,但对化学平衡的移动无影响,所以选项D正确。
[答案]C
[方法技巧]化学平衡经常会以图像来考查,不仅要掌握影响化学平衡的因素及勒沙特列原理,同时还要掌握识图的方法和一些规律,如“先拐先平数值大”和“定一议二”等原则。
考点4等效平衡规律
1.影响化学平衡的条件
主要有 和间接条件等。
要注意的是:使用催化剂可以改变反应速率但是不能使化学平衡移动。因为催化剂能同等程度的改变正、逆反应的反应速率,始终有v(正)=v(逆),故不会影响化学平衡移动,但可以大大提高反应速率,缩短达到平衡的时间,从而提高生成物的产率。
3.化学平衡状态的判定
|
例 举 反 应 |
m
A(g) + n B(g)  p C(g) + q D(g) p C(g) + q D(g) |
|
|
混合物体系中各成分的含量 |
各物质的
物质的量或各物质的质量分数一定 |
平衡 |
|
各物质的质量或物质的质量分数一定 |
平衡 |
|
|
各气体的体积或体积分数一定 |
平衡 |
|
|
总体积、总压强、总物质的量一定 |
不一定平衡 |
|
|
正、逆反应速率相等 |
在单位时间内消耗了m mol A,同时也生成了m mol A,即v(正)=v(逆) |
平衡 |
|
在单位时间内消耗了n mol B,同时也消耗了p mol C,即v(正)=v(逆) |
平衡 |
|
|
v(A): v(B): v(C):
v(D)=m:n:p:q,v(正)不一定等于v(逆) |
不一定平衡 |
|
|
在单位时间内生成了n mol B,同时也消耗了p mol C,因均指v(逆) |
不一定平衡 |
|
|
压强 |
m + n ≠ p + q 时,总压强一定(其他条件一定) |
平衡 |
|
m + n = p + q 时,总压强一定(其他条件一定) |
不一定平衡 |
|
|
混合气体的平均相对分子质量M r |
M r一定时,且m + n ≠ p + q时(非气体的不算) |
平衡 |
|
M r一定时,且m + n = p + q时(非气体的不算) |
不一定平衡 |
|
|
温度 |
任何化学反应都伴有能量的变化,当体系温度一定时(其他不变) |
平衡 |
|
气体的密度 |
密度一定 |
不一定平衡 |
|
颜色 |
反应体系内有色物质的颜色稳定不变 |
平衡 |
注意:“同边异,异边同”原理(平衡的判断方法之一)
同一边的物质(都是反应物或者都是生成物)一个“消耗”一定量,同时另一个“生成”一定量才可以说明是达到了平衡;而两个不同一边的物质(一个是反应物而另一个是生成物)都“同时消耗”一定量或者“同时生成”一定量也可以表示达到了平衡。
[例1]对可逆反应A2(g)+B2(g) 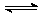 2AB(g) 在一定条件下,达到平衡状态的标志是( )
2AB(g) 在一定条件下,达到平衡状态的标志是( )
A、平衡时容器内各物质的物质的量比为1∶1∶2
B、平衡时容器内的总压强不随时间而变化
C、单位时间内生成2n mol AB的同时,生成n mol的B2
D、单位时间内,生成n mol A2的同时,生成n mol的B2
[解析] 平衡时容器内各物质的物质的量之比是没有规律的,只是各物质的物质的量浓度保持不变是一般规律,A错;对于反应前后气体不变的反应,容器内的总压强不随时间的变化而改变,无论是否平衡!B不能选择;对于C,D 类型需要了解六个字的“同边异,异边同”原理,对于D,如果反应向左进行,单位时间内,本来就是生成n mol A2的同时,一定生成了n mol的B2;对于C,表示反应向左进行的同时也在向右进行,而且程度相同!所以是正确的。
[答案]C
[方法技巧]“同边异,异边同”原理是一个很实用的原理,在学习中要灵活利用!
考点2化学平衡的影响因素及勒沙特列原理
2. 化学平衡的特征:
(1)化学平衡研究的对象是可逆反应;(逆)
(2)达到平衡时正反应速率等于逆反应速率;(等)
(3)达到平衡时反应混合物中各组分的浓度 ;(定)
(4)由于化学平衡状态时反应仍在进行,故其是一种 ; (动)
(5)条件改变平衡会发生移动.(变)
1. 定义:是指在一定条件下的 里,正反应和逆反应的 相等,反应体系中所有参加反应的物质的质量或浓度可以 的状态。
29.鉴赏古代诗词,感悟深刻哲理,传承中华文化:
唐代大诗人白居易的诗:“离离原上草,一岁一枯荣。野火烧不尽,春风吹又生。”
宋代诗人陈与义的诗:“飞花两岸照船红,百里榆堤半日风。卧看满天云不动,不知云与我俱动。”
请问:以上白居易和陈与义的古诗分别反映了什么哲学思想?(10分)
28.在一次大型科普展览中,有一个别具匠心的设计:三扇门上各有一个问题:“污染环境的是谁?”“饱受环境恶化之苦的是谁?”“保护环境的应该是谁?”拉开门,里面各是一面镜子,照出的是参观者自己。
这一巧妙的设计给我们什么启示?(4分)试说明理由。(10分)
27.甲认为,“万事万物都是由水构成的”;乙认为,“自然是绝对理念的外化,社会是绝对精神的体现”。
(1)甲、乙两人的观点分别属于哪两种哲学阵营?(4分)
(2)乙所在的哲学阵营可以划分为哪两种形态?(4分)基本观点各是什么?(8分)
(3)它们的根本分歧是什么?(2分)
26.哲学家周国平先生说:好奇心是人的理性的开端,人人都有好奇心,人人都可能是哲学家。而德国哲学家黑格尔又说:每个人都可以大谈哲学,但并非每个人都是哲学家。
请结合所学知识谈一谈对这两句话该如何理解?(8分)
25.“天地之变,寒暑风雨,水旱螟蝗,率皆有法。”这句话包含的哲学道理是( )
A.规律是事物本质的必然的联系
B.只有自然界的运动是有规律的
C.规律可以为人所认识
D.一切事物的运动都是有规律的
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com