
3.下列关于重心的说法正确的是( )
A重心是物体的各部分所受重力的合力的作用点。
B形状规则的物体的重心必与其几何中心重合。
C重心是物体上最重的一点。
D直铁丝被弯曲后,重心便不在中点,但一定还在铁丝上。
2.关于重力的说法中正确的是( )
A.在落向地球时,物体受的重力大于它静止时受的重力。
B.因重力的方向总是竖直向下的,故重力一定和地面重直。
C.重力就是物体对水平桌面的压力。
D.一个物体不论是静止还是运动,也不论是怎么运动,受到的重力都是一样。
1.下列力的说法中正确的是( )
A..力是物体对物体的作用,所以只有直接接触的物体间才有力的作用。
B. 由有一定距离的磁铁间有相互作用力可知,力可以离开物体而独立存在。
C. 力是使物体发生形变和改变物体运动状态的原因。
D. 力的大小可以用天平测量。
28.(10分) 取0.04molKMn04固体加热一段时间后,收集到amol气体,在反应后的残留固体中加入一定量的浓盐酸,又收集到bmol气体,设此时Mn元素全部以Mn2+存在于溶液中, 试求:
(1) a+b的最小值?
(2) 当a+b=0.09mol时,残留固体的质量为多少?
27.(12分)已知某饱和NaCl溶液的体积为VmL,密度为 g·cm-3,质量分数为
g·cm-3,质量分数为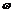 %,物质的量浓度cmol·L-l,溶液中含NaCl的质量为mg。通过计算求:
%,物质的量浓度cmol·L-l,溶液中含NaCl的质量为mg。通过计算求:
(1) 用m、V表示溶液物质的量浓度,
(2)
用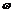 、
、 表示溶液物质的量浓度,
表示溶液物质的量浓度,
(3)
用c、 表示溶液的质量分数,
表示溶液的质量分数,
(4)
用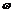 表示该温度下NaCl的溶解度。
表示该温度下NaCl的溶解度。
26.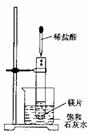 (8分)如右图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5 mL盐酸于试管中。试回答下列问题:
(8分)如右图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5 mL盐酸于试管中。试回答下列问题:
(1)实验中观察到的现象是:
(2)产生上述现象的原因是:
(3)写出有关反应的离子方程式:
(4)由实验推知,MgCl2溶液的总能量
(填“大于”、“小于”、“等于”)镁片和盐酸的总能量。
25.(8分)配制100mL0.25mol·L-1的NaOH溶液,某学生操作如下:
(1)用托盘天平称出1.00 gNaOH,操作是:将天平调好零点,再在两盘上各放一张同样质量的滤纸,把游码放在1 g的位置上,在左盘上放粒状NaOH至天平平衡,取下称好的 NaOH,并撤掉两盘上的纸;
(2)把称好的NaOH放入一个100mL的烧杯中,加入约10 mL水,搅拌使之溶解,溶解后立即用玻璃棒引流,将溶液移至一个100mL的容量瓶内,加水至距刻度线约2cm处,改用胶头滴管加水,恰至刻度;
(3)写一个记有配制日期的“0.2500mo1·L-1NaOH溶液”的标签,贴在容量瓶上,密闭保存。
指出上述操作和描述中的错误:
①
②
③
④
⑤
⑥
⑦
⑧
24.(8分)一瓶溶液里可能含有OH-、Cl-、NO3-、CO32-和SO42-五种阴离子的某几种。现分别取该溶液少量装于两支试管,进行以下实验:
①向第一支试管中滴入酚酞试液,溶液变红。
②向第二支试管中加入足量Ba(NO3)2溶液,生成白色沉淀。过滤,并将滤液移入第三支试管,在沉淀中加入稀硝酸,沉淀逐渐消失并有无色无味气体产生,该气体通入澄清石灰水,石灰水变浑浊。
③向第三支试管中加入少量AgNO3溶液,无现象。
通过以上实验可判断溶液中含有的离子为
。
不含有的离子为
无法确定是否含有的离子为
写出实验②中有关反应的离子方程式:
23.(10分)去年2月25日汉江再次发生严重的“水华”现象。“水华”主要是指向水中投入或排人生物所需的营养物质后,水中某些营养元素含量过高,导致水面上的藻类疯狂生长、繁殖,水质恶化而有腥臭味,造成鱼类死亡的现象。
(1)已知藻类含碳35.83%,氢7.41%,氮6.31%,磷0.8732%,其余为氧,式量不超过4000,则该藻类的式量为
,
化学式为 。
(2)根据藻类的化学式确定,工业和生活污水中导致藻
类生长过快的营养元素是 。
(3)为解决汉江污染问题,湖北省正式实施《湖北省汉江流域水污染防治条例》。条例规定:实行“污染源头”控制,严格管制沿江主要城市的污水排放……。下列措
施符合此条例规定的是(填写序号) 。
①汉江沿岸在新建住宅小区、宾馆、饭店、医院等采用生活污水净化装置;②汉江沿岸城市居民禁用含磷洗衣粉;③禁止用汉江水进行农用灌溉和作生活用水;④向汉江中加入大量净水剂和消毒剂以提高汉江的水质。
(4)汉江的“水华”现象发生在枯水期的原因是:
22.(8分)判断含氧酸强弱的一条经验是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强。如下表所示:
某些含氧酸的酸性
|
名称 |
次氯酸 |
磷酸 |
硫酸 |
高氯酸 |
||||||||
|
结构式 |
|
|
|
|
||||||||
|
非羟基氧原子数 |
0 |
1 |
2 |
3 |
||||||||
|
酸性 |
弱酸 |
中强酸 |
强酸 |
最强酸 |
(1)亚磷酸(H3P03)和亚砷酸(H3AsO3)的化学式相似,但是它们的酸性差别很大。亚磷酸是中强酸,亚砷酸既有弱酸性又有弱碱性。由此可以推知它们的结构分别为
①
②
(2)亚磷酸和亚砷酸分别跟过量氢氧化钠反应的化学方程式分别是
①
②
(3)在亚磷酸和亚砷酸中分别加入浓盐酸,分析反应情况,写出化学反应方程式
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com