
2.[解析]由题设条件,可看作气体A的式量为m,气体B的式量为n(这是至为关键的)本题即为阿佛加德罗定律及引伸的运用,显然在运用时注意前提条件A中缺少同温同压条件,只有同温同压下,体积相同,则A、B物质的量相同。质量比才为m:n,而B中与温度压强没有关系,但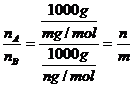 ,C中同温同压密度比等于其式量比,应为m:n,因此正确答案为A、B、C。
,C中同温同压密度比等于其式量比,应为m:n,因此正确答案为A、B、C。
[答案]D
[考题再现]
1.[解析]由于含个微粒为1mol ,所以含个H原子的中含氢原子为1mol,而1个氢分子中含有2个氢原子,则含个H原子的的物质的量为0.5mol。选项A错。由于CO和的摩尔质量相同,故个分子的质量也相同,且为了加28g,故选项B正确。1mol和分别含有2mol H和3mol H,故选项C错。5.6g铁离子为0.1mol ,得到0.2mol 电子后,刚好全部形成原子。故选项D正确。
[答案]B、D
17.向某二价金属M的氢氧化物澄清溶液100毫升中加入过量的NaHCO3溶液生成MCO3沉淀,过滤,将沉淀置于足量盐酸中放出标准状态下的气体4.48升。将滤液加水稀释到250毫升,取出25毫升恰好与20毫升盐酸完全反应,并在标准状态下收集到1.12升气体。
⑴写出M的氢氧化物澄清溶液与NaHCO3溶液反应的化学方程式
⑵要计算金属M的相对原子质量,你认为还必须提供下列哪项数据?(填标号)
A.M的氢氧化物的物质的量的浓度(设为2mol/L)
B.M的碳酸盐的质量(设为39.4克)
C.与M的碳酸盐反应的盐酸的物质的量浓度
D.题给条件充足,不需要补充数据
⑶根据你的选择计算金属M的相对原子质量和加入NaHCO3溶液中NaHCO3的质量
第 三章 物质的量第一课时 物质的量和气体摩尔体积
[例题解析]
15.用向下排气法在容积为V mL的集气瓶中收集氨气,由于空气尚未排净,最后瓶内气体的平均式量为19,将此盛满气体的集气瓶倒置于水中,瓶内水马上升到一定高度后,即停止上升,则在同温同压下,瓶内剩余气体的体积为( )
A.  mL B.
mL B.
 mL C.
mL C.
 mL D.
无法判断
mL D.
无法判断
16在天平的两个托盘上各放一个盛有等体积稀硫酸的烧杯(每杯溶液中都含有mmol的H2SO4),调节天平使其平衡。然后在一个烧杯中加入ag铁粉,在另一个烧杯中加入bg镁粉,充分反应后,天平仍平衡。试用代数式表示在下列各种情况下,a与b的关系(关系式中可含m)。
①若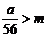 ,
, 时,___________________________。
时,___________________________。
②若 ,
,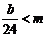 时,___________________________。
时,___________________________。
③若 ,
, 时,___________________________。
时,___________________________。
D.奥赛一瞥
14.P和O2放在两容器中,控制不同条件,分别发生:4P+3O2=2P2O3(容器1),4P+5O2=2P2O5(容器2),若在两容器中分别放1mol P和1mol O2,充分反应后得到P2O3和P2O5的物质的量之比是
A. 1∶1 B. 5∶4 C. 4∶3 D. 5∶3
13.H2和O2的混合气体,在120℃和101 kPa下体积为aL,点燃使其反应后恢复至原条件,其体积变为bL,则原混合气体中O2为 ( )
A. b L B.(a-b)L C. (2a-b)L D. (2b-a)L
12.一定温度下,物质W分解,其反应方程式4W  X3(g)+2Y(g),测得生成物组成的混合气体与H2的相对密度为18,则W的相对分子质量为 ( )
X3(g)+2Y(g),测得生成物组成的混合气体与H2的相对密度为18,则W的相对分子质量为 ( )
A. 27 B. 18 C. 36 D. 126
11.列说法正确的是 ( )
A.在标准状况下,1mol水的体积是22.4L
B.1mol H2所占的体积一定是22.4L
C.在标准状况下,NA个分子所占的体积约为22.4L
D.标准状况下,28g N2和CO混合气体,体积约为22.4L
10.反应3Cl2+6KOH  KClO3+5KCl+3H2O中,还原剂与氧化剂物质的量之比为( )
KClO3+5KCl+3H2O中,还原剂与氧化剂物质的量之比为( )
A. 1∶5 B. 1∶3 C. 5∶1 D. 3∶1
C.能力训练
9.某氮的氧化物和灼热的铁4NxOy+3yFe=yFe3O4+2x N2↑的反应进行反应,在一个特定的实验中,2mol该氧化物通过500g(过量)红热的铁,生成1mol N2和1mol Fe3O4,该氧化物的化学式为 ( )
A. NO B. NO2 C. N2O D. N2O4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com