
254£®BŌŚ25”ꏱ£¬“æĖ®µÄµēĄė¶ČĪŖ¦Į1£¬pH=3µÄ“×ĖįÖŠĖ®µÄµēĄė¶ČĪŖ¦Į2£¬pH=11µÄĒāŃõ»ÆÄĘČÜŅŗÖŠĖ®µÄµēĄė¶ČĪŖ¦Į3”£Čō½«ÉĻŹö“×ĖįČÜŅŗŗĶĒāŃõ»ÆÄĘČÜŅŗµČĢå»ż»ģŗĻ£¬ĖłµĆČÜŅŗÖŠĖ®µÄµēĄė¶ČĪŖ¦Į4£¬ŌņĻĀĮŠ¹ŲĻµÕżČ·µÄŹĒ”””””””””””””””””””” (”” ””)
”” A.¦Į1<¦Į3<¦Į2<¦Į4”””””””” ””B.¦Į3<¦Į2<¦Į1<¦Į4””
C.¦Į2=¦Į3<¦Į1<¦Į4”””””””””” ””D.¦Į2=¦Į3<¦Į4<¦Į1
253£®AĻņ0.1 mol”¤L£1µÄCH3COOHČÜŅŗÖŠ¼ÓČėCH3COONa¾§Ģå»ņ¼ÓĖ®Ļ”ŹĶŹ±£¬»įŅżĘš ”””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””” (”” ””)
A£®ČÜŅŗµÄpH¶¼Ōö¼Ó”””””””””” ”””””” B£®CH3COOHµēĄė³Ģ¶ČŌö“ó
C£®ČÜŅŗµ¼µēÄÜĮ¦¶¼¼õČõ”””””””””” ”” D£®ČÜŅŗÖŠc(OH£) ¶¼¼õŠ”
252£®AĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ”””””””””””””””””””””””””””””””””””””””””””” (”” ””)
A£®Ė®ŹĒ¼«ČõµÄµē½āÖŹ£¬ĖüÄÜĪ¢ČõµēĄėÉś³ÉĻąĶ¬ĪļÖŹµÄĮæµÄH+ŗĶOH£
B£®Ļ”ČÜŅŗÖŠc(H+)•c(OH£)=KW£¬ČĪŗĪĢõ¼žĻĀKW¶¼±£³Ö²»±ä
C£®ĪŽĀŪŌŚŹ²Ć“Ģõ¼žĻĀ£¬ÖŠŠŌČÜŅŗµÄc(H+)Ņ»¶ØµČÓŚ1”Į10£7mol/L
D£®H2O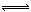 H++OH£ŹĒŅ»ĪüČČ·“Ó¦£¬ĖłŅŌĪĀ¶ČÉżøߣ¬KWŅ²ĖęÖ®Ōö“ó
H++OH£ŹĒŅ»ĪüČČ·“Ó¦£¬ĖłŅŌĪĀ¶ČÉżøߣ¬KWŅ²ĖęÖ®Ōö“ó
251£®AĖ®µÄµēĄė¹ż³ĢĪŖH2O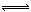 H++OH-£¬ŌŚ²»Ķ¬ĪĀ¶ČĻĀĘäĄė×Ó»żĪŖKw(250C)=1.0”Į10-14£¬Kw(350C)=2.1”Į10-14£¬ŌņĻĀĮŠŠšŹöÕżČ·µÄŹĒ£ŗ””””””””””””””””””””””””””””””
(”” ””)
H++OH-£¬ŌŚ²»Ķ¬ĪĀ¶ČĻĀĘäĄė×Ó»żĪŖKw(250C)=1.0”Į10-14£¬Kw(350C)=2.1”Į10-14£¬ŌņĻĀĮŠŠšŹöÕżČ·µÄŹĒ£ŗ””””””””””””””””””””””””””””””
(”” ””)
A£®c(H+)Ėę×ÅĪĀ¶ČµÄÉżø߶ų½µµĶ”””””””” B£®ŌŚ350CŹ±£¬c(H+)£¾c(OH-)
C£®Ė®µÄµēĄė³£ŹżKw(250C)£¾Kw(350C)”” D£®Ė®µÄµēĄėŹĒŅ»øöĪüČČ¹ż³Ģ
250£®AĻĀĮŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹéŠ“ÕżČ·µÄŹĒ”””””””””””””””””””””””””””””” (”” ””)
A£®ĻņĒāŃõ»ÆÄĘČÜŅŗÖŠĶØČėÉŁĮæCO2”” OH-+CO2=HCO3-
B£®ÓĆ°±Ė®ĪüŹÕÉŁĮæSO2”” 2OH-+SO2=SO32-+H2O
C£®ĻõĖįĀĮČÜŅŗÖŠ¼ÓČė¹żĮæ°±Ė®”” Al3++4NH3”¤H2O=AlO2-+4NH4++2H2O
D£®ĻņFe2(SO4)3µÄĖįŠŌČÜŅŗÖŠĶØČė×ćĮæH2S”” 2Fe3++H2S=2Fe2++S”ż+2H+
249£®BijŅ»ŌŖĖįŌŚ1mol/LµÄČÜŅŗÖŠµēĄė¶ČĪŖ0.001%£¬ŌņøĆČÜŅŗµÄµ¼µēÄÜĮ¦½Ó½üÓŚ (”””””” )
A£®1mol/L µÄNaOHČÜŅŗ”””””””””” B£®“æĖ®””
C£®10-6mol/LµÄNaOH”””””””””””””” D£®10-5mol/LµÄNaCl
248£®BŌŚŅ»¶ØĪĀ¶ČĻĀ£¬100mlijČõĖįHAČÜŅŗÖŠ£¬ŗ¬ÓŠøĆČõĖįµÄ·Ö×ÓŹżĪŖ5.42”Į1020øö£¬²¢²āµĆøĆČÜŅŗÖŠc(H+)=10-3mol/L£¬øĆČõĖįŌŚ“ĖĢõ¼žĻĀµÄµēĄė¶ČĪŖ£ŗ”””””””””””””” (”” ””)
”””” A£®9%”””””””””” B£®10%”””””””””” C£®3%”””””””””””” D£®0.1%
247£®AÖ÷ŅŖÓ°ĻģČõĖįµÄµēĄė³£ŹżÖµµÄŅņĖŲŹĒ”””””””””””””””””””””””””””””” (”” ””)
A£®ČÜŅŗµÄÅØ¶Č”””””””””””””””””” B£®ĖįµÄµēĄė¶Č””
C£®Ėį·Ö×ÓÖŠŗ¬ĒāŹż”””””””””””””” D£®ĖįµÄ±¾ÖŹŗĶČÜŅŗĪĀ¶Č
246£®AĻņHAcČÜŅŗÖŠ£¬¼ÓČėÉŁŠķĪļÖŹ£¬Ź¹HAcµēĄė¶Č¼õŠ”µÄŹĒ£ŗ”””””””” (”” ””)
A£®NaCl(¹ĢĢå)”””””””” B£®NaAc(¹ĢĢå)”””””””” C£®FeCl3(¹ĢĢå)”””””””””” D£®H2O
245£®Bc1”¢c2”¢¦Į1”¢¦Į2£¬pH1£¬pH2·Ö±š±ķŹ¾2ÖÖŅ»ŌŖČõĖįµÄĪļÖŹµÄĮæÅØ¶Č”¢µēĄė¶ČŗĶČÜŅŗµÄpHČē¹ūŅŃÖŖpH1<pH2,ĒŅ¦Į1>¦Į2,Ōņc 1ŗĶc 2µÄ¹ŲĻµ”””””””””””””””””””””””””””””” (”””””” )
A£®c 1> c 2”””””””””””” B£®c 1= c 2”””””””””””” C£®c 1< c 2”””””””””” ”” D£®ĪŽ·ØČ·¶Ø
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com