
264. A实验表明,液态时,纯硫酸的导电性强于纯水。已知液态电解质都能像水那样自身电离而建立电离平衡(即像H2O+H2O H3O++OH-那样),且在一定温度下都有各自的离子积常数。问在25℃时,纯硫酸的离子积常数K和水的离子积常数KW关系为___ ,纯硫酸电离方程式可表示为
。
H3O++OH-那样),且在一定温度下都有各自的离子积常数。问在25℃时,纯硫酸的离子积常数K和水的离子积常数KW关系为___ ,纯硫酸电离方程式可表示为
。
263. B重铬酸钾(K2Cr2O7)是橙色晶体,铬酸钾(K2CrO4)是黄色晶体,将重铬酸钾溶于水配成2%的溶液,重铬酸钾发生水解,反应的离子方程式如下:Cr2O72?+H2O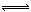 2CrO42-+2H+ 当达平衡时,溶液颜色介于橙色和黄色之间。
2CrO42-+2H+ 当达平衡时,溶液颜色介于橙色和黄色之间。
(1)滴入10滴2摩/升NaOH溶液于3毫升2%的K2Cr2O7溶液中,现象是________________, 理由__________________________;
(2)将3滴2摩/升H2SO4溶液加入上述(1)所得溶液中现象是____________________,理由____________________________________;
(3)在上述(2)所得溶液中,再滴入5滴2摩/升H2SO4溶液,现象是__________________理由____________________________________。
262.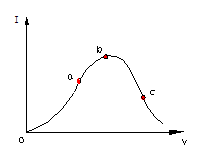 B在一定温度下,冰醋酸加水稀释过程中,溶液的导电能
B在一定温度下,冰醋酸加水稀释过程中,溶液的导电能
力I随加入水的体积V变化的曲线如右图所示。请回答:
⑴“O”点导电能力为O的理由是__________________________;
⑵a,b,c三点溶液中c(H+)由小到大的顺序为_________________;
⑶a,b,c三点中醋酸电离度最大的是________________________;
⑷若使C点溶液的c(CH3COO-)提高,在如下措施中可采取(填标号)
A.加盐酸 B.加浓醋酸 C.加入固体KOH D.加水 E.加固体CH3COONa F.加Zn粒
261. A请用电离平衡移动原理解释为何Al (OH)3既能溶于强酸,又能溶于强碱?
260. B设计一个实验,证明CH3COOH是弱电解质,盐酸为强电解质?
259. B试用简单的实验证明,在醋酸溶液中存在着CH3COOH CH3COO-+H+的电离平衡(要求写出简要操作,现象及实验能说明的问题)。
CH3COO-+H+的电离平衡(要求写出简要操作,现象及实验能说明的问题)。
258. AH2S溶液中存在着H2S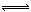 H+ +HS-,HS-
H+ +HS-,HS-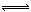 H+ +S2-的平衡
H+ +S2-的平衡
(1)当向H2S溶液中加入CuSO4溶液时,电离平衡向__________移动,c(S2-)______(填“增大”、“减小”或“不变”),c(H+)______(填“增大”、“减小”或“不变”)
(2)当向H2S溶液中加入少量NaOH固体时,电离平衡向__________移动,c(S2-)______(填“增大”、“减小”或“不变”),c(H+)______(填“增大”、“减小”或“不变”)
(3)当向H2S溶液中加入少量Na2S固体时,电离平衡向__________移动,c(S2-)______(填“增大”、“减小”或“不变”),c(H+)______(填“增大”、“减小”或“不变”)
(4)若将H2S溶液加热至沸,c(H2S)__________(填“增大”、“减小”或“不变”);若要增大H2S溶液中c(S2-),最好加入______________
257. ApH值相等且等体积的醋酸和盐酸与足量的Zn反应,产生H2起始速率醋酸 盐酸,放出的H2醋酸 盐酸(填>,<或=);物质的量浓度相等,且等体积的醋酸和盐酸与足量的Zn反应,产生H2起始速率醋酸 盐酸,放出的H2醋酸 盐酸。
256. A常温下将氯气通入水中得到新制的氯水,发生的化学方程式为 ______________________________,若其中Cl - 浓度为a mol/L ,ClO- 浓度为bmol/L,则a与b的关系为a___b,理由是____________________________________________________。
255.B氯化铜的稀溶液是淡蓝色的,可是加入浓盐酸后,溶液变成黄绿色了,这种颜色变化是由下列可逆反应造成的:Cu(H2O)42+(溶液)+4Cl-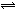 CuCl42-(溶液)+4H2O其中Cu(H2O)42+为淡蓝色,CuCl42-为黄绿色。下列哪种方法能使溶液变成淡蓝色:
①加蒸馏水,②加AgNO3溶液,③加入NaCl溶液,④加入NaOH溶液。
CuCl42-(溶液)+4H2O其中Cu(H2O)42+为淡蓝色,CuCl42-为黄绿色。下列哪种方法能使溶液变成淡蓝色:
①加蒸馏水,②加AgNO3溶液,③加入NaCl溶液,④加入NaOH溶液。
A.只有① B.只有② C.①和② D.③和④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com