
15.室温下,等体积、等物质的量浓度的下列溶液:①NaNO3 ②AlCl3 ③HF ④K2SO4的溶液中,所含阳离子数由多到少的顺序是 ( )
A.④=①>②=③ B.④>①>②>③
C.④>②>①>③ D.④>②>③>①
14.下列离子方程式正确的是 ( )
A.在碳酸氢钙溶液中加入硝酸
Ca(HCO3)2+2H+=2CO2↑+2H2O+Ca2+
B.Na2S溶液呈碱性
S2-+2H2O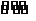 H2S↑+2OH-
H2S↑+2OH-
C.石灰石溶于盐酸
CaCO3+2H+=CO2↑+H2O+Ca2+
D.碳酸电离
H2CO3+H2O=H3O+十HCO3-
13.100mL1mol·L-1的盐酸和过量的铁粉反应,为了减缓反应速率且不影响生成H2的总量,可向反应物中加入
( )
A.KNO3溶液 B.KCl溶液
C.NaF固体 D.Na2CO3固体
12.下列关于铜一锌一稀硫酸原电池的有关叙述中,错误的是 ( )
A.锌为负极,锌发生氧化反应
B.铜为正极,铜不易失去电子而受保护
C.负极发生还原反应,正极发生氧化反应
D.外电路电子流入的极为负极,电子流出的极为正极
11.欲使硫化钠溶液中c(Na+)/c(S2-)减小,可向该溶液中加入:①NaOH(s) ②NaHS(s) ③KOH(s) ④KHS(s) ⑤Na2S(s) ⑥H2S ( )
A.③④⑤ B.⑥
C.①②⑤ D.③④
10.实验测得常温下0.1 mol·L-1某一元酸(HA)溶液中c(H+)/c(OH-)=1012,0.1 mol·L-1某一元碱(BOH)溶液的pH不等于13,将此两种溶液等体积混合后,所得溶液里各离子的物质的量浓度的关系正确的是 ( )
A.c(A-)>c(B+)>c(H+)>c(OH-)
B.c(B+)>c(A-)>c(OH-)>c(H+)
C.c(A-)=c(B+)>c(H+)=c(OH-)
D.c(A-)=0.1 mol·L-1
9.下列说法正确的是 ( )
A.强电解质溶液的导电能力不一定比弱电解质溶液强
B.0.1mol·L-1的HB溶液的pH为1,则HB一定是强酸
C.溶液的酸性越强,该溶液的pH越大
D.等温下,甲溶液的pH是乙溶液pH的2倍,则c(H+)甲=10-2c(H+)乙
8.在盛有饱和Na2CO3溶液的烧杯中插入惰性电极,保持温度不变,通电一段时间后 ( )
A.溶液的pH将增大
B.钠离子和碳酸根离子的比变小
C.溶液浓度不变,有晶体析出
D.溶液的浓度增大并有晶体析出
7.用普通食盐进行电解饱和食盐水的实验,食盐水装在U形管内。结果很快在某一电极附近出现食盐水浑浊现象。造成浑浊的难溶物主要是 ( )
A.碳酸镁 B.硫酸钡
C.氢氧化镁 D.碳酸钡
6.常温下将pH=9的Ba(OH)2溶液稀释为原体积的500倍所得溶液中:c(Ba2+)/c(OH-)约为 ( )
A.1/10 B.1/2
C.1/1 D.2/1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com