
19.用石墨电极在一定温度下电解K2SO4饱和溶液m g,当阴极
产生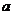 mol气体时,从溶液中析出
mol气体时,从溶液中析出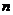 g无水晶体,则剩余溶液的
g无水晶体,则剩余溶液的
溶质质量分数是
A.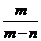 B.
B.
C.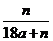 D.
D.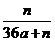
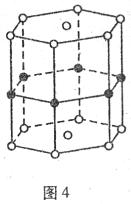
18.图4是硼和镁形成的化合物的晶体结构单元:镁
原子间形成正六棱柱,且棱柱的上下面还各有一
个镁原子;6个硼原子位于棱柱的侧棱上,则该化
合物的化学式可表示为
A.MgB B.Mg3B2
C.Mg2B D.Mg2B3
17. Cu2O是一种半导体材料,基于绿色化学理念设
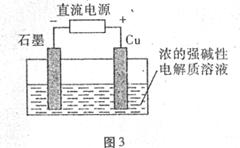
Cu2O是一种半导体材料,基于绿色化学理念设
计的制取Cu2O的电解池示意图如图3所示,电
解总反应为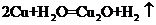 。下列说
。下列说
法正确的是
A.石墨电极上产生氢气
B.铜电极发生还原反应
C.铜电极接直流电源的负极
 D.当有0.1mol电子转移时,有0.1mol Cu2O生成
D.当有0.1mol电子转移时,有0.1mol Cu2O生成
16.重金属离子有毒性。实验室有甲、乙两种废液,均有一定毒性。甲废液经化验呈碱性,主要有毒离子为Ba2+离子,如将甲、乙废液按一定比例混合,毒性明显降低。则乙废液中可能含有的离子是
A.Cu2+和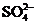 B.Cu2+和
B.Cu2+和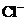
C.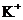 和
和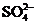 D.Ag+和
D.Ag+和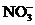
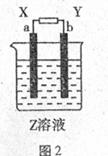
15.图2中X、Y分别是直流电源的两极,通电后,发现a极板质量增加.b极板处有无色无味气体放出,符合这一情况的是
|
|
a极板 |
b极板 |
X电极 |
Z溶液 |
|
A |
锌 |
石墨 |
负极 |
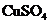 |
|
B |
石墨 |
石墨 |
负极 |
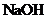 |
|
C |
银 |
铁 |
正极 |
 |
|
D |
铜 |
石墨 |
负极 |
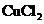 |
14.下列各组物质中,按熔点由低到高排列正确的是
A.O2、H2、Hg
B.CO2、KCl、SiO2
C.Na、K、Rb
D.SiC、NaCl、SO2
13.下列化学式表示的物质中,属于离子晶体,并且含
有非极性共价键的是
A.CaCl2
B.Na2O2
C.N2
D.NH4Cl
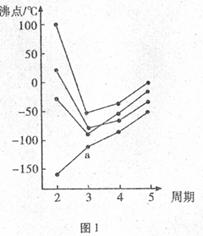
12.图1中每条折线表示周期表IVA-VIIA中的某一族
元素氢化物的沸点变化,每个小黑点代表一种氢化
物,其中a点代表的是
A.H2S
B.HCl
C.PH3
D.SiH4
11.下列反应能用勒夏特列原理解释的是
A.用二氧化硫和氧气反应生成三氧化硫需使用催化剂
 B.燃烧粉碎的磺铁矿更有利于二氧化硫的生成
B.燃烧粉碎的磺铁矿更有利于二氧化硫的生成
C.硫酸生产中用98%的浓硫酸吸收三氧化硫
D.用乙烯和水蒸气反应生成乙醇需采用高温操作
10.下列关于Fe(OH)3胶体的说法不正确的是
 A.Fe(OH)3胶体与硅酸溶胶混合,将产生凝聚现象
A.Fe(OH)3胶体与硅酸溶胶混合,将产生凝聚现象
 B.Fe(OH)3胶体粒子在电场作用下将向阳极运动
B.Fe(OH)3胶体粒子在电场作用下将向阳极运动
 C.Fe(OH)3胶体粒子不停地做布朗运动
C.Fe(OH)3胶体粒子不停地做布朗运动
D.光线通过Fe(OH)3溶胶时会产生丁达尔现象
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com