
26. (1)H2O (2)2Na2S
(1)H2O (2)2Na2S
(3)2Al(OH)3 Al2O3+3H2O
(4)2H2S+SO2=3S+2H2O
讲析:24.溶液呈碱性,Ag+、Fe3+不能存在,但溶液中必须有阳离子(K+)。
25.Al2O3、Al(OH)3、AlCl3、NaAlO2;
4AlCl3+6Na2O2+6H2O=4Al(OH)3↓+12NaCl+3O2↑
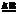 ②2Na+O2 Na2O2
②2Na+O2 Na2O2
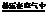 ③4Na+O2
2Na2O
③4Na+O2
2Na2O
(2)0;-1;-2
(3)4KO2+2CO2=2K2CO3+O2↑ (4)2,2,1,1,2OH-
23.①铝的燃烧热值高 ②铝矿资源丰富 ③质轻,便于贮存和运输、安全性好 ④燃烧过程中不会有SO2等有害气体的排放 ⑤生成的Al2O3可冶炼回收利用。
0.5mol/L·xL n(H2SO4)
n(H2SO4)=0.25xmol
20.沉淀最大时,溶液中只有溶质Na2SO4,则有:
2NaOH--H2SO4
2 1
19.混合物放入水中,发生的反应为2Na+2H2O=2NaOH+H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,当有沉淀时必为Al,则Al过量,溶液中只有NaAlO2.
15.设Mg的质量为m,铜铝合金中铝为x,则铜为m-x。
Mg+H2SO4=MgSO4+H2↑ Δm
24 2 22
m
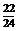 m
m
2Al+3H2SO4=Al2(SO4)3+3H2↑ Δm
54 6 48
x
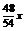
由题意有:(m-x)+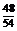 x=
x=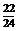 m
m
x=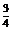 m 即铝为
m 即铝为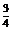 m,则Cu为
m,则Cu为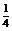 m。
m。
14.FeS+2Fe(OH)3+3H2SO4=S↓+3FeSO4+6H2O
88 2×107 32
m(FeS) m[Fe(OH)3] 1.6g
m(FeS)=4.4g m[Fe(OH)3]=10.7g
由此当Fe(OH)3过量时,FeS为4.4g,
当FeS过量时FeS为:28.3g-10.7g=17.6g。
10.Mg的物质的量相同的情况下,分别生成等物质的量的MgO和MgO及C;而Mg3N2的物质的量只有它们的1/3。
16.B 17.C 18.AD 19.C 20.C
讲析:9.溶液呈酸性,NO3-在酸性条件下能氧化Fe2+。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com