
|
三阶段 |
1.造气 |
2.接触氧化 |
3.SO3的吸收 |
|
三设备 |
|
|
|
|
三反应 |
|
|
|
尾气的吸收:通常工业上是用氨水来吸收SO2,其反应式为:
3. 浓硫酸的三大特性
A. 吸水性:将物质中含有的水分子夺去。 “水”可以是混合气体中的 ,也可以是结晶水合物中的 。用作干燥剂, 但不可干燥 等气体。
B. 脱水性:浓硫酸按 的组成比,夺取某些有机物质中的H、O元素形成
 可使有机物碳化。所以浓硫酸对有机物有强烈的 作用。
可使有机物碳化。所以浓硫酸对有机物有强烈的 作用。
C. 强氧化性:
a. 常温下,浓硫酸或浓硝酸使 等金属 。
|
|
c. 与非金属反应: C+2H2SO4(浓)====
d. 能与其他还原性物质反应 如H2S、HI、FeO等
2. 稀硫酸是 酸,电离方程式为:
1. 硫酸的物理性质:纯硫酸是 色 状的液体,沸点 ,密度 ,能与水以任意比互溶,由于溶解时 ,所以稀释浓硫酸时,一定要将 慢慢地注入 中,并不断的搅拌。
正常的雨水由于溶解CO2形成弱酸H2CO3,pH约为 。
空气中硫的氧化物和氮的氧化物随雨水降下就成为酸雨,酸雨的pH 。二氧化硫的来源:
硫酸型酸雨两条形成途径:(用反应方程式表示)
途径1:
途径2:
2.化学性质: 二氧化硫是一种酸性氧化物,溶于水生成 它的水溶液呈 。
(1)、SO2是酸性氧化物: a.与水反应:
(H2SO3不稳定,且容易被氧化生成硫酸: )
b.与碱反应:与NaOH溶液反应:
使澄清的石灰水变浑浊:
将SO2持续通入澄清石灰水中,现象如何?
(2)、SO2中S元素处于中间价态即 价,既有 性又有 性(以 性为主)
 a.弱氧化性:与硫化氢反应:
a.弱氧化性:与硫化氢反应:
b.较强还原性:可被多种氧化剂(如O2、Cl2、Br2、I2、HNO3、KMnO4、H2O2)氧化。
SO2与O2反应:
SO2使氯水(溴水、碘水)褪色:
SO2被双氧水氧化::
(3)、SO2的漂白性: SO2跟某些有色物质(如品红等)反应生成 ,此无色物质见光、遇热或长久放置又容易 ,又会恢复到原来的颜色。SO2 能漂白酸碱指示剂,如SO2只能使紫色石蕊试液变 ,不能使它 。
HClO、过氧化氢等的漂白原理:是利用他们的 性质。他们的漂白效果是 性的,不可逆的。氯气能使紫色石蕊试液变 ,继续通入又能使之 。
若将等物质的量的氯气和二氧化硫同时通入品红溶液中,品红溶液红色 。
1.物理性质:二氧化硫是一种 色有 气味的 毒气体,易液化;密度比空气 , 溶于水,常温、常压下1体积水约能溶解 体积的二氧化硫。
23.(5分)某氯碱化工厂以电解食盐水产生化工原料氢氧化钠(反应原理为:
2NaCl+2H2O 2NaOH+H2
2NaOH+H2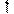 +Cl2
+Cl2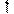 )。若电解含氯化钠23.4t的食盐水,理论上可得到多少氢氧化钠?
)。若电解含氯化钠23.4t的食盐水,理论上可得到多少氢氧化钠?
22.(4分)2010年4月14日,青海省玉树县发生大地震,某护士为在帐篷里的一位病人滴注500mL的生理盐水(NaCl的质量分数为0.9%,溶液的密度约为1g/mL)。
计算500mL的生理盐水中NaCl的质量为 g,水的质量为 g。
21.(18分)实验盒中有5种没有标签的溶液,老师让实验小组同学鉴别这些溶液。
[调查研究]
①实验盒中记录单上登记的5种溶液是:Na2CO3、CuSO4、Ca(OH)2、NaOH和稀盐酸,
其中有颜色的是 溶液;
②查阅资料:无色有刺激性气味的氯化氢气体溶于水得到盐酸;
③研究方式:从4种无色溶液中任意取出3种为一组进行鉴别。
[提出假设] 同学们从4种无色溶液中取出3种,贴上A、B、C标签,并且假设这一组溶液可能是Na2CO3、Ca(OH)2和NaOH。
[实验探究] 同学们按以下步骤进行鉴别:
|
溶液 |
A |
B |
C |
|
加入盐酸后的现象 |
无明显变化 |
无明显变化 |
有气泡产生 |
第一步 取3支试管,分别加入少量的A、B、C溶液,然后依次加入少量盐酸,实验现象记录如下:
实验结论:C是 溶液。
第二步 依据如图装置进行实验,其中夹持固定装置已略去。从长颈漏斗加入盐酸,可以观察到C溶液中气泡产生,A溶液中有白色沉淀生成,B溶液无明显变化。
实验解释:
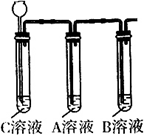 ①A溶液中产生的白色沉淀是
(写出化学式),
①A溶液中产生的白色沉淀是
(写出化学式),
则A是 溶液。
②写出C溶液中发生反应的化学方程式 。
第三步 取少量B溶液倒入蒸发皿,加热,闻到有刺激性气味,
停止加热。
实验结论:B是 溶液。
经过上述三步实验,同学们认为最后一种溶液是 溶液。
[实验反思]老师提出:鉴别出C溶液后,不需外加试剂,就可以简便地鉴别出A、B溶液。请完成下列实验报告
|
实验步骤 |
实验现象 |
结论 |
|
取A、B两溶液分别于两支试管中,各滴加C溶液 |
|
该溶液是A 溶液 |
|
|
该溶液是B溶液 |
|
|
|
|
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com