
381. B 某待测液中可能含有Fe2+、Fe3+、Ag+、Al3+、Ba2+、Ca2+、NH4+等离子,进行了下述实验(所加酸、碱、氨水、溴水都是过量的)
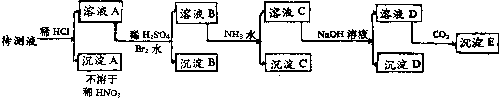
根据实验结果:
(1)判定待测液中有无Ba2+、Ca2+离子,并写出理由.答: .
(2)写出沉淀D的分子式: .
(3)写出从溶液D生成沉淀E的反应的离子方程式: .
380. B A、B、C和D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种.现利用另一种溶液X,用如下图所示的方法,即可将它们一一确定.试确定A、B、C、D、X各代表何种溶液.
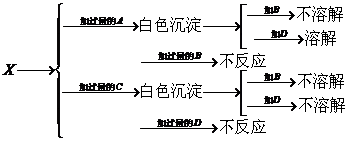
A: B: C: D: X:
379. B已知:AgCl+Br-=AgBr↓+Cl-,2AgI+S2-=Ag2S↓+2I-,AgBr+I-=AgI↓+Br-.由以上实验事实可知4种难溶银盐溶解度减小的顺序是 。
378. B已知在pH为4-5的环境中,Cu2+、Fe2+几乎不水解,而Fe3+几乎完全水解。工业上制CuCl2是将浓盐酸用蒸气加热到80℃左右,再慢慢加入粗氧化铜(含少量杂质FeO),充分搅拌使之溶解。欲除去溶液中的杂质离子,下述方法中可行的是 ( )
A 加入纯Cu将Fe2+还原为Fe
B 向溶液中通入H2S使Fe2+沉淀
C 向溶液中通入Cl2,再通入NH3,调节pH值为4-5
D 向溶液中通入Cl2,再加入纯净的CuO粉末调节pH值为4-5
377. B已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1) CuSO4 +Na2CO3 主要:Cu2+ + CO32─ + H2O == Cu(OH)2↓+ CO2↑
次要:Cu2+ + CO32─== CuCO3↓
(2) CuSO4 +Na2S 主要:Cu2+ + S2─== CuS↓
次要:Cu2+ + S2─+ 2H2O == Cu(OH)2↓+ H2S↑
下列几种物质的溶解度大小的比较中,正确的是 ( )
A、CuS <Cu(OH)2<CuCO3 B、CuS >Cu(OH)2>CuCO3
C、Cu(OH)2>CuCO3>CuS D、Cu(OH)2<CuCO3<CuS
376. B为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤,②加过量NaOH溶液,③加适量盐酸,④加过量Na2CO3溶液,⑤加过量BaCl2溶液.正确的操作顺 ( )
A.①④②⑤③ B.④①②⑤③
C.②⑤④①③ D.⑤②④①③
375. B BaSO4水液用于肠胃系统放射照片的拍摄。在3L BaSO4(Ksp=7.1´10-10)饱和溶液中,溶解的Ba2+离子的质量是 ( )
A、5.0 mg B、3.7 mg C、3.0 mg D、11.0 mg
374. B把a g铁铝合金粉末溶于足量盐酸中,加入过量NaOH溶液。过滤出沉淀,经洗涤、干燥、灼烧,得到红棕色粉末的质量仍为a g,则原合金中铁的质量分数为 ( )
A.70% B.52.4% C.47.6% D.30%
373. B某溶液中含三种离子,加入过量氨水有沉淀生成 ,过滤后滤液中加过量盐酸,又有沉淀生成,再过滤,滤液中加入过量Na2CO3溶液,仍有沉淀生成,原溶液中含有的离子可能是 ( )
A.Ag+、Fe2+、Ca2+ B. Al3+、Mg2+、Ba2+
C. Ca2+、Fe2+、Ba2+ D.Ag+、Mg2+、Ba2+
372. A 为了除去MgCl2酸性溶性中的Fe3+,可在加热搅拌的条件下加入一种试剂,过滤后再加入适量盐酸.这种试剂是 ( )
A.NH3·H2O B.NaOH C.Na2CO3 D.MgCO3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com