
27.(1)ЗжзгЁЁ ИЩБљЁЁ
(2)е§ЫФУцЬхЁЁ ЗЧМЋадЁЁ Si3N4ЁЁЁЁ
(3)Ш§НЧзЖаЮЁЁЁЁ 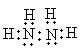 ЁЁЁЁЁЁ
ЁЁЁЁЁЁ
(4)CS2ЁЁЁЁ CCl4ЁЁ ЁЁ(2Зж)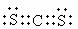 ЁЁ
ЗЧМЋадЁЁЁЁ
ЁЁ
ЗЧМЋадЁЁЁЁ
26.
(1)CaC2ЁЁ CaOЁЁ CO2ЁЁ Ca(OH)2ЁЁ C2H2
(2)Ca(OH)2+2CO2=Ca(HCO3)2ЁЁ (3)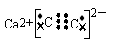

32. (07ФъИпПМРэзлжиЧьОэЁЄ29) (14Зж)aЁЂbЁЂcЁЂdЁЂeЪЧЖЬжмЦкдЊЫиЃЌжмЦкБэжаaгыbЁЂbгыcЯрСкЃЛaгыeЕФзюЭтВуЕчзгЪ§жЎБШЮЊ2:3ЃЌbЕФзюЭтВуЕчзгЪ§БШeЕФзюЭтВуЕчзгЪ§Щй1ИіЃЛГЃМћЛЏКЯЮяd2c2гыЫЎЗДгІЩњГЩcЕФЕЅжЪЃЌЧвШмвКЪЙЗгЬЊЪдвКБфКьЁЃ
(1)eЕФдЊЫиЗћКХЪЧ__________ЁЃ
(2)aЁЂbЁЂcЕФЧтЛЏЮяЮШЖЈадЫГађЮЊ(гУЗжзгЪНБэЪО)__________________ЃЛbЕФЧтЛЏЮяКЭbЕФзюИпМлбѕЛЏЮяЕФЫЎЛЏЮяЗДгІЩњГЩZЃЌдђZжаЕФЛЏбЇМќРраЭЮЊ__________________ЃЌZЕФОЇЬхРраЭЮЊ_____________ЃЛabЃРызгЕФЕчзгЪНЮЊ____________ЁЃ
(3)гЩaЁЂcЁЂdаЮГЩЛЏКЯЮяЕФЫЎШмвКЯдМюадЃЌЦфдвђЪЧ(гУРызгЗНГЬЪНБэЪО)_______________ЁЃ
(4)вЛЖЈСПЕФd2c2гыac2ЗДгІКѓЕФЙЬЬхЮяжЪЃЌЧЁКУгы0.8 molЯЁбЮЫсШмвКЭъШЋЗДгІЃЌВЂЪеМЏЕН0.25 molЦјЬхЃЌдђгУЮяжЪЕФСПБэЪОИУЙЬЬхЮяжЪЕФзщГЩЮЊ__________________ЁЂ___________________ЁЃ
ЂђОэЗЧбЁдёЬтД№АИЃК
31. (07ФъИпПМРэзлЬьНђОэЁЄ26)UЁЂVЁЂWЁЂXЁЂYЁЂZЪЧдзгађЪ§вРДЮдіДѓЕФСљжжГЃМћдЊЫиЁЃYЕФЕЅжЪдкW2жаШМЩеЕФВњЮяПЩЪЙЦЗКьШмвКЭЪЩЋЁЃZКЭWдЊЫиаЮГЩЕФЛЏКЯЮяZ3W4ОпгаДХадЁЃUЕФЕЅжЪдкW2жаШМЩеПЩЩњГЩUWКЭUW2СНжжЦјЬхЁЃXЕФЕЅжЪЪЧвЛжжН№ЪєЃЌИУН№ЪєдкUW2жаОчСвШМЩеЩњГЩКкЁЂАзСНжжЙЬЬхЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
(1)VЕФЕЅжЪЗжзгЕФНсЙЙЪНЮЊ______________ЃЛXWЕФЕчзгЪНЮЊ__________________ЃЛZдЊЫидкжмЦкБэжаЕФЮЛжУЪЧ_________ЁЃ
(2)UдЊЫиаЮГЩЕФЭЌЫивьаЮЬхЕФОЇЬхРраЭПЩФмЪЧ(ЬюађКХ)________________ЁЃ
ЂйдзгОЇЬхЁЁЁЁ ЂкРызгОЇЬхЁЁЁЁ ЂлЗжзгОЇЬхЁЁЁЁ ЂмН№ЪєОЇЬх
(3)UЁЂVЁЂWаЮГЩЕФ10ЕчзгЧтЛЏЮяжаЃЌUЁЂVЕФЧтЛЏЮяЗаЕуНЯЕЭЕФЪЧ(аДЛЏбЇЪН)__________ЃЛVЁЂWЕФЧтЛЏЮяЗжзгНсКЯH+ФмСІНЯЧПЕФЪЧ(аДЛЏбЇЪН)__________ЃЌгУвЛИіРызгЗНГЬЪНМгвджЄУї___________________________________ЁЃ
(4)YW2ЦјЬхЭЈШыBaCl2КЭHNO3ЕФЛьКЯШмвКЃЌЩњГЩАзЩЋГСЕэКЭЮоЩЋЦјЬхVWЃЌгаЙиЗДгІЕФРызгЗНГЬЪНЮЊ__________________ЁЃ
гЩДЫПЩжЊVWКЭYW2ЛЙдадНЯЧПЕФЪЧ(аДЛЏбЇЪН)____________ЁЃ
30. (08ФъЩЯКЃЛЏбЇЁЄ23BгаЩОМѕ)дЊЫиA-DЪЧдЊЫижмЦкБэжаЖЬжмЦкЕФЫФжждЊЫиЃЌЧыИљОнБэжааХЯЂЛиД№ЯТСаЮЪЬтЁЃ
|
дЊЫи |
A |
B |
C |
D |
|
аджЪЛђНсЙЙаХЯЂ |
ЕЅжЪжЦГЩЕФИпбЙЕЦЃЌЗЂГіЕФЛЦЙтЭИЮэСІЧПЁЂЩфГЬдЖЁЃ |
ЙЄвЕЩЯЭЈЙ§ЗжРывКЬЌПеЦјЛёЕУЦфЕЅжЪЁЃдзгЕФзюЭтВуЮДДяЕНЮШЖЈНсЙЙЁЃ |
ЕЅжЪГЃЮТЁЂГЃбЙЯТЪЧЦјЬхЃЌдзгЕФLВугавЛИіЮДГЩЖдЕФpЕчзгЁЃ |
+2МлбєРызгЕФКЫЭтЕчзгХХВМгыФЪдзгЯрЭЌЁЃ |
(1)ЩЯБэжагыAЪєгкЭЌвЛжмЦкЕФдЊЫиЪЧЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)DКЭCаЮГЩЕФЛЏКЯЮяЪєгкЁЁЁЁЁЁЁЁ ОЇЬхЁЃаДГіCЕЅжЪгыЫЎЗДгІЕФЛЏбЇЗНГЬЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
(3)ЖддЊЫиBЕФЕЅжЪЛђЛЏКЯЮяУшЪіе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁ ЁЃ
aЃЎЁЁ BдЊЫиЕФзюИпе§МлЮЊ+6
bЃЎЁЁ ГЃЮТЁЂГЃбЙЯТЕЅжЪФбШмгкЫЎ
cЃЎЁЁ ЕЅжЪЗжзгжаКЌга18ИіЕчзг
dЃЎЁЁ дквЛЖЈЬѕМўЯТУОЬѕФмгыЕЅжЪBЗДгІ
(4)AКЭDСПдЊЫиН№ЪєадНЯЧПЕФЪЧ(аДдЊЫиЗћКХ)ЁЁЁЁЁЁЁЁ ЁЃаДГіФмжЄУїИУНсТлЕФвЛИіЪЕбщЪТЪЕЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
29. (08ФъЩЯКЃЛЏбЇЁЄ23AгаЩОМѕ)ЫФжжЖЬжмЦкдЊЫиЕФаджЪЛђНсЙЙаХЯЂШчЯТБэЁЃЧтИљОнаХЯЂЛиД№ЯТСаЮЪЬтЁЃ
|
дЊЫи |
A |
B |
C |
D |
|
аджЪЛђНсЙЙаХЯЂ |
ЪвЮТЯТЕЅжЪГЪЗлФЉзДЙЬЬхЃЌМгШШвзШлЛЏЁЃЕЅжЪдкПеЦјжаШМЩеЃЌЗЂГіУїССЕФРЖзЯЩЋЛ№бцЁЃ |
ЕЅжЪГЃЮТЁЂГЃбЙЯТЪЧЦјЬхЃЌФмШмгкЫЎЁЃдзгЕФMВуга1ИіЮДГЩЖдЕФpЕчзгЁЃ |
ЕЅжЪжЪШэЁЂвјАзЩЋЙЬЬхЁЂЕМЕчадЧПЁЃЕЅжЪдкПеЦјжаШМЩеЗЂГіЛЦЩЋЕФЛ№бцЁЃ |
дзгзюЭтВуЕчзгВуЩЯsЕчзгЪ§ЕШгкpЕчзгЪ§ЁЃЕЅжЪЮЊПеМфЭјзДОЇЬхЃЌОпгаКмИпЕФШлЁЂЗаЕуЁЃ |
(1)BдЊЫидкжмЦкБэжаЕФЮЛжУЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌ
(2)аДГіCЕЅжЪгыЫЎЗДгІЕФЛЏбЇЗНГЬЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
AгыCаЮГЩЕФЛЏКЯЮяШмгкЫЎКѓЃЌШмвКЕФpHЁЁЁЁЁЁЁЁ 7(ЬюЁАДѓгкЁБЁЂЁАЕШгкЁБЛђЁАаЁгкЁБ)ЁЃ
(3)DдЊЫизюИпМлбѕЛЏЮяОЇЬхЕФгВЖШЁЁЁЁЁЁ (ЬюЁАДѓЁБЁЂЁАаЁЁБ)ЃЌЦфРэгЩЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(4)AЁЂBСНдЊЫиЗЧН№ЪєадНЯЧПЕФЪЧ(аДдЊЫиЗћКХ)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃаДГіжЄУїетвЛНсТлЕФвЛИіЪЕбщЪТЪЕЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
28. (08ФъФўЯФРэзлЁЄ35гаЩОМѕ)
XЁЂYЁЂZЁЂQЁЂEЮхжждЊЫижаЃЌXдзгКЫЭтЕФMВужажЛгаСНЖдГЩЖдЕчзгЃЌYдзгКЫЭтЕФLВуЕчзгЪ§ЪЧKВуЕФСНБЖЃЌZЪЧЕиПЧФкКЌСП(жЪСПЗжЪ§)зюИпЕФдЊЫиЃЌQЕФКЫЕчКЩЪ§ЪЧXгыZЕФКЫЕчКЩЪ§жЎКЭЃЌEдкдЊЫижмЦкБэЕФИїдЊЫижаЕчИКадзюДѓЁЃЧыЛиД№ЯТСаЮЪЬтЃК
(1)XЁЂYЕФдЊЫиЗћКХвРДЮЮЊЁЁЁЁЁЁЁЁЁЁ ЁЂЁЁЁЁ ЁЁЁЁЁЁЃЛ
(2)XZ2гыYZ2ЗжзгЕФСЂЬхНсЙЙЗжБ№ЪЧЁЁЁЁЁЁЁЁЁЁ КЭЁЁЁЁЁЁЁЁЁЁ ЃЌЯрЭЌЬѕМўЯТСНепдкЫЎжаЕФШмНтЖШНЯДѓЕФЪЧЁЁЁЁЁЁЁЁЁЁ (аДЗжзгЪН)ЃЌРэгЩЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
(3)QЕФдЊЫиЗћКХЪЧЁЁЁЁЁЁЁЁ ЃЌЫќЪєгкЕкЁЁЁЁЁЁ жмЦкЃЌдкаЮГЩЛЏКЯЮяЪБЫќЕФзюИпЛЏКЯМлЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
(4)гУЧтМќБэЪОЪНаДГіEЕФЧтЛЏЮяШмвКжаДцдкЕФЫљгаЧтМќЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
27. (08ФъШЋЙњРэзлIIЁЄ27)QЁЂRЁЂXЁЂYЁЂZ ЮЊЧА20КХдЊЫижаЕФЮхжжЃЌQЕФЕЭМлбѕЛЏЮягыXЕЅжЪЗжзгЕФЕчзгзмЪ§ЯрЕШЃЌRгыQЭЌзхЃЌYКЭZЕФРызггыArдзгЕФЕчзгНсЙЙЯрЭЌЧвYЕФдзгађЪ§аЁгк20
(1)QЕФзюИпМлбѕЛЏЮяЃЌЦфЙЬЬЌЪєгк___________ОЇЬхЃЌЫзУћНа________________ЁЃ
(2)RЕФЧтЛЏЮяЗжзгЕФПеМфЙЙаЭЪЧ_______________ЃЌЪєгк_____________Зжзг(ЬюЁАМЋадЁБЛђЁАЗЧМЋадЁБ)ЃЛЫќгыXаЮГЩЕФЛЏКЯЮяПЩзїЮЊвЛжжживЊЕФЬеДЩВФСЯЃЌЦфЛЏбЇЪНЪЧЃЛ____________________________ЁЃ
(3)XЕФГЃМћЧтЛЏЮяЕФПеМфЙЙаЭЪЧ__________________ЃЛЫќЕФСэвЛЧтЛЏЮяX2H4ЪЧвЛжжЛ№М§ШМСЯЕФГЩЗжЃЌЦфЕчзгЪНЪЧ_________________ЁЃ
(4)QЗжБ№гыYЁЂZаЮГЩЕФЙВМлЛЏКЯЮяЕФЛЏбЇЪНЪЧ_________КЭ__________ЃЛQгыYаЮГЩЕФЗжзгЕФЕчзгЪНЪЧ______________ЃЌЪєгк__________Зжзг(ЬюЁАМЋадЁБЛђЁАЗЧМЋадЁБ)ЁЃ
26. (08ФъШЋЙњРэзлIЁЄ27)VЁЂWЁЂXЁЂYЁЂZ ЪЧгЩжмЦкБэ1-20КХВПЗждЊЫизщГЩЕФ5жжЛЏКЯЮяЃЌЦфжаVЁЂWЁЂXЁЂZОљЮЊСНжждЊЫизщГЩЁЃЩЯЪі5жжЛЏКЯЮяЩцМАЕФЫљгадЊЫиЕФдзгађЪ§жЎКЭЕШгк35ЫќУЧжЎМфЕФЗДгІЙиЯЕШчЯТЭМЃК
 ЁЁ
ЁЁ
ЁЁ (1)5 жжЛЏКЯЮяЗжБ№ЪЧ VЁЁЁЁЁЁ ЁЂWЁЁЁЁ ЁЂ XЁЁЁЁЁЁ ЁЂYЁЁЁЁЁЁ ЁЂZЁЁЁЁЁЁ ЃЛ(ЬюЛЏбЇЪН)
(2)гЩЩЯЪіЮхжжЛЏКЯЮяжаЕФФГ 2 жжЛЏКЯЮяЗДгІПЩЩњГЩвЛжжаТЛЏКЯЮяЃЌЫќАќКЌСЫ 5 жжЛЏКЯЮяЕФЫљгадЊЫиЃЌЩњГЩИУЛЏКЯЮяЕФЛЏбЇЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)VЕФЕчзгЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
25ЃЎ(07ФъИпПМРэзлЬьНђОэЁЄ9)ЯТСаЙигкСЃзгНсЙЙЕФУшЪіВЛе§ШЗЕФЪЧC
AЃЎH2SКЭNH3ОљЪЧМлЕчзгзмЪ§ЮЊ8ЕФМЋадЗжзг
BЃЎHSЃКЭHClОљЪЧКЌвЛИіМЋадМќЕФ18ЕчзгСЃзг
CЃЎCH2Cl2КЭCCl4ОљЪЧЫФУцЬхЙЙаЭЕФЗЧМЋадЗжзг
DЃЎ1 mol D216OжаКЌжазгЁЂжЪзгЁЂЕчзгИї10NA(NAДњБэАЂЗќМгЕТТоГЃЪ§ЕФжЕ)
ЂђОэЗЧбЁдёЬт
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com