
1.(广东省中山一中2009届高三第二次统测化学试题)(14分)黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。
⑴冶炼铜的反应为
8CuFeS2+21O2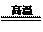 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)。
⑵上述冶炼过程产生大量SO2。下列处理方案中合理的是 (填代号)。
a.高空排放
b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO4
d.用浓硫酸吸收
⑶过二硫酸钾(K2S2O8)具有强氧化性,可将I-氧化为I2:
S2O82-+2I-=2SO42-+I2
通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe3+对上述反应催化的过程。
、 (不必配平)
⑷利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
a.除去Al3+的离子方程式是 。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为 。
证明炉渣中含有FeO的实验现象为
。
答案⑴Cu、O;⑵b、c;⑶2Fe3++2I-=2Fe2++I2;S2O82-+2Fe2+=2SO42-+2Fe3+;(离子方程式不配平不扣分)⑷a:2Al3++4OH-=AlO2-+2H2O[或Al3++4OH-=Al(OH)4-];b:稀硫酸、KMnO4溶液;稀硫酸浸取炉渣所得溶液使KMnO4溶液褪色
2.外内:
(1)浓度:浓度越大,单位体积内活化分子数 ,有效碰撞的几率 ,发生化学反应的速率 ;因此,化学反应速率与浓度有密切的关系,浓度越大,化学反应速率越快。增大反应物的浓度,正反应速率加快。
(2)温度:温度越高,一方面活化分子百分数 ,另一方面含有较高能量的分子间的碰撞频率 ,两个方面都使分子间有效碰撞的几率 ,反应速率 (正逆反应速率都加快)。
(3)压强:对于有气体参与的化学反应,通过改变容器体积而使压强变化的情况(PV=nRT):压强增大,相当于浓度 ,反应速率 。(反应物和生成物的浓度都增大,正逆反应速率都增大,相反,亦然)。
(4)催化剂:使用正催化剂,反应所需的活化能 ,活化分子百分数 ,有效碰撞的几率 ,化学反应速率 (对于可逆的反应使用催化剂可以同等程度地改变正逆反应速率)。
试题枚举
[例1]已知:4NH3+5O2 4NO+6H2O,若反应速率分别用υ(NH3)、υ(O2)、υ(NO)、υ(H2O)
[mol·L-1·min-1]表示,则关系正确的是
4NO+6H2O,若反应速率分别用υ(NH3)、υ(O2)、υ(NO)、υ(H2O)
[mol·L-1·min-1]表示,则关系正确的是
A.4υ(NH3)=5υ(O2) B. 5υ(O2)=6υ(H2O)
C. 3υ(NH2)=2υ(H2O) D. 4υ(O2=5υ(NO)
解析:化学反应方程式的系数与分别用各物质表达的化学反应速率成正比。
答案:C、D
[变式]在2L密闭容器中,发生3A(气)+B(气)=2C(气)的反应,若最初加入A和B都是4mol,A的平均反应速率为0.12mol/L·s,则10秒钟后容器中B的物质的量为
A.2.8mol B.1.6mol C.3.2mol D.3.6mol
答案:C
[例2]某温度时,浓度都是1mol·L-1的两种气体,X2、Y2在密闭容器中反应生成气体Z,达到平衡时c(X2)=0.4mol·L-1、c(Y2)=0.8mol·L-1、c(Z)=0.4mol·L-1,则该反应的反应式是
A. X2+2Y2
 2XY2 B. 2X2+Y2
2XY2 B. 2X2+Y2  2X2Y
2X2Y
C. 3X2+Y2 2X3Y D. X2+3Y2
2X3Y D. X2+3Y2  2XY3
2XY3
解析:根据化学反应方程式的系数与分别用各物质表达的化学反应速率成正比的关系,只需分别计算同一时间内用各物质表达的化学反应速率,然后进行比较。
答案:C
[变式]A和B反应生成C,假定反应由A、B开始,它们的起始浓度均为1mol/L。反应进行2min后A的浓度为0.8mol/L,B的浓度为0.6mol/L,C的浓度为0.6mol/L。则2min内反应的平均速率υA=__________,υB=_____________,υC=___________。该反应的化学反应方程式为___________________________。
答案υA=0.1mol·L-1·min-1, υB=0.2mol·L-1·min-1, υC=0.3mol·L-1·min-1;
化学反应方程式为A+2B=3C。
[例3]在一定条件下,反应N2+3H2
 2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为
A. υ(H2)=0.03mol/(L·min) B. υ(N2)=0.02mol/(L·min)
C. υ(NH3)=0.17g/(L·min) D. υ(NH3)=0.01mol/(L·min)
解析:根据题目可知V(NH3)=0.01mol/(L·min),根据反应系数与化学反应速率的关系可求出V(H2)=0.015mol/(L·min)
答案:D
[变式]4NH3+5O2
 4NO+6H2O反应在5L的密闭容器中进行,半分钟后,NO物质的量增加了0.3mol,则此反应的反应速率为
4NO+6H2O反应在5L的密闭容器中进行,半分钟后,NO物质的量增加了0.3mol,则此反应的反应速率为
A.υ(O2)=0.01mol/L·s B.υ(NO)=0.008mol/L·s
C.υ(H2O)=0.003mol/L·s D.υ(NH3)=0.002mol/L·s
答案:CD
[变式]把0.6molX气体和0.4molY气体混合2L于容器中使它们发生如下反应,3X(气)+Y(气) nZ(气)+2W(气),5min末已生成0.2mol W,若测知以Z浓度变化来表示的反应平均速率为0.01mol/L·min,则
(1)上述反应中Z气体的反应方程式系数n的值是
A.1 B.2 C.3 D.4
(2)上述反应在5分钟末时,已消耗的Y值占原来的分数是
A.20% B.25% C.33% D.50%
答案:(1)A (2)B
[例4]下列体系加压后,对化学反应速率没有影响的是
A.2SO2+O2
 2SO3 B.CO+H2O(气)
2SO3 B.CO+H2O(气)  CO2+H2
CO2+H2
C.CO2+H2
 H2CO3 D.OH-+H+=H2O
H2CO3 D.OH-+H+=H2O
解析:压强对没有气体参加的反应无影响。
答案:D
[例5]把镁带投入盛有盐酸的敞口容器里,在下列因素中:①盐酸的浓度,②镁带的表面积,③溶液的温度,④氯离子的浓度。对反应速率有影响的是
A.①② B.③④ C.①②③④ D.①②③
解析:根据影响反应速率的因素有:浓度、温度、压强和催化剂可知,①③肯定对反应速率有影响,而镁带的表面积越大则与盐酸的接触越充分,显然反应速率越快。此反应的实质是Mg+2H+=Mg2++H2↑,与氯离子浓度无关,所以④对此反应速率无影响。故本题的正确答案为D。
答案:D
1.内因: (如:钠与水反应和钾与水反应速率明显不同)。
3.相互关系:
4NH3+5O2 4NO+6H2O(g)
4NO+6H2O(g)
υ(NH3)∶υ(O2)∶υ(NO)∶υ(H2O)=4∶5∶4∶6
2.单位:mol/(L·s);mol/(L·min);mol/L·S。
用单位时间里反应物浓度的减少或生成物浓度的增加来表示。
1.表示方法:υ=△c/△t
16.B 解析:利用HCl易溶于水,而有机物一般难溶于水的特征,采用水洗分液法是最简便易行的方法,故选B项。
点评:分离某种混合物所采用的具体方法取决于混合物中各组分的不同性质。
15.(1)蒸馏方法(2)以一支小试管,打开分液漏斗的活塞,慢慢放出少量液体,往其中加入少量水,如果加水后,试管中的液体不分层,说明分液漏斗中下层是“水层”,反之,则上层是“水层”。
解析:(1)互不相溶的液体混合物,常用分液法分离,而沸点不同但又互溶的液体混合物,则用蒸馏方法分离;(2)本题是萃取的操作,静置分层后,若要检验哪一层液体是“水层”,可从分液漏斗中放出液体,然后进行溶解性试验,从而确定哪一层是“水层”。
点评:在拥有扎实的基础知识后,解一些训练,思维灵活性的题目很有好处。
14.(1)试管外壁应干燥,有水珠应擦干,试管里的液体不应超过试管容积的l/3。
(2)试管应用试管夹夹持,不能用尹拿着加热以免烫伤手。(试管夹夹持试管的方法是:把试管夹张开,由试管底部套上、取下,不得横套、横出)试管夹应夹在离试管口1/3处。加热时握持试管夹的方法是:右手三指(拇、食、中)握持试管夹长柄。
(3)加热时,应将试管倾斜,以与桌面成45°角为宜。
(4)加热时,应先使整个试管均匀受热,然后小心地在溶液的中下部加热(不要集中烧试管底部以防溶液喷出),并不断摇动试管,保持试管在灯焰内缓缓转动。
(5)试管底部应位于酒精灯的外焰部分(外焰温度最高),加热时不能使试管底部跟灯芯接触(因灯芯温度较低,较热的试管底部突然冷却容易炸裂)。
(6)试管口不要对着自己或别人,更不能把眼睛对着正在加热的试管口张望。
13.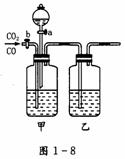 见图1-8将混合气体通过浓NaOH,进行洗气,则先将CO2吸收,将剩余的CO气体通过浓H2SO4即得到干燥的CO。再将盐酸滴入洗气瓶中将CO2放出,并通过浓硫酸进行干燥,即得到干燥的CO2。
见图1-8将混合气体通过浓NaOH,进行洗气,则先将CO2吸收,将剩余的CO气体通过浓H2SO4即得到干燥的CO。再将盐酸滴入洗气瓶中将CO2放出,并通过浓硫酸进行干燥,即得到干燥的CO2。
解析:要将CO2和CO分离并得到干燥的气体,可根据两种气体化学性质上的差异,选择适当的吸收剂,先将一种气体吸收,将另一种气体干燥,然后再将吸收的气体放出并进行干燥。所以,应先用浓NaOH将CO2吸收,生成Na2CO3。将不溶于NaOH的CO通过浓H2SO4干燥得到干燥的CO。再将盐酸滴入Na2CO3中,将生成的CO2通过浓硫酸干燥,从而得到干燥的CO2。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com