
2.第Ⅱ象限符号为“+、-”(△S>0、△H<0)时化学反应的方向--所有温度下反应均能自发进行
[例2]已知双氧水、水在298K、100kPa时的标准摩尔生成焓的数据如下:
|
物 质 |
△fH /kJ·mol-1 /kJ·mol-1 |
|
H2O(l) |
-258.8 |
|
H2O2(l) |
-191.2 |
|
O2(g) |
0 |
(1)试由以上数据计算双氧水发生分解反应的热效应。
(2)若双氧水发生分解反应生成液态水和氧气时,其△S==57.16J·mol-1·K-1
试判断该反应在常温下能否自发进行。若温度达到2000K时,反应能否自发进行。
[解析]
(1)根据△H ==H(产物)-H(反应物)得,△H ==2×(-258.8kJ·mol-1)+0-2×(-191.2kJ·mol-1)=== -135.2kJ·mol-1。
(2)在298K时,△H-T△S=-135.2kJ·mol-1-(298K×10-3×57.16kJ·mol-1·K-1) == -152.23 kJ·mol-1<0
∴该反应在常温下可自发进行。
温度达到2000K,且假定焓变和熵变不随温度变化而变化,△H-T△S=-135.2kJ·mol-1-(2000K×10-3×57.16kJ·mol-1·K-1)== -249.52kJ·mol-1<0
故△S>0、△H<0时,仅从符号上进行分析,无论温度如何变化,恒有△H-T△S<0,故化学反应的方向--所有温度下反应均能自发进行。
1.第Ⅰ象限符号为“+、+”(△S>0、△H>0)时化学反应的方向--高温下反应自发进行
[例1]石灰石的分解反应为:CaCO3(s)==CaO(s) +CO2(g)
其△H(298K)==178.2kJ·mol-1,△S(298K)==169.6J·mol-1·K-1
试根据以上数据判断该反应在常温下是否自发进行?其分解温度是多少?
[解析]
∵△H-T△S=178.2kJ·mol-1-298K×10×-3×169.6kJ·mol-1·K-1
==128kJ·mol-1>0
∴298K时,反应不能自发进行。即常温下该反应不能自发进行。
由于该反应是吸热的熵增加反应,升高温度可使△H-T△S<0,假设反应焓变和熵变不随温度变化而变化,据△H-T△S<0可知,T>△H/△S ==178.2kJ·mol-1/10×-3×169.6kJ·mol-1·K-1==1051K,即温度高于778℃时反应可自发进行。
4.焓变和熵变对反应方向的共同影响--“四象限法”判断化学反应的方向。
在二维平面内建立坐标系,第Ⅰ象限的符号为“+、+”,第Ⅱ象限的符号为“+、-”,第Ⅲ象限的符号为“-、-”,第Ⅳ象限的符号为“-、+”。借肋于数学坐标系四个象限的符号,联系焓变与熵变对反应方向的共同影响,可以从热力学的角度快速判断化学反应的方向。
在温度、压强一定的条件下,化学反应的方向的判据为:
△H-T△S<0 反应能自发进行
△H-T△S==0反应达到平衡状态
△H-T△S>0反应不能自发进行
 反应放热和熵增加都有利于反应自发进行。该判据指出的是化学反应自发进行的趋势。
反应放热和熵增加都有利于反应自发进行。该判据指出的是化学反应自发进行的趋势。
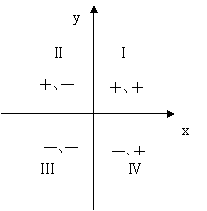
|

2.反应熵变与反应方向
(1)熵:描述大量粒子混乱度的物理量,符号为S,单位J·mol-1·K-1,熵值越大,体系的混乱度越大。
(2)化学反应的熵变(△S):反应产物的总熵与反应物总熵之差。
(3)反应熵变与反应方向的关系
①多数熵增加的反应在常温常压下均可自发进行。产生气体的反应、气体物质的量增加的反应,熵变都是正值,为熵增加反应。
②有些熵增加的反应在常温下不能自发进行,但在较高温度下则可自发进行。如碳酸钙的分解。
③个别熵减少的反应,在一定条件下也可自发进行。如铝热反应的△S== -133.8 J·mol-1·K-1,在点燃的条件下即可自发进行。
1.反应焓变与反应方向
(1)多数能自发进行的化学反应是放热反应。如氢氧化亚铁的水溶液在空气中被氧化为氢氧化铁的反应是自发的,其△H(298K)==-444.3kJ·mol-1
(2)部分吸热反应也能自发进行。
如NH4HCO3(s)+CH3COOH(aq)==CH3COONH4(aq)+CO2(g)+H2O(l),其△H(298K)== +37.30kJ·mol-1。
(3)有一些吸热反应在常温下不能自发进行,在较高温度下则能自发进行。如碳酸钙的分解。
因此,反应焓变不是决定反应能否自发进行的唯一依据。
4.活化能:对基元反应而言,活化分子的平均能量与普通反应物分子的平均能量之差叫该反应的活化能(用Ea表示,其单位为kJ/mol)。活化能越大,反应越难进行。
催化剂能降低化学反应的活化能,增大活化分子的百分数,进而增大化学反应速率。催化剂具有选择性。
解释化学反应速率快慢的链条思维:活化能→活化分子→有效碰撞→化学反应速率。
 影响 影响外因 |
单位体积内 |
有效碰撞次数 |
化学反应速率 |
||
|
分子总数 |
活化分子数 |
活化分子百分数 |
|||
|
增大反应物浓度 |
增加 |
增加 |
不变 |
增加 |
加快 |
|
增大压强 |
增加 |
增加 |
不变 |
增加 |
加快 |
|
升高温度 |
不变 |
增加 |
增大 |
增加 |
加快 |
|
使用催化剂 |
不变 |
增加 |
增大 |
增加 |
加快 |
|

[例1](2010福建卷,12)化合物Bilirubin在一定波长的光照射下发生分解反应,反应物尝试随反应时间变化如右图所示,计算反应4~8 min间的平均反应速率和推测反应16 min 反应物的浓度,结果应是

A 2.5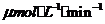 和2.0
和2.0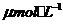
B 2.5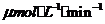 和2.5
和2.5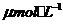
C 3.0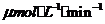 和3.0
和3.0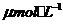
D 3.0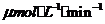 和3.0
和3.0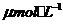
解析:本题考察化学反应速率的计算
第8秒与第4秒时反应物浓度差△C为10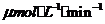 ,
,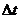 为4秒,所以在4~8
为4秒,所以在4~8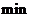 间的平均反应速率为2.5
间的平均反应速率为2.5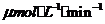 ,可以排除CD两个答案;图中从0
,可以排除CD两个答案;图中从0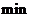 开始到8
开始到8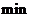 反应物浓度减低了4倍,根据这一幅度,可以推测从第8
反应物浓度减低了4倍,根据这一幅度,可以推测从第8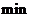 到第16分也降低4倍,即由10
到第16分也降低4倍,即由10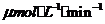 降低到2.5
降低到2.5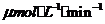 ,因此推测第16
,因此推测第16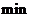 反应物的浓度为2.5
反应物的浓度为2.5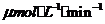 ,所以可以排除A而选B
,所以可以排除A而选B
答案:B
[例2](2010全国卷1,27)
(15分)在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为
C分别在三种不同实验条件下进行,它们的起始浓度均为 、
、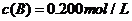 及
及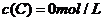 。反应物A的浓度随时间的变化如下图所示。
。反应物A的浓度随时间的变化如下图所示。
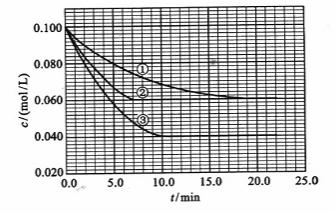
请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
②_______________;
③_______________;
(2)实验②平衡时B的转化率为_________;实验③平衡时C的浓度为____________;
(3)该反应的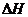 _________0,判断其理由是__________________________________;
_________0,判断其理由是__________________________________;
(4)该反应进行到4.0min时的平均反应速度率:
实验②: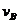 =__________________________________;
=__________________________________;
实验③: =__________________________________。
=__________________________________。
[解析](1)②使用了(正)催化剂;理由:因为从图像可看出,两者最终的平衡浓度相同,即最终的平衡状态相同,而②比①所需要的时间短,显然反应速率加快了,故由影响反应速率和影响平衡的因素可知是加入(正)催化剂;③升高温度;理由:因为该反应是在溶液中进行的反应,所以不可能是改变压强引起速率的改变,又由于各物质起始浓度相同,故不可能是改变浓度影响反应速率,再由于③和①相比达平衡所需时间短,平衡时浓度更小,故不可能是改用催化剂,而只能是升高温度来影响反应速率的
(2)不妨令溶液为1L,则②中达平衡时A转化了0.04mol,由反应计量数可知B转化了0.08mol,所以B转化率为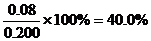 ;同样在③中A转化了0.06mol,则生成C为0.06mol,体积不变,即平衡时C(c)=0.06mol/L
;同样在③中A转化了0.06mol,则生成C为0.06mol,体积不变,即平衡时C(c)=0.06mol/L
(3) 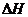 ﹥0;理由:由③和①进行对比可知升高温度后A的平衡浓度减小,即A的转化率升高,平衡向正方向移动,而升温是向吸热的方向移动,所以正反应是吸热反应,
﹥0;理由:由③和①进行对比可知升高温度后A的平衡浓度减小,即A的转化率升高,平衡向正方向移动,而升温是向吸热的方向移动,所以正反应是吸热反应,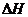 ﹥0
﹥0
(4)从图上读数,进行到4.0min时,实验②的A的浓度为:0.072mol/L,则△C(A)=0.10-0.072=0.028mol/L,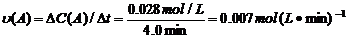 ,∴
,∴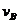 =2
=2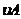 =0.014mol(L·min)-1;进行到4.0mi实验③的A的浓度为:0.064mol/L:△C(A,)
=0.10-0.064=0.036mol/L,
=0.014mol(L·min)-1;进行到4.0mi实验③的A的浓度为:0.064mol/L:△C(A,)
=0.10-0.064=0.036mol/L,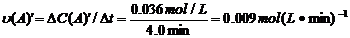 ,∴
,∴ =
=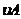 =0.0089mol(L·min)-1
=0.0089mol(L·min)-1
[答案](1)②加催化剂;达到平衡的时间缩短,平衡时A的浓度未变
③温度升高;达到平衡的时间缩短,平衡时A的浓度减小
(2)40%(或0.4);0.06mol/L;(3)﹥;升高温度向正方向移动,故该反应是吸热反应
(4)0.014mol(L·min)-1;0.008mol(L·min)-1
[命题意图]考查基本理论中的化学反应速率化学平衡部分,一些具体考点是:易通过图像分析比较得出影响化学反应速率和化学平衡的具体因素(如:浓度,压强,温度,催化剂等)、反应速率的计算、平衡转化率的计算,平衡浓度的计算,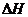 的判断;以及计算能力,分析能力,观察能力和文字表述能力等的全方位考查。
的判断;以及计算能力,分析能力,观察能力和文字表述能力等的全方位考查。
[点评]本题所涉及的化学知识非常基础,但是能力要求非常高,观察和分析不到位,就不能准确的表述和计算,要想此题得满分必须非常优秀才行!此题与2009年全国卷II理综第27题,及安微卷理综第28题都极为相似,有异曲同工之妙,所以对考生不陌生!
|

第2课时 化学反应的方向及判据
2.影响反应速率的因素
内因:反应物的性质是反应速率大小的决定因素。
外因:主要因素有浓度、温度、压强、催化剂等。
(1)浓度:其它条件不变时,增大反应物浓度,化学反应速率加快。
(2)温度:其它条件不变时,升高温度,化学反应速率加快。一般来说,温度每升高10℃,反应速率增大为原来的2-4倍。
(3)压强:其它条件不变时,增大压强,对于有气体物质参加的化学反应,反应速率加快。
(4)催化剂:使用正催化剂,能加快反应速率。未特别指明时,均指正催化剂。
1.化学反应速率的表示方法:通常用单位时间内反应物浓度的减少或者生成物浓度的增加来表示化学反应速率。单位:mol/L·s ;mol/L·min ;mol/L·h等。
对于任一化学反应:aA +bB==cC +dD可用υ(A)、υ(B)、υ(C)、υ(D)表示其速率,则有υ(A):υ(B):υ(C):υ(D)== a:b:c:d,即化学反应速率之比等于化学方程式中各物质的系数之比(还可等于其学其浓度变化之比或物质的量变化之比)。
2、熵:描述体系滋乱度的物理理 单位:J.mol-1 .k-1 符号S
影响熵的因素:①同一条件下,不同物质熵不同②同一物质,聚集状态不同熵不同S(g)>S(l)>S(s)
反应的熵变(△S):△S=S反应产物-S反应物
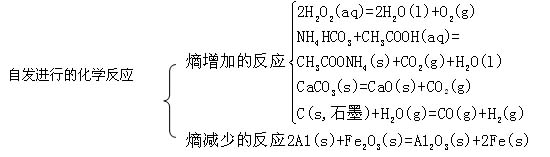
T、P一定,反应焓变和熵变共同影响反应方向,反应方向判据:△H-T△S<0 反应能自发进行;△H-T△S=0 反应达到平衡状态;△H-T△S>0 反应不能自发进行
|

第1课时 化学反应速率
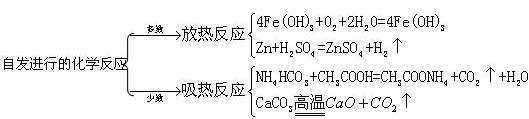
1、反应焓变是与反应能否自发进行有关的一个因素,但不是惟一因素
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com