
25.(6分) 某溶液中含有SO42-、CO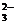 、OH-三种阴离子,如果只取一次该溶液,分别将三种离子检验出来,则检验顺序是:
、OH-三种阴离子,如果只取一次该溶液,分别将三种离子检验出来,则检验顺序是:
(1) 先检验____________离子,加入的试剂是_______________________________;
(2) 再检验____________离子,加入的试剂是_______________________________;
(3) 最后检验__________离子,加入的试剂是_______________________________。
24.(10分)
(1) 标出指定元素的化合价: ZnSO4 (S元素) KClO (Cl元素) NH4Cl(N元素)
(2) 实验室中所用少量氯气可用二氧化锰和浓盐酸共热制取氯气,反应的化学方程式为:
4HCl(浓)+MnO2 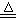 Cl2↑+
MnCl2
+ 2H2O
,该反应 (填“是”或“否”)氧化还原反应,判断依据是
。
Cl2↑+
MnCl2
+ 2H2O
,该反应 (填“是”或“否”)氧化还原反应,判断依据是
。
若是氧化还原反应请回答:MnO2 做 剂, 元素被氧化。
(3)98 g H2SO4中含O的物质的量为 ;含S的数目为 ,
含H的质量为
23.(12分)
(1)下列物质能导电的是 ,属于电解质的是 ,属于非电解质的是 。
①水银 ②烧碱 ③大理石 ④氯化钠晶体 ⑤盐酸 ⑥干冰 ⑦蔗糖
(2)按要求写出下列方程式:
① 氢氧化钡电离的电离方程式:
② 小苏打电离的电离方程式:
③ 碳酸钙与盐酸反应的离子方程式:
22. 实验中的下列操作正确的是( )
A.用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中
B.Ba(NO3)2 溶于水,可将含有Ba(NO3)2 的废液倒入水槽中,再用水冲入下水道
C.用蒸发方法使NaCl 从水溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干
D.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
2008-2009学年度上学期郑中钧中学
新课标高一化学必修1-期中考试
班别 学号 姓名 成绩
第II卷(非选择题 共44分)
21. 下列化学变化中,需加入还原剂才能实现的是 ( )
A.CO2→ CO B.C→CO2 C.CuO→Cu D.H2SO4→BaSO4
20. 下列溶液中Cl- 的物质的量浓度与50 mL 1 mol·L-1的AlCl3溶液中Cl-的物质的量浓度相等的是( )
A. 150 mL 1 mol·L-1的NaCl B. 75 mL 1.5 mol·L-1的CaCl2
C. 150 mL 3 mol·L-1的KCl D. 75 mL 2 mol·L-1的NH4Cl
19. 下列离子方程式与化学反应事实一致的是( )
A.硫酸铜溶液与氢氧化钡溶液反应 :Cu2+ + 2OH- == Cu(OH)2↓
B.石灰石溶于盐酸:CO32- + 2H+ == H2O +CO2↑
C.硫酸溶液与氢氧化钾溶液反应:H+ + OH- == H2O
D.硝酸银溶液与氯化钠溶液反应:AgNO3 + Cl- == AgCl↓+NO3-
18. 下列离子在溶液中可大量共存,并能形成无色溶液的一组是( )
A.K+、Na+、OH-、Cl- B.Ba2+、Cu2+、NO3-、SO42-
C.Mg2+、Na+、OH-、SO42- D.H+、Ba2+、NO3-、OH-
17. 用NA表示阿伏德罗常数,下列叙述正确的是( )
A.标准状况下,22.4L O2 含有的分子数为1 NA
B.常温常压下, 1.06g Na2CO3含有的Na+ 离子数为0.02 NA
C.通常状况下,NA 个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为1 NA
16. 能用H+ + OH- = H2O表示的是 ( )
A. 氢氧化钡和稀硫酸 B. 氢氧化铜和稀硝酸
C. 醋酸和氢氧化钾 D. 氢氧化钠和盐酸
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com