
2£®(ÎÂÖƯÊĐÊ®Đ£ÁªºÏ̀å¸ßÈưÁª¿¼)2007Äê¹ú¼̉Öʼ́×ܾÖÂÁºÏ½đ³é¼́ºÏ¸ñÂÊԼΪ90%¡£̉ÑÖª¹ú¼̉ĐĐ̉µ±ê×¼ÖĐÖưỐÂÁºÏ½đµÄ¸÷³É·ÖµÄÖÊÁ¿·ÖÊưΪ£ºSi£4.5%-5.5%£¬Cu£1.0%-1.5%£¬Mg£0.4%-0.6%£¬ÆäÓàΪAl¡£
ÏÖ¶ÔijƷÅƵÄÖưỐÂÁºÏ½đÖĐËùº¬µÄËÄÖֳɷÖ×÷ÈçϵÄʵÑé¼́²â£º
¢Ù³ÆÈ¡18.0gÖưỐÂÁºÏ½đÑùÆ·£¬·Ö³ÉµÈÖÊÁ¿µÄA¡¢BÁ½·Ư¡£Ị̈A·Ư¼ÓÈë×ăÁ¿NaOHÈÜ̉º£¬B·Ư¼ÓÈë×ăÁ¿µÄÏ¡ÑÎËá¡£(̉ÑÖª£ºSi+2NaOH+H2O£½Na2SiO3+2H2¡ü)
¢Ú´ưÁ½·Ư·´Ó¦Îﶼ³ä·Ö·´Ó¦Ö®ºó£¬³ÆµĂÂËÔüÖÊÁ¿Ïà²î0.512g£¬ÊƠ¼¯µĂµ½µÄÁ½·ƯÆø̀åµÄ̀å»ưÏà²î851.2mL(±ê×¼×´¿öÏÂ)¡£
ÊԻشđÏÂÁĐÎỀ⣺
¢ÅÑùÆ·ÖĐSiºÍMgµÄÎïÖʵÄÁ¿·Ö±đÊǶàÉÙ¡£
¢Æͨ¹ư¼ÆËăÅĐ¶Ï¸ĂÆ·ÅƵÄÖưỐÂÁºÏ½đÊÇ·ñΪºÏ¸ñ²úÆ·(̉»Ïî²»´ï±ê¼´Îª²»ºÏ¸ñ²úÆ·)
´đ°¸ ¢ÅÉè9gÑùÆ·ÖĐËùº¬SiµÄÎïÖʵÄÁ¿Îªx£¬MgµÄÎïÖʵÄÁ¿Îªy¡£
 ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
28x£24y£½0.512¡¡
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
28x£24y£½0.512¡¡
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
2x£y£½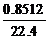
¡¡¡¡ ½âµĂ£ºx£½0.02mol£¬y£½0.002mol
¡¡¡¡ ¢Æ̣̉ΪºÏ½đÖĐSiµÄ°Ù·Öº¬Á¿Îª£º0.02mol¡Á28g/mol¡Â9g¡Á100%£½6.2%£¬³¬¹ư¹ú¼̉±ê×¼£¬¹Ê¸ĂÖưỐÂÁºÏ½đÊôÓÚ²»ºÏ¸ñ²úÆ·¡£
1.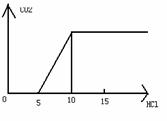 (ɽ¶«Ê¡ÁÙăđ̉»ÖĐ2009½́¸ßÈưÉÏѧÆÚÆÚÖĐ¿¼ÊÔ)(6·Ö)ͼ±íʾÍùijNa2CO3ÈÜ̉ºÖеÎÈëÏ¡ÑÎËá²úÉúCO2µÄ¹ư³̀£º
(ɽ¶«Ê¡ÁÙăđ̉»ÖĐ2009½́¸ßÈưÉÏѧÆÚÆÚÖĐ¿¼ÊÔ)(6·Ö)ͼ±íʾÍùijNa2CO3ÈÜ̉ºÖеÎÈëÏ¡ÑÎËá²úÉúCO2µÄ¹ư³̀£º
¢ÅĐ´³öaµẳÔÇ°·¢Éú·´Ó¦µÄ»¯Ñ§·´Ó¦·½³̀ʽ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¢Æ Đ´³öaµăµ½bµă·¢Éú·´Ó¦µÄÀë×Ó·´Ó¦·½³̀ʽ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¢ÇÈôijNa2CO3ÈÜ̉ºÖĐº¬m moLNa2CO3£¬µÎÈë̉»¶¨Á¿µÄÏ¡ÑÎËᣬǡºĂʹ¡¡
ÈÜ̉ºÖĐCl£ºÍHCO3£µÄÎïÖʵÄÁ¿Ö®±ÈΪ2£º1£¬ỘµÎÈëµÄÑÎËáÖĐHClµÄ¡¡
ÎïÖʵÄÁ¿µÈÓÚ¡¡¡¡¡¡ moL(ÓĂm±íʾ)¡£
´đ°¸ ¢ÅNa2CO3+HCl£½NaCl+Na2CO3
¢ÆHCO3£+H+£½H2O+CO2
¢Ç4m/3(Ă¿¸ö2·Ö¹²6·Ö)
1£®C¡¡ 2£®D¡¡ 3£®A¡¡ 4£®D¡¡ 5£®D¡¡ 6£®B¡¡ 7£®C
½üÈưÄêµäĐÍÁª¿¼̀â»ă±à
7£®ÈổÔ¦Ø1ºÍ¦Ø2·Ö±đ±íʾŨ¶ÈΪa mol¡¤L£1ºÍb mol¡¤L£1°±Ë®µÄÖÊÁ¿·ÖÊư£¬Ç̉Öª2a£½b£¬ỘÏÂÁĐÍƶÏƠưÈ·µÄÊÇ(°±Ë®µÄĂܶȱȴ¿Ë®µÄĐ¡)
A£®2¦Ø1£½¦Ø2¡¡¡¡ ¡¡¡¡¡¡B£®2¦Ø2£½¦Ø1¡¡¡¡ ¡¡¡¡¡¡C£®¦Ø2£¾2¦Ø1¡¡¡¡ ¡¡¡¡¡¡D£®¦Ø1<¦Ø2<2¦Ø1
6£®ÔÚ100 mL 0.10 mol/LµÄAgNO3ÈÜ̉ºÖĐ¼ÓÈë100 mLÈÜÓĐ2.08 g BaCl2µÄÈÜ̉º£¬ÔÙ¼ÓÈë100 mLÈÜÓĐ0.010 mol CuSO4 ¡¤ 5H2OµÄÈÜ̉º£¬³ä·Ö·´Ó¦¡£ÏÂÁĐ˵·¨ÖĐƠưÈ·µÄÊÇ
¡¡ A£®×îÖƠµĂµ½°×É«³ÁµíºÍÎ̃É«ÈÜ̉º
¡¡ B£®×îÖƠµĂµ½µÄ°×É«³ÁµíÊǵÈÎïÖʵÄÁ¿µÄÁ½ÖÖ»¯ºÏÎïµÄ»́ºÏÎï
¡¡ C£®ÔÚ×îÖƠµĂµ½µÄÈÜ̉ºÖĐ£¬Cl£µÄÎïÖʵÄÁ¿Îª0.02 mol
¡¡ D£®ÔÚ×îÖƠµĂµ½µÄÈÜ̉ºÖĐ£¬Cu2+µÄÎïÖʵÄÁ¿Å¨¶ÈΪ0.10 mol/L
4£®½«±ê×¼×´¿öϵÄaÉưÂÈ»¯ÇâÆø̀åÈÜÓÚ100¿ËË®ÖĐ£¬µĂµ½µÄÑÎËáµÄĂܶÈΪb¿Ë/ºÁÉư£¬Ộ¸ĂÑÎËáµÄÎïÖʵÄÁ¿µÄŨ¶È(mol/L)ÊÇ
|
|||||||||
|
|
|
|||||||
|

|


|

|
|
A£®0¡æ-10¡æ¡¡B£®10¡æ-20¡æ¡¡
C£®20¡æ-30¡æ¡¡ D£®30¡æ-40¡æ
3£®300ºÁÉưijŨ¶ÈµÄNaOHÈÜ̉ºÖĐº¬ÓĐ60¿ËÈÜÖÊ¡£ÏÖÓûÅäÖÆ1Ħ/ÉưNaOHÈÜ̉º£¬Ó¦È¡ÔÈÜ̉ºÓëƠôÁóË®µÄ̀å»ư±ÈԼΪ
A£®1©U4¡¡¡¡ ¡¡¡¡B£®1©U5¡¡¡¡¡¡ ¡¡¡¡C£®2©U1¡¡¡¡¡¡ ¡¡D£®2©U3
2£®ÔÚ10mL0.01mol/LµÄ´¿¼îÈÜ̉ºÖĐ£¬²»¶Ï½Á°è²¢ÖđµÎ¼ÓÈë1.2mL 0.05mol/LÑÎËᣬÍêÈ«·´Ó¦ºóÔÚ±ê×¼×´¿öÏÂÉú³É¶₫Ñơ»¯̀¼µÄ̀å»ưΪ
A£®1.34mL¡¡ ¡¡¡¡B£®2.240mL¡¡ ¡¡¡¡C£®0.672mL¡¡ ¡¡¡¡ D£®0mL
1£®ĂܶÈΪ0.91¿Ë/ÀåĂ×3µÄ°±Ë®£¬ÖÊÁ¿°Ù·Ö±ÈŨ¶ÈΪ25%(¼´ÖÊÁ¿·ÖÊưΪ0.25)£¬¸Ă°±Ë®ÓõÈ̀å»ưµÄˮϡÊͺó£¬ËùµĂÈÜ̉ºµÄÖÊÁ¿°Ù·Ö±ÈŨ¶ÈΪ
A£®µÈÓÚ12.5%¡¡¡¡¡¡¡¡ B£®´óÓÚ12.5%¡¡¡¡¡¡¡¡ C£®Đ¡ÓÚ12.5%¡¡¡¡¡¡¡¡ D£®Î̃·¨È·¶¨
4¡¢̉ÑÖª»́ºÏÎï¸÷³É·ÖµÄĦ¶ûÖÊÁ¿ºÍÔÚ»́ºÏ̀åϵÄÚµÄÎïÖʵÄÁ¿·ÖÊư»̣̀å»ư·ÖÊư¡£
M(»́)£½Ma¡ÁA%+ Mb¡ÁB% + Mc¡ÁC% +--
µäĐ͸߿¼̀â»ă±à
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com