
2. 了解电离平衡概念,能描述弱电解质在水溶液中的电离平衡。
1. 了解强电解质、弱电解质在水溶液中电离程度的差异,能判断常见的强电解质和弱电解质。
21.(1) Na<Al<Si<N(2分)
(2)高 、 NaCl为离子晶体而SiCl4为分子晶体(2分)
(3) sp2 ,平面正三角形 (2分)
(4) [Ar] 3d104s1 , [Cu(NH3)4]2+.(2分)
(5) Cu3 N (2分)
(6) AlN , 共价键 (2分)
20.(1) F_________________________________;J_______________________________。
(2)E→F ____取代_____ ; H→L________缩聚___。
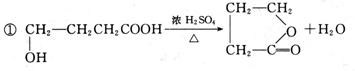
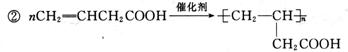 ①H→I_________________________________________________________________;
①H→I_________________________________________________________________;
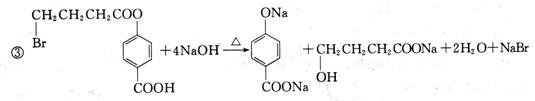 ②J→K_______________________________________________________________;
②J→K_______________________________________________________________;
③A→B+C___________________________________________________________。
19. (1)___ N2、H2 ______;
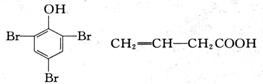 (2)__ BC
__;
(2)__ BC
__;
(3)_b __, a 。
(4) ①<②<③
17.(1)B HNO3 、C Ag ;
(2) 氧气 、 氢氧化铜悬浊液(或其他合理答案) ;
(3) ① 4Ag++2H2O = 4Ag↓+4H++O2↑
②HCHO+4Ag(NH3)2++4OH- CO32-+2NH4++2Ag↓+2NH3+H2O
CO32-+2NH4++2Ag↓+2NH3+H2O
w.w.w.k.s.5.u.c.o18.(1) 氯化铵 。
(2)原因是降低KH2PO4溶解度,使其析出后,降低了生成物浓度,(同时生成的HCl与、 三正丁胺反应,也降低了HCl的浓度),使平衡向正反应方向移动。
、 分离出氯化氢(其他合理答案均给分) 。
16.(1) 10-12 。
开始时Cl-抑制了AgCl的溶解,但后来Cl-浓度增大使AgCl形成络合物
(2) b
(3) AgI的溶解度小于AgCl的溶解度
(4) 白色沉淀溶解,形成无色溶液
、 AgCl+2NH3=Ag(NH3)2++ Cl-
15. (1) NH4[CuCl2] =CuCl↓+NH4Cl ,
(2) 避免CuCl溶于水而造成损耗,洗去晶体表面的杂质离子及水分 。
(3) 氯化铵溶于水吸收大量热量,造成反应液温度降低。 ,
、 a或c
(4)蒸馏
21.(12分)已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数
A<B<C<D<E<F。其中A原子核外有三个未成对电子;化合物B2E的晶体为离
子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属
元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数
与B相同,其余各层电子均充满。请根据以上信息,回答下列问题:(答题时,A、
B、C、D、E、F用所对应的元素符号表示)
(1)A、B、C、D的第一电离能由小到大的顺序为 。(用元素符
号表示)
(2)B的氯化物的熔点比D的氯化物的熔点 (填高或低),理由
是 。
(3)A的最高价氧化物对应的水化物分子中其中心原子采取 杂化,E的
最高价氧化物分子的空间构型是 。
(4)F的核外电子排布式是 ,F的高价离子与A的简单氢化物形成的配离
 子的化学式为 .
子的化学式为 .
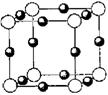
(5)A、F形成某种化合物的晶胞结构如图所示,则其化学式
为 ;(每个球均表示1个原子)
(6)A、C形成的化合物具有高沸点和高硬度,是一种新型无机非
金属材料,则其化学式为 ,其晶体中所含的
化学键类型为 。
周练答案(2.22)
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
A |
A |
B |
B |
C |
C |
D |
D |
|
9 |
10 |
11 |
12 |
13 |
14 |
|
|
|
C、D |
C、D |
C、D |
A |
B |
C |
每空2分
20.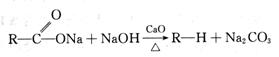 已知:Ⅰ.
已知:Ⅰ.
Ⅱ.氯苯在氢氧化钠水溶液中很难水解生成苯酚。
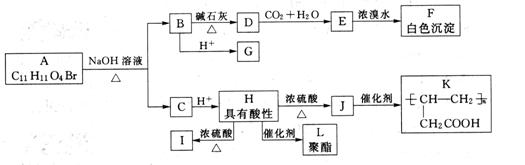 某有机物A和其他有机物存在如下图所示的转化关系:
某有机物A和其他有机物存在如下图所示的转化关系:
又知:A的水溶液显酸性,遇FeCl3溶液不显色,A分子结构中不含甲基,含苯环,苯环上的一氯代物只有两种;I是五元环状化合物,I和J互为同分异构体;K和L都是医用高分子材料。
试回答下列问题:
(1) 写出F、J的结构简式:
F_________________________________;J_______________________________。
(2)写出下列反应的类型:E→F _______________ ; H→L_________________。
(2) 写出下列反应的化学方程式:
①H→I_________________________________________________________________;
②J→K__________________________________________________________________;
③A→B+C______________________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com