
9.如图装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色.下列说法中不正确的是 ( )
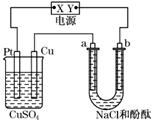
A.X是正极,Y是负极
B.X是负极,Y是正极
C.CuSO4溶液的pH逐渐减小
D.NaCl溶液的pH逐渐变大
解析:根据实验现象知道,b极是电解池的阴极,则X是正极,Y是负极.烧杯内电解CuSO4溶液,产物为Cu、O2和H2SO4,电解后溶液酸性增强,U形管电解NaCl溶液,产物为Cl2、H2和NaOH,溶液的碱性增强.
答案:B
8.按如图装置实验,若x轴表示流入阴极的电子的物质的量,则y轴可表示( )
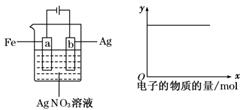
①c(Ag+) ②c(AgNO3) ③a棒的质量 ④b棒的质量 ⑤溶液的pH
A.①③ B.③④
C.①②④ D.①②⑤
解析:该电解池中随着电解的进行,c(Ag+)不变,c(AgNO3)不变,溶液的pH不变,阳极反应为:Ag-e-===Ag+;阴极反应为:Ag++e-===Ag.
答案:D
7.金属镍有广泛的用途.粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备
高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+) ( )
A.阳极发生还原反应,其电极反应式:Ni2++2e-===Ni
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt
解析:用电解法制备高纯度的镍时,用纯镍作阴极,粗镍作阳极,含Ni2+的溶液作电解质溶液.
其中阳极反应式:Zn-2e-===Zn2+,Fe-2e-===Fe2+,Ni-2e-===Ni2+;阴极反应式:Ni2++2e-===Ni.因此电解过程中,阳极质量的减少和阴极质量的增加并不相等.电解质溶液中存在的阳离子有Zn2+、Fe2+、Ni2+.阳极泥中只有Cu和Pt.
答案:D
6.500 mL KNO3和Cu(NO3)2的混合溶液中c(NO)=6 mol/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是 ( )
A.原混合溶液中c(K+)为2 mol/L
B.上述电解过程中共转移2 mol电子
C.电解得到的Cu的物质的量为0.5 mol
D.电解后溶液中c(H+)为2 mol/L
解析:该溶液用石墨作电极电解,阳极反应为:4OH--4e-===2H2O+O2↑,生成1
 mol氧气失去4
moL电子,阴极反应先为:Cu2++2e-===Cu,后为:2H++2e-
mol氧气失去4
moL电子,阴极反应先为:Cu2++2e-===Cu,后为:2H++2e-
===H2↑,生成1 mol氢气得2 mol电子,而阴阳两极得失电子数相等,故Cu2+得2 mol电子生成1 mol铜,原溶液中c(Cu2+)=2 mol/L,由电荷守恒式c(K+)+2c(Cu2+)=c(NO)得c(K+)为2 mol/L[Cu(NO3)2水解的c(H+)忽略不计].电解后c(H+)应为4 mol/L.
答案:A
5.(2010·潍坊模拟)现将氯化铝溶液蒸干灼烧并熔融后用铂电极进行电解,下列有关电极产物的判断正确的是 ( )
A.阴极产物是氢气 B.阳极产物是氧气
C.阴极产物是铝和氧气 D.阳极产物只有氯气
解析:将氯化铝溶液蒸干灼烧得到Al2O3,电解熔融的Al2O3,阳极为O2-放电,阳极产物为氧气;阴极为Al3+放电,阴极产物为Al.
答案:B
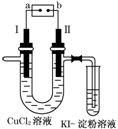
4.如图为用惰性电极电解CuCl2溶液并验证其产物的实验装
置,则下列说法不正确的是 ( )
A.电源a极为负极
B.KI-淀粉溶液会变蓝色
C.若加入适量CuCl2可使电解后的溶液恢复原状态
D.电极Ⅰ上发生的电极反应为:Cu-2e-===Cu2+
解析:用惰性电极电解CuCl2溶液,阳极反应:2Cl--2e-===Cl2↑,故Ⅱ为阳极,电源b为正极,a为负极,阴极(Ⅰ)的反应为Cu2++2e-===Cu.
答案:D
3. 某溶液中含有两种溶质NaCl和H2SO4,它们的物质的量之比为
某溶液中含有两种溶质NaCl和H2SO4,它们的物质的量之比为
3∶1.用石墨做电极电解该混合溶液时,根据电极产物,可明显分
为三个阶段.下列叙述不正确的是 ( )
A.阴极自始至终只析出H2
B.阳极先析出Cl2,后析出O2
C.电解最后阶段为电解水
D.溶液pH不断增大,最后为7
解析:由题意知:n(H+)∶n(Cl-)=2∶3,在阴极放电的是H+,在阳极放电的是Cl-,Cl-放电完后是OH-.因此反应开始在两极放电的是H+、Cl-,相当于电解盐酸.由H2SO4电离的H+放电完后,在两极放电的是由水电离的H+和剩余的Cl-,相当于电解NaCl的水溶液.Cl-放电完后,在两极放电的是由水电离的H+和OH-,相当于电解水.故A、B、C是正确的.溶液pH的变化是不断增大,但最后溶质是NaOH和Na2SO4,pH不会为7.
答案:D
2.如图装置分别通电一段时间后,溶液的质量增加的是 ( )

解析:A池中的反应是:2H2O2H2↑+O2↑,B池中的反应为:CuCl2Cu+Cl2↑,A、B两池中溶液质量都减少;C池是电镀池,溶液质量不变;D池中的反应是2Ag+Cu(NO3)22AgNO3+Cu,溶液的质量增加.
答案:D
1.下列有关用惰性电极电解AgNO3溶液一段时间后的说法正确的是 ( )
A.电解过程中阳极质量不断增加
B.电解过程中溶液的pH不断升高
C.此时向溶液中加入适量的Ag2O固体可使溶液恢复到电解前的状况
D.电解后两极产生的气体体积比为2∶1
解析:用惰性电极电解AgNO3溶液,总反应式为:4AgNO3+2H2O4Ag+O2↑+4HNO3.在阴极上有Ag生成,所以阴极质量不断增加.电解产生了HNO3,pH不断减小.加入Ag2O后,Ag2O+2HNO3===2AgNO3+H2O,恰好可使溶液恢复至电解前的状况.阴极析出银,不产生气体.
答案:C
珍爱生命
自救自护 互帮互助
积极进取 拥抱平安
我的做课完毕,谢谢各位领导!
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com