
13.某硫酸厂周围的空气含有较多二氧化硫,为了测定空气中二氧化硫的体积分数做了如下实验:取上述标准状况下的空气1L(内含N2、O2、SO2、CO2)慢慢通过足量溴水,然后在此溶液中加入过量的BaCl2溶液,产生白色沉淀,将沉淀洗净、干燥后称重为0.233g。请回答:
(1)通入足量溴水的目的是: 。
(2)加入过量BaCl2溶液的目的是: 。
(3)过滤后,若在滤液中加K2SO4溶液,有白色沉淀产生,证明: 。
(4)用蒸馏水洗涤沉淀2-3次,若在洗液中加入AgNO3溶液,无沉淀出现,证明: 。
(5)空气中,SO2的体积分数为 。
12.有甲、乙、丙三瓶等体积、等物质的量浓度的硫酸,将甲用水稀释,在乙中加少量BaCl2溶液,丙维持原状。然后分别跟同一种NaOH溶液反应至完全时,所需NaOH溶液的体积( )
A.甲=乙=丙 B.丙>甲>乙 C.甲=丙>乙 D.无法比较
11.下列物质中既能与浓硫酸反应也能与氢氧化钠溶液反应的是( )
A.Cl2 B.SO2 C.(NH4)2S D.Na2SO3
10.根据反应:2H2SO4(稀、热)+2Cu+O2(足量)  2CuSO4+2H2O,判断下列说法正确的是( )
2CuSO4+2H2O,判断下列说法正确的是( )
A.铜可以和稀硫酸发生氧化还原反应 B.铜只有在稀、热硫酸中才能被氧气氧化
C.反应中H2SO4只起了酸的作用没有起氧化剂作用 D.上述反应中若不加热也能发生
9.碳跟浓硫酸共热产生的气体和铜跟浓硝酸反应产生的气体同时通入盛有足量硝酸钡溶液的洗气瓶中,下列有关说法正确的是( )
A.洗气瓶中产生的沉淀是碳酸钡 B.在导管出来的气体中无二氧化碳
C.洗气瓶中产生的沉淀是硫酸钡 D.在导管口有红棕色气体出现
8.等体积硫酸铝、硫酸锌、硫酸钠溶液分别与足量的氯化钡溶液反应。若生成的硫酸钡沉淀的质量比为1:2:3,则三种硫酸盐的物质的量浓度比为( )
A.1:2:3 B.1:6:9 C.1:3:3 D.1:3:6
7.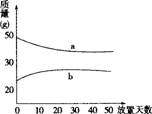 浓硫酸和2mol/L的稀硫酸,在实验室中敞口放置。它们的质量和放置天数的关系如右图,分析a、b曲线变化的原因是( )
浓硫酸和2mol/L的稀硫酸,在实验室中敞口放置。它们的质量和放置天数的关系如右图,分析a、b曲线变化的原因是( )
A.a升华、b冷凝 B.a挥发、b吸水
C.a蒸发、b潮解 D.a冷凝、b吸水
6.向50mL 18mol·L-1的硫酸中加入足量的铜片并加热,被还原的硫酸的物质的量( )
A.等于0.9mol B.大于0.45mol、小于0.9m01 C.等于0.45mol D.小于0.45mol
5.检验某未知溶液中是否含有SO42-的下列操作中最合理的是( )
A.加入硝酸酸化了的硝酸钡溶液 B.先加硝酸酸化,再加硝酸钡溶液
C.先加盐酸酸化,再加氯化钡溶液 D.加入盐酸酸化了的氯化钡溶液
4.为确证碳与浓H2SO4反应产生的气体中含有CO2时,不需要的试剂是( )
A.澄清石灰水 B.KMnO4溶液 C.品红试液 D.NaOH溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com